Adolescente con pérdida brusca de la agudeza visual
Adolescente con pérdida brusca de la agudeza visual
G. Perkal Rug.
Pediatra. Hospital Santa Caterina. I.A.S. Girona Servicio de Pediatría. Consulta de Adolescentes.
Adolescere 2017; V (2): 104-109
Resumen
|
La Esclerosis Múltiple (EM) Pediátrica se define como el inicio de la enfermedad antes de los 18 años. Se considera una enfermedad rara a esta edad que puede conducir a déficits tanto físicos como cognitivos. Su prevalencia es: 1.35-2.35 / 100.000 niños. 5% en <18 años; 3% en < 16 años; 1% en < 10 años. Predomina en el sexo femenino en una relación de 2.8. En pediatría destacan dos formas clínicas de presentación: a) Encefalopatía (16-20%), en menores de 11 años; b) Síndrome clínico aislado: neuritis óptica, mielitis transversa, síndrome cortical. Dado que la adolescencia es una época de la vida en la que es frecuente el debut de enfermedades con una base etiopatogénica de tipo inmunológico, presentamos este caso clínico, en el que destaca una clínica de aparición aguda y sugestiva de otras patologías.. Palabras clave: Cefaleas; Pérdida aguda de la agudeza visual; Neuritis óptica. |
Abstract
|
Pediatric Multiple Sclerosis (MS) is defined as the onset of the disease before age 18. It is considered a rare disease at this age that can lead to both physical and cognitive deficits. Its prevalence is: 1.35-2.35 / 100,000 children. 5% in <18 years; 3% in <16 years; 1% in <10 years. It predominates in the female sex in a ratio of 2/8. In pediatrics, there are two clinical forms of presentation: a) Encephalopathy (16-20%), in children under 11 years; B) Isolated clinical syndrome: optic neuritis, transverse myelitis, cortical syndrome. Since adolescence is a time of life in which it is frequent the debut of diseases with an etiopathogenic base of immunological type, we present this clinical case, in which a clinic of acute onset and suggestive of other pathologies stands out. Key words: Headache; Acute loss of visual acuity; Neuritis |
Motivo de consulta
Adolescente de 16 años 2 meses, de sexo femenino, que consulta por disminución importante de la agudeza visual en el último mes.
Antecedentes personales: Menarquia: 13a 8m. Amigdalitis recurrentes. Bronquitis aisladas hasta los 4-5 años. Adenoidectomía a los 4 años. Astigmatismo y miopía desde los 6 años. Controles anuales sin aumento significativo de la graduación. Cefaleas migrañosas frontotemporales derechas desde los 8 años que se intensifican a los 14 años y cambian a la localización frontotemporal izquierda, controladas parcialmente con tratamiento con Propanolol preventivo y Sumatriptan nasal. 14a 11m: Astenia marcada, insomnio de conciliación y síntomas sugestivos de un trastorno depresivo, en seguimiento psiquiátrico y psicológico y en tratamiento con Fluoxetina y Diazepam. 15a 9m: episodios infecciosos secuenciales: infección vírica con fiebre y cefalea de 10 días de evolución luego una faringitis con fiebre asociada y posteriormente una GEA prolongada. 15a 11m: gastritis aguda con hematemesis, ingresada 48hs. Posteriormente nuevo episodio de infección vírica con fiebre alta y cefalea de 7 días de evolución. Analítica con pruebas reumáticas, serología víricas (VEB y CMV), Ig y subclases de IgG normales.
Antecedentes familiares: Sin interés.
Exploración física: BEG. Eutrófica. Hemodinámicamente estable. Glasgow 15.PICNR.Sin signos de focalidad neurológica. Tono y fuerza muscular conservados.ROT presentes y simétricos. Sensibilidad conservada. Fondo de ojo: no se observa edema de papila. Resto de la exploración por aparatos normal. Tañer 5.
Orientación diagnóstica
Adolescente. Disminución aguda de la agudeza visual. Antecedente de cefaleas, parcialmente controladas con tratamiento preventivo que han cambiado la localización. Todo ello sugiere: ¿Masa ocupante? ¿Patología oftalmológica aguda?
Exámenes complementarios
— Valoración oftalmológica se observa Mieloneuritis óptica izquierda.
— RM: Lesiones puntiformes en SB periventricular frontoparietal de predominio izquierdo. Alteración de la señal del nervio óptico. Médula espinal: pequeña lesión de 6 mm en cordones posteriores a la altura de odontoides.
— LCR Aumento de IgG oligoclonal.
Evolución
11 meses posteriores: Neuritis óptica derecha. 4 meses posteriores: brote medular con urgencia miccional. Nueva RM: 18 lesiones nuevas= 12 periventriculares, 4 cuerpo callos, 1 infratentorial, 1 medular.
TRATAMIENTO: Fingolimod + Ditropan.
Comentario
La esclerosis múltiple es una enfermedad rara, que produce déficits físicos y cognitivos
La Esclerosis Múltiple (EM) Pediátrica se define como el inicio de la enfermedad antes de los 18 años. Se considera una enfermedad rara a esta edad que puede conducir a déficits tanto físicos como cognitivos. Su diagnóstico en la edad pediátrica se ve dificultado por su baja incidencia y por las diferentes formas clínicas de presentación. Dentro de los grupos que estudian los avances en el estudio y tratamiento de la enfermedad destaca el International Pediatric Multiple Sclerosis Study Group.
Epidemiología: Prevalencia:1,35-2,35 / 100.000 niños. 5% en <18 años; 3% en < 16 años; 1% en < 10 años. Sexo: fem./masc.= 2/8. Raza: diferentes etnias y procedencias (Caribe, Asia, África, Europa central y del este). Edad: influenciada por el lugar de residencia durante la infancia. Estudios migratorios sugieren que los individuos menores de 14 años que migran adquieren el riesgo de EM del lugar donde residen.
La causa es una disregulación del sistema inmune periférico
Patogenia: La causa es una disregulación del sistema inmune periférico que conduce a una lesión del SNC y que requiere la combinación de factores de riesgo genético y ambiental que actúan como detonantes. Genética: el riesgo de desarrollar EM en familiares de primer grado es del 5%; en gemelos monocigóticos del 25% y en dicigóticos del 5%. Interactúan genes relacionados con factores inmunológicos neuroprotectores y con la mielina. Hay 110 variantes genéticas; el factor de mayor riesgo genético para el inicio precoz de la enfermedad es la presencia de al menos una copia del HLA-DRB1* 15: 01 o 15:03 en africanos ambos son correceptores para que VEB entre en el LB. Otros son el DQA1*0102 y DQB1*0602.Factores ambientales: VEB (el Ag nuclear tiene una estructura similar a la de la proteína básica de la mielina).El 86% de niños con EM tienen marcadores serológicos de infección pasada por VEB. Niveles bajos de vitamina D: es uno de los factores de riesgo más importantes y determinantes de la severidad en niños y adultos; principalmente en los HLA-DRB1*15. Por cada 10 ng/ml de aumento de los niveles séricos de 25-OH- vitamina D disminuyen en un 34% los botes de la enfermedad. Inadecuada exposición a la luz solar. Exposición al humo del cigarrillo.
Clínica: Episodios recurrentes de desmielinización en el SNC separados en espacio y tiempo. Formas de presentación: 1-Síndrome clínico aislado: Neuritis óptica, Mielitis trasversa, Síndrome cortical 2-Encefalopatía:cefalea, vómitos, convulsiones, alteración de la consciencia (16-20%). La mayoría < 11 años.
Curso clínico: Recaída-Remisión: forma de inicio en el 97-99% de los niños, con recuperación parcial o completa de sus funciones. EM Primaria Progresiva: pérdida progresiva de funciones, sin brotes. Fatiga(muy frecuente). Depresión (20-50%). Déficits cognitivos:procesamiento de la información, lenguaje, integración visomotora, memoria visual y verbal. Están relacionados con la duración y severidad de la enfermedad.
Diagnóstico
En la RM se observan múltiples lesiones en la sustancia blanca y aumento de áreas inflamatorias y compromiso de la barrera hematoencefálica
RM: Secuencias T2: múltiples lesiones, bien delimitadas, en la sustancia blanca periventricular, yuxtacortical, infratentorial y médula espinal.Secuencias T1: «agujeros negros» o lesiones hipointensas que representan pérdida completa de tejido secundarias a un proceso inflamatorio previo. Secuencias T1 con contraste con gadolinium: aumento de las áreas inflamatorias y compromiso de la barrera hematoencefálica.
LCR (variable en los niños): Bandas oligoclonales de IgG. Aumento de IgG.
Potenciales evocados visuales y somatosensoriales(variables en pediatría) (Criterios diagnósticos de Mc Donald 2010). Tienen alta sensibilidad y especificidad para el diagnóstico de EM pediátrica en > 12 años. El objetivo es la demostración objetiva de la diseminación de las lesiones en tiempo y espacio. Se basa tanto en hallazgos clínicos aislados como la combinación de hallazgos clínicos y en la RM.
Diseminación en espacio: en la RM, presencia de1 más T2 lesiones en al menos 2 de 4 localizaciones típicas de la EM en el SNC (periventricular, yuxtacortical, infratentorial o médula espinal) o la afectación de una localización diferente del SNC en el curso de un nuevo brote.
Diseminación en tiempo: demostración simultánea en la RM, en cualquier momento de la evolución, de lesiones asintomáticas, realzadas o no con gadolinium o aparición de nuevas lesiones en T2 y/o realzadas con gadolinium en el seguimiento con RM o en el curso de un nuevo brote.
Criterios diagnósticos de EM en pediatría
Debe cumplirse cualquiera de los siguientes criterios:
•Dos o más manifestaciones clínicas de afectación del SNC (no encefalíticas) de posible causa inflamatoria, separadas por >30 días y con afectación de más de un área del SNC.
•Un episodio típico de EM, no encefalítico, asociado a imágenes en la RM que cumplen los criterios de Mc Donald 2010 para diseminación en espacio y que, en el seguimiento con RM, presenta al menos una lesión nueva para cumplir el criterio de diseminación en tiempo.
• Un episodio de encefalomielitis aguda diseminada (ADEM) seguido en un mínimo de 3 meses por una manifestación clínica no encefalítica y asociado a nuevas lesiones en la RM que cumplen los criterios de McDonald 2010 de diseminación en espacio.
• Un primer y único episodio que no reúne los criterios de ADEM y que se asocia a imágenes en la RM que cumplen los criterios de McDonald 2010 de diseminación en espacio y en tiempo (sólo aplicable en > 12 años).
Diagnóstico Diferencial (Tabla I)
Tratamiento
Aunque las siguientes terapias aún no han sido formalmente aprobadas para su uso en pediatría, cada vez se utilizan más, formando parte de ensayos clínicos. Es importante que tanto el paciente como su familia participen en la elección del tipo de tratamiento a seguir para garantizar así una mayor adherencia al mismo.
Tratamiento de primera línea: acetato de glatiramer, Interferón beta
Tratamientos de primera línea. Incluyen tratamientos parenterales IM: Acetato de glatiramer, Interferón beta. Ambos reducen en un 30% las recaídas clínicas. Si no hay respuesta o los efectos secundarios son difíciles de controlar se puede cambiar a otras drogas de primera línea o pasar a las de segunda línea.
Tratamiento de segunda línea: Natalizumab
Tratamientos de segunda línea Su eficacia es mayor pero también lo es el riesgo potencial de presentar importantes efectos secundarios. El más estudiado en pediatría es el Natalizumab. Hay en estudio nuevas terapias orales que podrían ser una alternativa más segura para su uso en pediatría. En las exacerbaciones agudas se utilizan los corticoides. Metilprednisolona ev, 30 mg/Kg/d (dosis máxima 1000 mg/d) durante 3-5 días. Si no hay respuesta: Gamaglobulina ev Plasma. Tratamiento sintomático Tratamiento psicológico.
Tablas y figuras
Tabla 1. Diagnóstico diferencial
|
Enf. Inflamatoria |
ADEM/MDEM, LES, S. Anticuerpos antifosfolípidos E. Sjögren, E.Behçet |
|
Tumores del SNC |
Linfoma, Glioma de alto grado |
|
Leucodistrofias |
L.Metacromática, Adrenoleucodistrofia ligada al X, E. de Alexander |
|
Infecciones del SNC |
Inf.agudas bacterianas o virales, E. de Lyme, Virus West Nile, Sífilis, HIV |
|
Deficiencias de vitaminas |
B12, Folatos |
|
Enf. Granulomatosa |
Neurosarcoidosis, Granulomatosis de Wegener |
|
Enf. Mitocondriales |
Neuropatía óptica hereditaria de Leber |
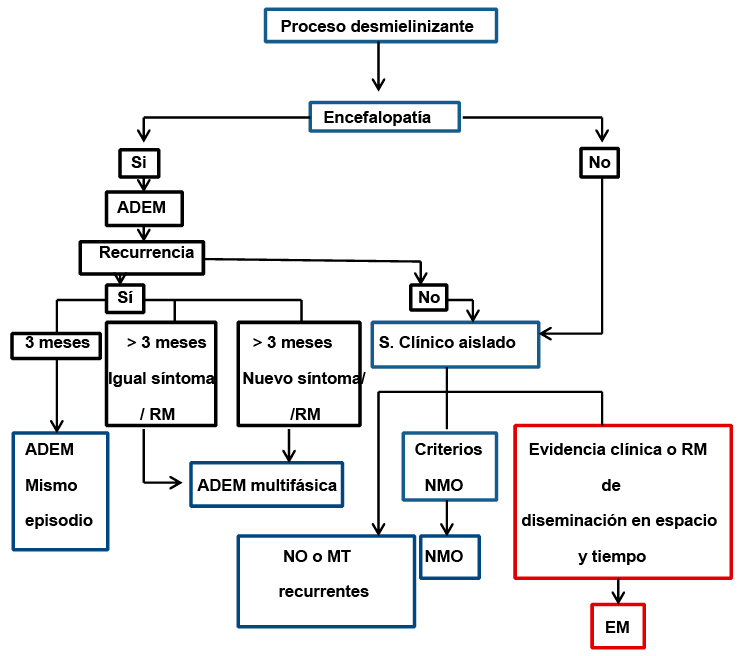
Figura 1. Diagnóstico de un cuadro clínico de desmielinización
Bibliografía
1. Pathogenesis, clinical features, and diagnosis of pediatric multiple sclerosis. Timothy E Lotze,MD Section Editors: Marc C Patterson,MD,FRACP. Francisco Gonzalez-Scarano,MD. Deputy Editor: John F Dashe, MD, PhD UpToDate, Set.21, 2015.
2. Esclerosis múltiple en pediatría. Dr. David Lyncet-Mejorado, Dr. Eduardo Barragán-Pérez. Bol Med Hosp Infant Mex Vo.63, enero-febrero 2006.
3. Pediatric Multiple Sclerosis in the Spotlight CME.Lauren Krupp, MD Medscape Education.Set.25, 2015.
4. Pediatric multiple sclerosis: update in diagnosis and management.A.Ghezzi.Eur Neurol.2014;72 Suppl 1:26-28.
5. Vitamin D status is associated with relapse rate in pediatric-onset multiple sclerosis. EM Mowry, LB Krupp, M Milazzo, D Chabas, JB Strober, AL Belman.Ann Neurol.2010; 67(5):618-624.
6. Diagnostic criteria for multiple sclerosis: 2010 revisions to the Mc Donald criteria.C Polman, S Reingold, B Banwell et al.Ann Neurol.2011; 69(2):292-302.
7. Elevated relapse rates in pediatric compared to adult MS persist for at least 6 years.LA Benson, BC Healy, MP Gorman et al.Mult Scler Relat Disord.2014;3(2):186-193.
8. Clinical and MRI activity as determinants of sample size for pediatric multiple sclerosis trials.LH Verhey, AL Signori, D Arnold et al.Neurology. 2013; 81(14):1215-1221.
9. Pediatric multiple sclerosis: what we know and where are we headed? WS MacAllister, C Christodoulou, M Milazzo et al.Child Neuropsychol.2013; 19(1):1-22.
10. Treatment of pediatric multiple sclerosis.S Narula,SE Hopkins,B Barnwell.Curr Treat Options Neurol.2015; 17(3): 336.