Cefaleas primarias en la adolescencia
Cefaleas primarias en la adolescencia
U.A. Barrios Machain(1), A.M. Nieto Serrano(2), M.I. Hidalgo Vicario(3).
(1)Residente de Pediatría. Hospital Universitario La Paz. (2)Pediatra. Médica Adjunta. Unidad de Adolescente. Hospital Universitario La Paz. (3)Pediatra. Doctora en Medicina. Acreditada en Medicina de la Adolescencia. Centro de Salud “Barrio del Pilar”.
Fecha de recepción: 24 de enero 2018
Fecha de publicación: 28 de febrero 2018
Adolescere 2018; VI (1): 51.e1-51.e11
Resumen
|
La cefalea en la adolescencia es uno de los síntomas o trastornos más frecuentes, la mayoría son de origen primario y se pueden orientar con una correcta anamnesis y examen físico sin requerir una derivación a un servicio especializado ni pruebas de imagen. Debido a que es uno de los motivos más frecuentes de consulta, es imperante su conocimiento, permitiendo reducir así tanto pruebas complementarias innecesarias como el gasto sanitario. A continuación se describirá los principales tipos de cefalea primaria y su manejo. Palabras clave: cefaleas primarias, tensional, migraña, trigémino-autonómica, tratamiento. |
Abstract
|
Headache in adolescence is one of the most frequent symptoms or disorders, where most are of primary origin and can be guided with a correct history taking and physical examination without requiring a referral to a specialized service or imaging tests. Because it is one of the most frequent reasons for consultation, the physician must be knowledgeable about it, thus reducing both unnecessary complementary tests and health expenditure. The main types of primary headache and their management will be described here. Key words: primary headache, tensional, migraine, autonomic-trigeminal, treatment. |
Introducción
Las cefaleas son con gran diferencia las enfermedades neurológicas más frecuentes en la edad infantil y la adolescencia con una frecuencia aproximada del 88%(1).
Pese a la alta frecuencia de cefaleas en la edad pediátrica, abarrotando las consultas tanto en los centros de Atención Primaria como en los servicios de Urgencias Pediátricos, conocemos poco y tememos mucho, lo que conlleva a una alta tasa de derivaciones a unidades de Neurología pediátrica y a la realización de pruebas de neuroimagen sin indicación.
En los pacientes con un diagnostico establecido de cefalea primaria con ausencia de signos de alarma y de alteraciones neurológicas, la posibilidad de que ésta se deba a un tumor del SNC, es muy baja y cercana incluso al 1%. Hay estudios que indican que la realización de pruebas de neuroimagen de forma innecesaria en pacientes con cefalea, supone un alto gasto de salud pública y no modifica el manejo en la mayoría de las ocasiones(2).
En ausencia de signos de alarma y de alteraciones neurológicas, la posibilidad de que la cefalea se deba a un tumor del SNC, es muy baja y cercana incluso al 1%
Clasificación
Las cefaleas se dividen en 2 tipos:
— Primarias: sin causa identificable (idiopáticas).
— Secundarias: atribuible a una causa.
La clasificación internacional y más reciente de las cefaleas es la del International Headache Society 3, versión beta (ICH-3b), publicada en el año 2013.
Aproximación al paciente con cefalea
El abordaje de un paciente con cefalea empezará con una exhaustiva y prolija historia clínica, ya que se ha visto que en un muy alto porcentaje de los casos se consigue un correcto diagnóstico. El cuestionario propuesto por Rothner(1) puede ser de gran utilidad para, en la práctica clínica, hacer una entrevista dirigida. Entre los datos que tienen máxima importancia cabe destacar los siguientes: ¿Cuándo empezó la cefalea?, ¿cómo empezó?, ¿cuál es el patrón temporal?, frecuencia, duración, ¿en qué circunstancia apareció?, ¿dónde se localiza el dolor?, ¿cómo es el dolor?, ¿hay algún síntoma asociado?, ¿qué mejora/empeora la cefalea?, ¿existen síntomas entre los episodios de cefalea?, ¿toma la medicación?, ¿existen antecedentes de cefalea?, etc.
En cuanto al examen físico debe ser lo más exhaustivo posible. Dentro del examen físico se debería incluir:
— Anotación de los signos vitales (incluyendo tensión arterial).
— Exploración cervical (buscar signos de trauma, irritación meníngea, zonas de tensión).
— Si existe dolor a la palpación de los senos paranasales y la maniobra de Mueller (tapar las narinas, hacer contar hasta 3 y pedir que tosa; el dolor en la maniobra sugiere sinusitis aguda, no debe realizarse si hay evidencia de aumento de la presión intercraneal (PIC) o durante el episodio agudo de cefalea).
— Examen de la cavidad oral y valorar si hay disfunción de la articulación temporomandibular.
— Examinar la piel en busca de estigmas neurocutáneos.
— Examen neurológico en el que se debe evaluar: estado mental, diálogo, visión, fondo de ojo, pares craneales, evaluación motora y de la fuerza, sensibilidad, coordinación, marcha y reflejos; cualquier asimetría o hallazgo focal debe ser muy tenido en cuenta.
Por último, es muy útil en la práctica clínica el uso de calendarios/diarios de cefalea que pueden ayudar sobre todo a definir la fecha, frecuencia, tiempo de evolución, desencadenantes, modificadores y la posible interacción de estrés psicosocial en las cefaleas(1,3-5). No es infrecuente que un paciente tenga diferentes tipos de cefaleas, de ahí la importancia de constatarlas en un diario(5). La mayoría de las cefaleas agudas que se presentan en el servicio de urgencias son parainfecciosas y debidas a un cuadro infeccioso de vías aéreas, por tanto siempre debe constatarse esto(6).
No es infrecuente que un paciente tenga diferentes tipos de cefaleas, de ahí la importancia de constatarlas en
un diario
Lo más importante en la evaluación del paciente con cefalea es buscar y descartar datos sugerentes de patología secundaria, ver Tabla I.
La neuroimagen está indicada en adolescentes con cefalea aguda y al menos una de las siguientes características(1):
— Examen neurológico alterado.
— Presentación atípica de cefalea, incluyendo vértigo, vómitos incoercibles o cefalea que despierta por la noche.
— Cefalea reciente de menos de 6 meses de evolución.
— Niño de menos de 6 años de edad.
— Si no existen antecedentes familiares de migraña o de cefaleas primarias.
— Cefalea occipital.
— Cambios en el tipo de cefalea.
— Inicio subagudo y con severidad progresiva de la cefalea.
— Nueva cefalea en un niño inmunodeprimido.
— Primera y/o empeoramiento de la cefalea.
— Signos y síntomas sistémicos.
— Cefalea asociada a confusión, alteración del estado mental o focalidad neurológica.
Cefaleas primarias
Existen 3 categorías de cefaleas primarias: cefalea tensional, migraña y cefalea autonómica
trigeminal. La cefalea tensional y la migraña son las más frecuentes en adolescentes.
Cefalea tensional
Es la cefalea más frecuente, la mayor parte de la población la sufrirá al menos una vez en su vida(1). Llama más la atención su duración que su intensidad(5), ya que esta es leve-moderada y por lo tanto pocos pacientes consultarán por ella, de forma urgente, aunque si lo harán por su cronicidad. Suele relacionarse a un factor estresante como el estrés emocional, sueño alterado/interrumpido, depresión, saltarse comidas, etc.(1,4).
Existe una influencia genética(5). Es más frecuente en jóvenes del sexo femenino(5) y tiende a disminuir su frecuencia con la edad(1).
Al examen físico en la cefalea tensional lo único que puede encontrarse es tensión de los músculos pericraneales, así como de los músculos de la nuca y el trapecio
Al examen físico lo único que puede encontrarse es tensión de los músculos pericraneales, así como de los músculos de la nuca y el trapecio(5).
Las cefaleas tensionales se clasifican a su vez según la ICHD-3b en episódicas (que se subclasifican en frecuentes o infrecuentes) o crónicas(7). A continuación se citan los criterios diagnósticos de cada una de ellas.
Cefalea tensional episódica
A. Al menos 10 episodios de cefalea + criterios B, C y D.
Cefalea tensional episódica infrecuente: cefalea menos de 1 día por mes (menos de 12 días por año).
Cefalea tensional episódica frecuente: cefalea de 1-14 días por mes durante más de 3 meses (≥12 días y ˂180 días por año).
B. La cefalea dura de 30 min – 7 días.
C. Al menos 2 de los siguientes:
Bilateral.
Opresiva o tensional (no pulsátil).
Intensidad leve o moderada.
No se agrava por la actividad física rutinaria como caminar o subir escaleras.
D. Ambas de las siguientes:
No náuseas ni vómitos.
No más de un episodio de fotofobia o sonofobia.
E. No es posible atribuirlo a otro diagnóstico de la ICHD-3b.
(Adaptada de: The International Classification of Headache Disorders, 3rd edition (beta versión). Cephalalgia 2013)
Cefalea tensional crónica
A. 15 o más episodios de cefalea al mes durante al menos 3 meses (˃180 días al año) + criterios B, C y D.
B. La cefalea dura de horas – días o no remite.
C. Al menos 2 de los siguientes:
Bilateral.
Opresiva o tensional (no pulsátil).
Intensidad leve o moderada.
No se agrava por la actividad física rutinaria como caminar o subir escaleras.
D. Ambas de las siguientes:
Solo un episodio de los siguientes: fotofobia, sonofobia o náuseas leves.
No náuseas moderadas o intensas ni vómitos.
E. No es posible atribuirlo a otro diagnóstico de la ICHD-3b.
(Adaptada de: The International Classification of Headache Disorders, 3rd edition (beta versión). Cephalalgia 2013)
Migraña
Es relativamente infrecuente en la edad infantil, pero aumenta su frecuencia conforme aumenta la edad. La prevalencia es similar entre ambos géneros durante la edad infantil, pero conforme se acerca la adolescencia, aumenta la prevalencia en mujeres. Éste patrón se ha asociado al cambio hormonal que sucede durante la pubertad, sobre todo al efecto estrogénico en la musculatura vascular lisa intracraneal(1). El subtipo de migraña más frecuente es la migraña sin aura(1, 3- 5).
La migraña es relativamente infrecuente en la edad infantil, pero aumenta su frecuencia conforme aumenta la edad. La más frecuente
es sin aura
Se sabe que existe una susceptibilidad genética a la migraña (70%), con una alta tasa de antecedentes familiares de migraña en los pacientes afectados(6).
La principal diferencia entre la migraña en edad pediátrica y la del adulto es el tiempo de duración, en el adulto dura como mínimo 4 horas, en cambio la migraña del niño es más corta(6), tomándose como criterio una duración mínima de 2 horas(7).
La principal diferencia entre la migraña del niño y adulto es el tiempo de duración, en el adulto dura como mínimo 4 horas, en los niños son más cortas
Dependiendo de la existencia de aura, se clasifica en migraña con aura (migraña clásica) o sin aura. El aura se define como ataques recurrentes, unilaterales, de minutos de duración y completamente reversibles en las que existe una alteración visual, sensorial u otra sintomatología del sistema nervioso central, se establece en general de manera gradual y frecuentemente es seguida por la cefalea. El aura más frecuente es el visual(7). Los síntomas del tronco encefálico (disartria, vértigo, acúfenos, etc; excepto debilidad motora) se clasifican por la ICHD-3b como migraña con aura del tronco(7). Si el aura incluye debilidad motora se debe clasificar como migraña hemipléjica(5,7), la cual tiene una variante familiar (enfermedad migrañosa monogénica(1)) que se clasifica en otro grupo dada su base genética.
No es infrecuente la presencia de aura que no se acompañe posteriormente de cefalea, en caso de que estos episodios sean frecuentes, deben barajarse otros posibles diagnósticos como el accidente isquémico transitorio o las crisis convulsivas(8).
Algunos pacientes describen síntomas premonitorios antes del inicio de la cefalea, éstos pueden comenzar horas o un día o dos antes del resto de los síntomas de una crisis migrañosa (con o sin aura), suele describirse fatiga, dificultad para concentrarse, rigidez cervical, sensibilidad a la luz o al ruido, náuseas, visión borrosa, bostezos o palidez. Debe evitarse llamar a los síntomas premonitorios “pródromos” o “síntomas previos” para no confundirlos con el aura(7).
Existen ciertos factores que tienden a desencadenar una crisis migrañosa, los más comunes son comidas o aditivos como: chocolate, quesos, levaduras, frijoles. Otros desencadenantes
asociados son: la menstruación, el hambre, exposición a estrógenos (anticoncepción oral), sueño, estrés, calor y el esfuerzo excesivo(4).
Las principales diferencias entre cefalea tensional y migraña se encuentran en la Tabla II.
Los criterios diagnósticos de las migrañas son los siguientes:
Criterios diagnósticos de migraña sin aura
A. Al menos cinco crisis que cumplen los criterios B, C y D.
B. Duración entre 4 y 72 horas (no tratados o tratados sin éxito).*
C. La cefalea presenta al menos dos de las siguientes cuatro características:
1. Localización unilateral.**
2. Carácter pulsátil.
3. Intensidad moderada o severa.
4. Empeora con la actividad física habitual
D. Al menos uno de los siguientes durante la cefalea:
1. Náuseas y/o vómitos.
2. Fotofobia y fonofobia.
E. Sin mejor explicación por otro diagnóstico de la ICHD-3b.
* En adolescentes, las crisis pueden durar entre 2 y 72 horas. Si el paciente concilia el sueño durante la crisis y se despierta sin dolor, la duración será hasta el momento del despertar.
** La localización bilateral de la cefalea migrañosa es frecuente en adolescentes; la unilateral se ve en la adolescencia tardía o al inicio de la adultez.
(Adaptada de: ICHD, 3rd edition (beta versión). Cephalalgia 2013)
Criterios diagnósticos de migraña con aura
A. Al menos dos crisis que cumplen los criterios B y C.
B. Uno o más de los siguientes síntomas de aura totalmente reversibles:
1. Visuales.
2. Sensitivos.
3. Del habla o del lenguaje.
4. Motores.
5. Troncoencefálicos.
6. Retinianos.
C. Al menos dos de las siguientes cuatro características:
1. Progresión gradual de al menos uno de los síntomas de aura durante un período ≥ 5 min y/o dos o más síntomas que se presentan consecutivamente.
2. Cada síntoma de aura tiene una duración entre 5 y 60 minutos.
3. Al menos uno de los síntomas de aura es unilateral
4. El aura se acompaña, o se sigue antes de 60 min, de cefalea.
D. Sin mejor explicación por otro diagnóstico de la ICHD-3b y se ha descartado un accidente isquémico transitorio.
(Adaptada de: ICDH, 3rd edition (beta versión). Cephalalgia 2013)
Debe tenerse especial cuidado en aquellas crisis migrañosas que se prolongan más de 72 horas (podrían tener remisiones de hasta 12 horas por uso de fármacos o el sueño) pues se clasifican como estatus migrañoso el cual tiene un manejo diferente(8). Cuando la cefalea ocurre 15 o más días al mes por al menos 3 meses se considera siempre una migraña crónica y cuando durante este período la cefalea tenga características de migraña al menos 8 días al mes(7).
Cuando la cefalea ocurre 15 o más días al mes durante al menos 3 meses se considera una migraña crónica
Por último, existe una entidad llamada migraña relacionada con la menstruación, suele ser predecible y darse en ±1-2 días de la regla(7).
Cefaleas trigémino-autonómicas
Suelen aparecer durante la adolescencia o la adultez aunque son infrecuentes.
— Cefalea en racimos: consiste en ataques de dolor severo unilaterales en la región orbitaria, supraorbitaria, temporal o combinación de las anteriores de breve duración asociado a manifestaciones autonómicas faciales, más frecuente en los hombres. Existen periodos de ataques frecuentes seguidos de otros completamente asintomáticos, pocos son los pacientes que no tienen este periodo asintomático.
Cefalea en racimos: consiste en ataques de dolor severo unilaterales en la región orbitaria, supraorbitaria, temporal o combinación de las anteriores de breve duración asociado a manifestaciones autonómicas faciales
— Hemicránea paroxística: ataque de dolor severo unilateral en región orbitaria, supraorbitaria, temporal o combinación de las anteriores de corta duración que se presenta muchas veces durante el día, se acompaña de sintomatología autonómica homolateral y remiten con indometacina. Más frecuente en mujeres.
Criterios de cefalea en racimos
A. Al menos cinco ataques que cumplen los criterios B, C y D.
B. Dolor unilateral de intensidad severa o muy severa en región orbitaria, supraorbitaria o temporal, con una duración de 15 a 180 minutos sin tratamiento.
C. Cualquiera o los dos siguientes:
- Al menos uno de los siguientes síntomas o signos, homolaterales a la cefalea:
a) Inyección conjuntival y/o lagrimeo.
b) Congestión nasal y/o rinorrea.
c) Edema palpebral.
d) Sudoración frontal y facial.
e) Rubefacción frontal y facial.
f) Sensación de taponamiento en los oídos.
g) Miosis y/o ptosis.
- Inquietud o agitación.
D. La frecuencia de los ataques varía entre una vez cada dos días y ocho al día durante más de la mitad del tiempo que el trastorno está activo.
E. Sin mejor explicación por otro diagnóstico de la ICHD-3b.
(Adaptada de: ICHD, 3rd edition (beta versión). Cephalalgia 2013)
Criterios de hemicránea paroxística
La hemicránea paroxística es más frecuente en las mujeres y remite con indometazina
A. Al menos 20 ataques que cumplen los criterios B, C, D y E.
B. Dolor severo unilateral en región orbitaria, supraorbitaria o temporal, con una duración de 2 a 30 minutos.
C. Al menos uno de los siguientes síntomas o signos, homolaterales al dolor:
1. Inyección conjuntival o lagrimeo.
2. Congestión nasal o rinorrea.
3. Edema palpebral.
4. Sudoración frontal y facial.
5. Rubefacción frontal y facial.
6. Sensación de taponamiento en los oídos.
7. Miosis y/o ptosis.
D. Los ataques tienen una frecuencia mayor de cinco por día durante más de la mitad del tiempo.
E. Los episodios responden completamente a dosis terapéuticas de indometacina.
F. Sin mejor explicación por otro diagnóstico de la ICHD-3b.
(Adaptada de: ICHD, 3rd edition (beta versión). Cephalalgia 2013)
Existe la entidad llamada hemicránea persistente que tiene características de hemicránea paroxística pero sin remisiones al menos durante 1 año, o con una remisión menor a 1 mes(7).
Tratamiento de las cefaleas primarias
Medidas generales
En la cefalea tensional son muy importantes los cambios en el estilo de vida, técnicas conductuales y de relajación
Para casos de cefalea tensional son muy importantes los cambios en el estilo de vida como la hidratación adecuada (3-4 vasos de agua al día), realizar 4-5 comidas al día, ejercicio físico regular y llevar un ritmo adecuado de sueño, es importante evitar los factores estresantes ya que éste tipo de cefalea se ve desencadenada frecuentemente por esos factores(5), la realización de técnicas conductuales y de relajación ayudan bastante(8).
En el caso de las migrañas es importante aparte de lo citado previamente, identificar si existe o no un factor precipitante y controlarlo en caso de que se asocie a los ataques(5).
Tratamiento de rescate
Los analgésicos simples como el paracetamol o el ibuprofeno son las primeras líneas del tratamiento sintomático de las cefaleas, sobretodo en la cefalea tensional episódica. No se recomienda el uso de terapia basada en opioides por ser menos efectiva y más propensa al aumento progresivo de las dosis y dependencia, aparte de los efectos secundarios posibles(10).
En las migrañas con y sin aura, en el tratamiento abortivo se usan los triptanes y deben probarse al menos 3 triptanes diferentes antes de poder afirmar que no funcionan para
la migraña
Para las migrañas con y sin aura en el tratamiento abortivo se usan los triptanes que son agonistas de receptores serotoninérgicos 1B/1D/1F con un efecto antimigrañoso espectacular por su efecto vasoconstrictor cerebral. Los triptanes no han demostrado disminuir la severidad de otros tipos de cefaleas, por tanto una respuesta a estos compuestos se podría considerar como diagnóstica de migraña(1). Pueden repetirse después de 2 horas si es necesario pero no más de 2 dosis en 24 horas y no más de 2 días a la semana, si no funciona durante una crisis migrañosa no debe ser excluido como parte del tratamiento, debe probarse al menos en 3 episodios diferentes y al menos 3 triptanes diferentes antes de poder afirmar que no funcionan para la migraña(10). Es muy útil la combinación de un triptan + paracetamol y/o ibuprofeno. Esta combinación es más efectiva y costo-efectiva que cada medicación por separado(10). En caso de vómitos o intolerancia por vía oral se usa la vía intravenosa asociada a un antiemético.
En cuanto a las cefaleas en racimos es particularmente útil el uso de oxígeno al 100% a alto flujo (12 litros/min) a través de una máscara cerrada con reservorio, los triptanes vía oral o subcutánea también podrían ayudar(10-11). En la hemicránea paroxística es muy efectiva la indometacina (debe ser combinada con omeprazol o ranitidina), es tan típica la respuesta al tratamiento que constituye uno de los criterios diagnósticos de ésta(8,10).
Se debe advertir a los pacientes sobre el exceso en la toma de medicación, ya que existe la cefalea crónica por sobreuso de medicación que se debe sospechar si el paciente ha consumido triptanes, ergotamina, opioides o combinación de analgésicos durante 10 o más días al mes, o paracetamol/AINES más de 15 días al mes. El tratamiento de ésta es la suspensión brusca de la medicación(10).
Para las migrañas relacionadas con la menstruación, si los analgésicos simples no funcionan se podría probar con los triptanes, 2 e inclusive 3 veces al día en los días en los que se espere que tenga la migraña incluso en días consecutivos, se ha tenido buena experiencia con el zolmitriptan(10).
Profilaxis
En general una cefalea tensional crónica no suele recibir tratamiento profiláctico medicamentoso, en caso de precisarlo sería por asociarse a una migraña, si no es así deberían considerarse otros diagnósticos; algunas publicaciones recomiendan como primera línea de profilaxis de ésta cefalea la acupuntura (10 sesiones en 5-8 semanas), aunque tradicionalmente se ha utilizado con éxito la amitriptilina y también se observan buenos resultados con el topiramato(5, 10, 11).
En el tratamiento profiláctico, los dos fármacos que cuentan con mayor evidencia científica son el topiramato y la flunarizina
En el caso de las migrañas se debe ofrecer una medicación profiláctica diaria sobre todo en aquellos pacientes con más de 3-4 episodios al mes dependiendo de la severidad y repercusión que tenga en su vida diaria. Todos los fármacos deberían iniciarse a dosis bajas e ir aumentando según la respuesta(10), en general debe probarse el fármaco hasta llegar a la dosis objetivo durante 4-6 semanas, si no funciona pasado este tiempo debería cambiarse a otra medicación, se debe evitar combinar 2 fármacos profilácticos(8). La elección del fármaco dependerá de las preferencias y comorbilidades del paciente(10). No se sabe si la utilización de estos fármacos afecta el curso natural de la enfermedad, deberá mantenerse como mínimo 6 meses y luego intentar su retirada(16). Los dos fármacos que cuentan con mayor evidencia científica son el topiramato(10,11) y la flunarizina(5), existen otros con menor evidencia como el propanolol, valproato, amitriptilina, riboflavina, magnesio y coenzima Q10(1,8) . También hay autores que recomiendan la acupuntura como tratamiento profiláctico en las migrañas pero como tratamiento de segunda línea(11).
Tablas y figuras
Tabla I. Datos sugerentes de cefalea secundaria(4)
|
En la historia clínica |
|
Calidad: cefalea de inicio brusco o “la peor cefalea de mi vida”, reciente empeoramiento de la severidad o frecuencia, cambios en la cualidad de la cefalea, Nuevos síntomas consistentes con cefalea en racimos |
|
Localización: unilateral sin alteración de los lados, occipital crónica o recurrente |
|
Tiempo: despierta por la noche, son matinales, o causan vómitos al despertar, patrón crónico progresivo |
|
Posicional o variación con las actividades: empeora con el decúbito, aparece con la tos o con Valsalva |
|
Historia neurológica asociada: sensorio alterado durante la cefalea, déficit sensorial o cambios en la visión, marcha o coordinación, déficit focal neurológico, síncope o crisis convulsiva, cambios en el estado mental (ej. confusión o desorientación), regresión de hitos motores finos o gruesos, disminución en el rendimiento escolar, cambios en el comportamiento o personalidad |
|
Asocia: vómitos sin náuseas, poliuria o polidipsia, edad preescolar o menor, historia de trauma craneal, comorbilidades médicas, sin antecedentes familiares de cefaleas primarias |
|
En el examen físico |
|
Hipertensión |
|
Signos meníngeos con o sin fiebre |
|
Evidencia de trauma craneal |
|
Sensibilidad en el hueso frontal |
|
Hallazgos oftalmológicos anormales: papiledema, anomalías en los movimientos oculares, desviación de la mirada, reflejo fotomotor alterado, defectos en el campo visual |
|
Hallazgos neurológicos anormales: alteración del estado mental, parálisis de pares craneales, ataxia, marcha alterada, coordinación alterada, reflejos osteotendinosos alterados, asimetría motora o sensorial, hemiparesia, regresión del desarrollo |
|
Pubertad precoz o retrasada |
|
Hallazgos en piel: manchas café con leche, máculas en hojas de fresno, púrpuras o petequias, hemangioma facial, rash malar |
Tabla II. Características diferenciales entre cefalea tensional y migraña(1, 4, 5, 9)
|
Migraña |
Cefalea tensional |
|
|
Horario |
Cualquiera |
Vespertino |
|
Intensidad |
Moderada-intensa |
Leve-moderada |
|
Localización |
Hemi u holocraneal |
Holocraneana |
|
Característica del dolor |
Pulsátil |
Opresivo |
|
Asociaciones |
Disminución de la actividad Síntomas gastrointestinales Fotofobia Sonofobia Osmofobia (miedo a oler) |
Situaciones estresantes Ansiedad Depresión Fotofobia/sonofobia (nunca ambas) |
|
Aura |
Posible |
No |
|
Empeora/mejora |
Actividad física/reposo |
Estrés/reposo |
Tabla III. Tratamiento de rescate para las cefaleas primarias
|
Fármaco |
Dosis |
Efectos adversos. Advertencias. Recomendaciones |
|
Paracetamol10 |
Oral: 20 mg/kg cada 4-6h; máx 75 mg/kg/día Rectal: inicio con 40 mg/kg y luego 20 mg/kg IV: 15 mg/kg cada 4-6h; máx 60 mg/kg/día |
Daño hepático y renal |
|
Ibuprofeno5, 10 |
Oral: 10-20 mg/kg/dosis; máx 50 mg/kg/día u |
Daño gástrico, sangrados, úlceras, reacciones alérgicas |
|
Sumatriptan5 |
Intranasal: 10 mg en ˂40kg; 20 mg en˃40kg Subcutáneo: 3-6 mg Malos resultados con formas orales |
Cardiotoxicidad, enrojecimiento, mareos, en la forma intranasal podría surgir molestias con respecto al sabor |
|
Zolmitriptan5 |
Intranasal: 5 mg |
|
|
Tratamiento profiláctico para las cefaleas primarias: migraña con y sin aura |
||
|
Topiramato10 |
Oral: inicio con 0,5 mg/kg y aumento progresivo a 10 mg/kg/día, máximo 200 mg/día |
Pérdida de peso, parestesias, fatiga, somnolencia, deterioro de la memoria. Riesgo de teratogenicidad |
|
Flunarizina5 |
Oral: inicio 2,5-5 mg/día (a la noche), aumento progresivo hasta 10 mg/día (dosis máxima |
Sedación, ganancia de peso, tremor, irregularidad menstrual. |
|
Propanolol10 |
Oral: 12-18 años: 30 mg 2 veces al día; incremento hasta 60 mg 2 veces al día |
Evitar en asma, problemas con el sueño. Evitar la retirada brusca |
|
Valproato10 |
Oral: 10 mg/kg/día aumento hasta 40 mg/kg/día; máximo 1,5 g 2 veces al día |
Ganancia de peso, tremor. Evitar en mayores de 12 años, riesgo de teratogenicidad. Irregularidad menstrual |
|
Amitriptilina5, 10 |
Oral: 12-18 años: 25-50 mg a la noche. |
Boca seca, sedación, visión borrosa, estreñimiento. Riesgo de cardiotoxicidad a dosis altas |
|
Riboflavina8 (vitamina B2) |
5 mg/kg/día en 1 o 2 tomas; máx 400 mg/día |
Sobre todo en pacientes con dietas con pocas frutas y verduras. Olor fuerte en la orina, molestias gastrointestinales |
|
Magnesio8 |
9 mg/kg/día en 2 tomas |
Diarreas |
|
CoQ108 |
1-3 mg/kg/día a la mañana |
Insomnio |
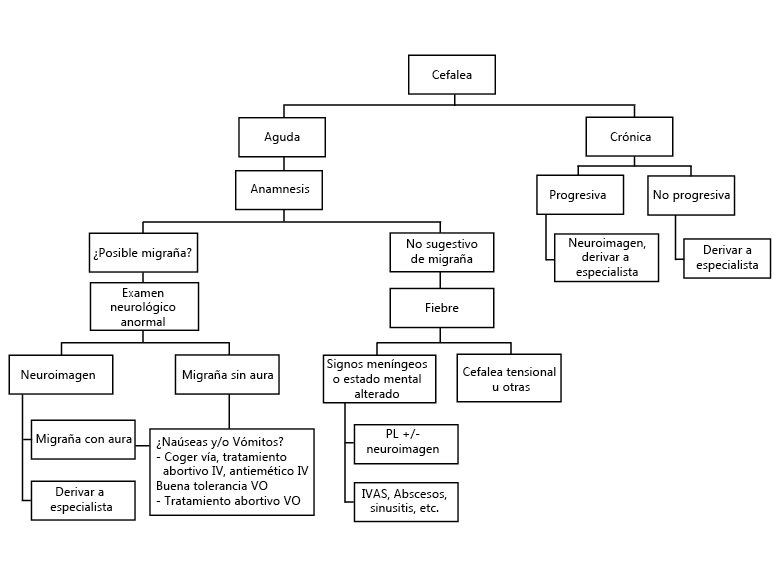
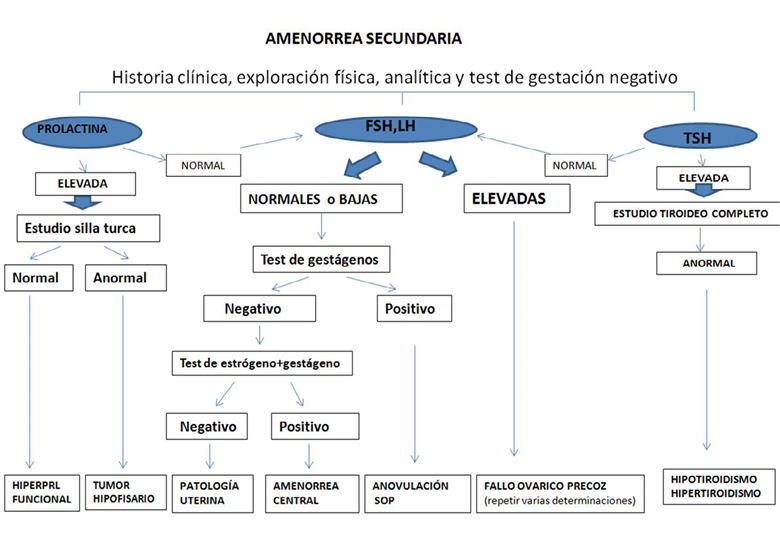
Figura 1. Algoritmo de actuación ante una cefalea
VO Via oral, IV: via intravenosa, PL: punción lumbar, IVAS: infección de vía aérea superior
Bibliografía
1. Langdon R, DiSabella MT. Pediatric Headache: An Overview. Curr Probl Pediatr Adolesc Health Care. 2017 Mar;47(3):44-65. doi: 10.1016/j.cppeds.2017.01.002.
2. Schwedt, T. J., Guo, Y. and Rothner, A. D. (2006), “Benign” Imaging Abnormalities in Children and Adolescents With Headache. Headache: The Journal of Head and Face Pain, 46: 387–398. doi:10.1111/j.1526-4610.2006.00371.x
3. R. Cancho Candela, A. Hedrera Fernández. Cefalea en el niño y adolescente. Pediatr Integral 2015; XIX (9): 632 – 639.
4. Lauck Sara M.,Gage Sandra. 28 – Headaches, Nelson Pediatric Symptom-Based Diagnosis, edited by Kliegman Robert M., et al. 2018, Pages 439-454. doi: 10.1016/B978-0-323-39956-2.00028-5.
5. Martín Fernández-Mayoralas, A. L. Fernández-Perrone, A. Fernández-Jaén. Cefaleas y migrañas en la adolescencia. Adolescere 2015; III (3): 9-28.
6. Mukhopadhyay Sourabh,White Catharine P. Evaluation of headaches in children. Paediatrics and Child Health, 2008 18:1. doi:10.1016/j.paed.2007.10.004.
7. The International Classification of Headache Disorders, 3rd edition (beta version). Cephalalgia. July 1, 2013; 33 (9); 629-808
8. Gofshteyn, Jacqueline S. et al. Diagnosis and Management of Childhood Headache. Curr Probl Pediatr Adolesc Health Care 2016 46:36-51
9. Slover Robin, Kent Sheryl. Pediatric Headaches. Advances in Pediatrics. 2015 62:283-293. doi:10.1016/j.yapd.2015.04.006.
10. Whitehouse WP, Agrawal S. Arch Dis Child Educ Pract Ed. 2017 102:58–65. doi:10.1136/archdischild-2016-311803.
11. Headaches in over 12s: diagnosis and management. Clinical guideline. Published: 19 September 2012. nice.org.uk/guidance/cg150