Sesión I Actualización: El adolescente cansado. Manejo en la consulta
Sesión I Actualización: El adolescente cansado.
Manejo en la consulta
D. Clemente Garulo.
Médico adjunto. Unidad de Reumatología Pediátrica. Hospital Infantil Universitario Niño Jesús. Madrid.
Adolescere 2023; XI (2): 7-17
Resumen
| No es infrecuente recibir en la consulta a adolescentes que se encuentren agotados y con falta de energía. En la mayoría de las ocasiones son problemas transitorios debidos a un aumento de las demandas educativas, actividades extraescolares o sociales, y que se resuelven una vez es posible regresar a una situación basal. En algunos casos este cansancio es debido a manifestaciones de enfermedades ya conocidas o en las que la fatiga es uno de los síntomas iniciales. Por último, en algunos adolescentes aparece una fatiga persistente (más de 3 o 6 meses) e inexplicable que impide mantener el rendimiento académico y las actividades sociales que se realizaban previamente. Estos pacientes pueden estar afectados por un síndrome de fatiga crónica (o encefalomielitis miálgica). Su diagnóstico precoz evita la realización de un exceso de pruebas complementarias inapropiadas y permite el inicio de un tratamiento individualizado cuyo principal objetivo es el retorno progresivo a las actividades habituales. El abordaje de estos pacientes es complicado para los profesionales que los atienden, siendo fundamental combinar intervenciones educativas y psicológicas, planificar actividades de forma progresiva y asegurar una correcta higiene del sueño. Los tratamientos farmacológicos suelen tener una eficacia limitada utilizados de forma aislada, pero pueden ser útiles para mejorar el sueño, disminuir la intensidad del dolor y aliviar la ansiedad y/o la depresión que pueden acompañar al resto de manifestaciones clínicas. |
Palabras clave: Síndrome de fatiga crónica; Encefalomielitis miálgica; Cansancio.
Abstract
|
It is not uncommon to attend adolescents who are exhausted and lacking energy. In most cases, these are transitory problems due to an increase in educational demands, and extracurricular or social activities, and which are resolved once they re¬turn to a baseline situation. In some cases, this fatigue is due to manifestations of known illnesses or in which fatigue is one of the initial symptoms. Finally, in some adolescents, persistent (more than 3 to 6 months) and unexplained fatigue appears and prevents them from maintaining their previous academic performance and social activities. These patients may be affected by chronic fatigue syndrome (or myalgic encephalomyelitis). Early diagnosis avoids an excess of inappropriate complementary tests and allows the initiation of individualized treatment with the main objective of a progressive return to normal activities. The approach to these patients is complicated for the professionals who care for them. It is essential to combine educational and psychological interventions, plan activities progressively and ensure proper sleep hygiene. Pharmacological treatments tend to have limited efficacy when used separately but can be useful in improving sleep, reducing the intensity of pain, and alleviating the anxiety and/or depression that can accompany the rest of the clinical manifestations. Key words: Chronic fatigue syndrome; Myalgic encephalomyelitis; Tiredness. |
Introducción
La adolescencia se caracteriza por ser una etapa de rápido desarrollo y de importantes cambios a nivel fisiológico, psicológico y social. Esto supone un aumento de las demandas que ocasiona que muchos adolescentes experimenten periodos transitorios de “cansancio” o de “falta de energía” tras esfuerzos prolongados (p.ej., periodos de exámenes, prácticas deportivas extenuantes, elevada actividad social). Sin embargo, con un tiempo de descanso adecuado (normalmente en días), es posible regresar a una situación basal.
En algunos casos el cansancio es debido a manifestaciones de enfermedades ya conocidas o en las que la fatiga es uno de los síntomas iniciales
En algunos casos este cansancio es debido a manifestaciones de enfermedades ya conocidas o en las que la fatiga es uno de los síntomas iniciales, como es el caso de enfermedades inflamatorias crónicas (p.ej., artritis idiopática juvenil, enfermedad inflamatoria intestinal), trastornos nutricionales (anorexia nerviosa, déficit de hierro) o psicológicas (p. ej., depresión). Así, un tratamiento dirigido de estas enfermedades mejorará la fatiga.
Por último, en algunos adolescentes aparece una fatiga persistente (más de 3 o 6 meses) e inexplicable, que ocasiona un grave deterioro del funcionamiento físico y de alteraciones cognitivas, impidiendo mantener el rendimiento académico y las actividades sociales que se realizaban previamente. En estos casos, no hay una mejoría clara con reposo o es necesario un periodo de tiempo excesivamente prolongado. Estos pacientes pueden estar afectados por un síndrome de fatiga crónica o encefalomielitis miálgica (SFC/EM). Es importante reconocer a los posibles afectados por este síndrome dado el mejor pronóstico que hay en adolescentes, en comparación con adultos, con un manejo adecuado(1).
Epidemiología
Se estima una prevalencia del SFC/EM en población pediátrica entre el 0,1 y el 0,75 %
El SFC/EM es una enfermedad globalmente endémica que afecta a todas las edades, etnias y grupos socioeconómicos. Aunque la mayoría de los casos son esporádicos, se han descrito brotes en diferentes partes del mundo. El sexo femenino es un factor de riesgo en adolescentes, donde es 3-4 veces más frecuente, pero en niños menores no parece existir diferencias por género. Se estima una prevalencia en población pediátrica entre el 0,1 y el 0,75 %, aunque puede variar dependiendo de los criterios empleados para su diagnóstico. Hay que destacar que menos de un 5 % de los adolescentes que cumplen los criterios para SFC/EM habían sido previamente diagnosticados(2).
Etiología
No existe una causa definitiva identificada para el SFC, aunque se han descrito una serie de factores predisponentes, desencadenantes y perpetuadores del cuadro(1).
Factores predisponentes
Entre los factores de riesgo para el desarrollo de un SFC en adultos se encuentran antecedentes de traumas infantiles (abuso sexual o físico, maltrato emocional y físico). Aunque depresión y ansiedad son frecuentes en niños y adolescentes con SFC no está claro si las alteraciones emocionales contribuyen al desarrollo del cuadro o son consecuencia de este. Tanto un ejercicio excesivo como una inactividad física prolongada parecen ser también factores de riesgo. Aunque era una enfermedad asociada a la clase socioeconómica alta, los estudios más recientes sugieren que realmente es más común en clases sociales más desfavorecidas, pero con mayor probabilidad de ser diagnosticada en familias con más recursos.
Factores desencadenantes
Algunos casos de SFC están precedidos por infecciones, especialmente por el virus de Epstein Barr (VEB). También se han descrito así cirugías, situaciones vitales estresantes o traumatismos como desencadenantes del cuadro.
Factores perpetuadores
El principal es el retraso en el diagnóstico de la enfermedad, debido a la búsqueda prolongada de una causa física por diferentes especialistas y la realización de numerosas pruebas complementarias. La realización de sobresfuerzos físicos o mentales, una atención excesiva a las manifestaciones clínicas y la falta de apoyo social son otros factores perpetuadores.
Patogenia
Diversos factores influyen en la patogenia del SFC/EM: infecciosos, genéticos, alteraciones vasculares, metabólicas…
La aparición de las manifestaciones clínicas del SFC/EM parecen el resultado de la participación de uno o varios de los siguientes factores(1,3):
- Infecciones: apoyado por el hecho de la aparición en brotes epidémicos en algunos casos y el inicio de los síntomas como un cuadro pseudogripal. También su relación con una infección por VEB; de hecho, hasta un 13 %, 7 % y 4 % de los pacientes con mononucleosis cumplen criterios de SFC/EM a los 6, 12 y 24 meses de la infección. Se han descrito casos después de otros microorganismos como herpesvirus 6, adenovirus o enterovirus. Algunos estudios en adultos han comunicado mejoría tras tratamientos antivirales.
- Disfunción inmune: se ha propuesto una respuesta inmunológica prolongada tras una infección como causante de SFC, apoyado por la publicación de casos con respuesta a tratamientos con inmunoglobulinas intravenosas o inmunosupresores como rituximab. Entre los cambios encontrados en población pediátrica se encuentra una disminución de la actividad de células NK, un aumento del número de autoanticuerpos o una respuesta alterada de las células T.
- Alteraciones vasculares: apoyado por la presencia habitual de una disfunción autonómica y una intolerancia ortostática, con mejoría de la fatiga con el tratamiento de esta. La presencia de anticuerpos frente a receptores β-adrenérgicos y muscarínicos se han relacionado con estas alteraciones(4). Las manifestaciones clínicas pueden ser resultado de una inadecuada regulación del flujo sanguíneo que no satisface las demandas de los tejidos y ocasiona hipoxia tisular y la acumulación de ácido láctico.
- Alteraciones metabólicas: los estudios sugieren un aumento del uso de aminoácidos y de ácidos grasos en el ciclo de Krebs y una disminución de la oxidación de glucosa y piruvato.
- Factores genéticos: apoyado por la agregación familiar en hasta un 20 % de los casos. Se han detectado variantes genéticas en los pacientes que están asociadas a una mayor vulnerabilidad al estrés/infecciones, disfunción mitocondrial, trastornos del sueño y desarrollo de enfermedades autoinmunes(5).
Aproximación al diagnóstico
Manifestaciones clínicas
El cuadro clínico puede comenzar tras una infección u otro tipo de estrés físico o mental, o de forma insidiosa. Los síntomas son persistentes, pero pueden fluctuar de un día para otro o durante un mismo día. Algunas personas experimentan una remisión parcial y temporal de los síntomas, que va seguida de una recaída tras un esfuerzo físico o mental superior a su nivel de tolerancia.
La fatiga en el SFC/EM es descrita como persistente (más de 3 o 6 meses), de intensidad moderada-grave, y se acompaña de una disminución sustancial de las actividades académicas, sociales y personales previas
Aunque la fatiga es una manifestación referida habitualmente por niños y adolescentes, en el SFC/EM la fatiga es descrita como persistente (más de 3 o 6 meses), de intensidad moderada-grave, y se acompaña de una disminución sustancial de las actividades académicas, sociales y personales previas. La descripción e interpretación de la fatiga por los adolescentes es variable, aunque suele representar una sensación de intensa falta de energía o de resistencia, cansancio o debilidad. Un 62 % de los pacientes atendidos en consulta no es capaz de asistir a clase más de 2 días a la semana y renuncian a todo tipo de aficiones.
Es muy característico el malestar post-ejercicio que no se alivia con reposo y/o con tiempos de recuperación muy prolongados
Es muy característico el malestar post-ejercicio, un incremento marcado de la fatiga tras realizar un sobreesfuerzo físico o mental mayor de lo que pueden tolerar, que no se alivia con reposo y/o con tiempos de recuperación muy prolongados (habitualmente de días a semanas). Esto puede ocurrir inmediatamente o, más frecuentemente, retrasarse tras un periodo posterior al esfuerzo que puede ser superior a un día. Esta intolerancia al esfuerzo es un síntoma clave, que se relaciona con la gravedad de la enfermedad y los niveles previos de funcionamiento.
Los afectados más graves pueden verse limitados para realizar actividades básicas de la vida diaria (p.ej., ir al baño, bañarse, ducharse o vestirse), mientras los casos más leves que antes eran muy activos (p.ej., deportistas), pueden seguir siéndolo, aunque mucho menos que antes.
Otra de las manifestaciones habituales son las alteraciones del sueño, especialmente de sueño no reparador. También aparecen insomnio de conciliación y despertares frecuentes.
Son frecuentes las quejas de deterioro cognitivo, como falta de memoria, atención y concentración (“olvidos frecuentes”), disminución de la claridad mental con lentitud de pensamiento y dificultades para comprender y procesar la información, y sensación de desorientación (“niebla cerebral”).
También van a ser habituales los dolores musculares y articulares, que pueden afectar a múltiples localizaciones y ser migratorios, pero sin signos locales de inflamación, y las cefaleas de tipo tensional o migrañoso.
Otras manifestaciones adicionales son:
- Intolerancia ortostática, definida por síntomas que sólo se producen o empeoran en posición erguida (en particular en bipedestación estática), y que mejoran al tumbarse (p.ej., palpitaciones, temblores, mareo, vértigo, debilidad, náuseas). Suele aparecer después de unos minutos en bipedestación (o incluso segundos) dependiendo de la gravedad.
- Sensibilidad excesiva a estímulos sensoriales como luz, ruido, cambios de temperatura o tacto.
- Síntomas frecuentes y prolongados de infecciones de las vías respiratorias superiores: cuadro pseudogripal, adenopatías cervicales, dolor de garganta, congestión nasal, disnea.
- Manifestaciones de un síndrome del intestino irritable como dolor abdominal crónico y alteración del hábito intestinal.
- Pérdida o aumento de peso.
- Inestabilidad emocional, ansiedad y depresión.
Los fenotipos no están relacionados con la duración de la enfermedad, con la edad de aparición o con manifestaciones depresivas
Pueden distinguirse 3 fenotipos en población pediátrica dependiendo de las manifestaciones asociadas predominantes (Tabla I)(6). Estos fenotipos no están relacionados con la duración de la enfermedad, con la edad de aparición o con manifestaciones depresivas.
Para medir la intensidad de los síntomas y poder hacer un seguimiento en el tiempo se pueden utilizar las siguientes escalas:
- Dolor: escala numérica 0-10.
- Fatiga: escala FACIT-F (Functional Assessment of Chronic Illness Therapy-Fatigue, disponible en: https://calc.artritis-il6.es/facit-f) o DSQ (DePaul Symptom Questionnaire, sobre todo las versiones corta y pediátrica, disponibles en https://csh.depaul.edu/about/centers-and-institutes/ccr/myalgic-encephalomyelitis-cfs/Pages/measures.aspx)(7).
- Despistaje de psicopatología: se puede usar el cuestionario Strengths and Difficulties Questionnaire (SDQ), disponible en https://www.sdqinfo.org/a0.html.
Exploración física
La exploración física puede ser completamente normal, incluyendo constantes vitales (Tª axilar, tensión arterial (TA), frecuencia cardiaca (FC), frecuencia respiratoria y saturación de O2) en situación basal. El estado nutricional es aceptable, aunque puede existir sobrepeso consecuencia de la inmovilidad prolongada.
Es relativamente frecuente la palidez cutánea y la frialdad acra, especialmente en bipedestación. En algunos casos pueden objetivarse adenopatías cervicales o faringitis no exudativa. Aunque no se objetivan articulaciones tumefactas ni limitadas, la palpación puede ser dolorosa y pueden cumplirse criterios de Beighton de hiperlaxitud articular. La fuerza está conservada y la sensibilidad es normal.
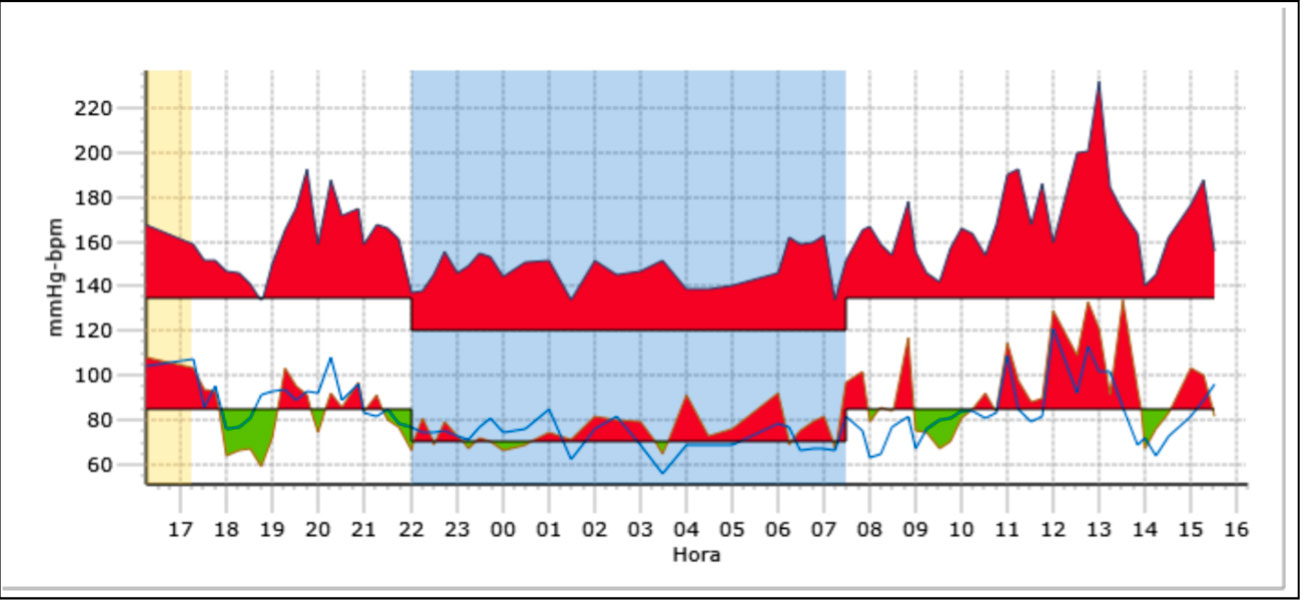
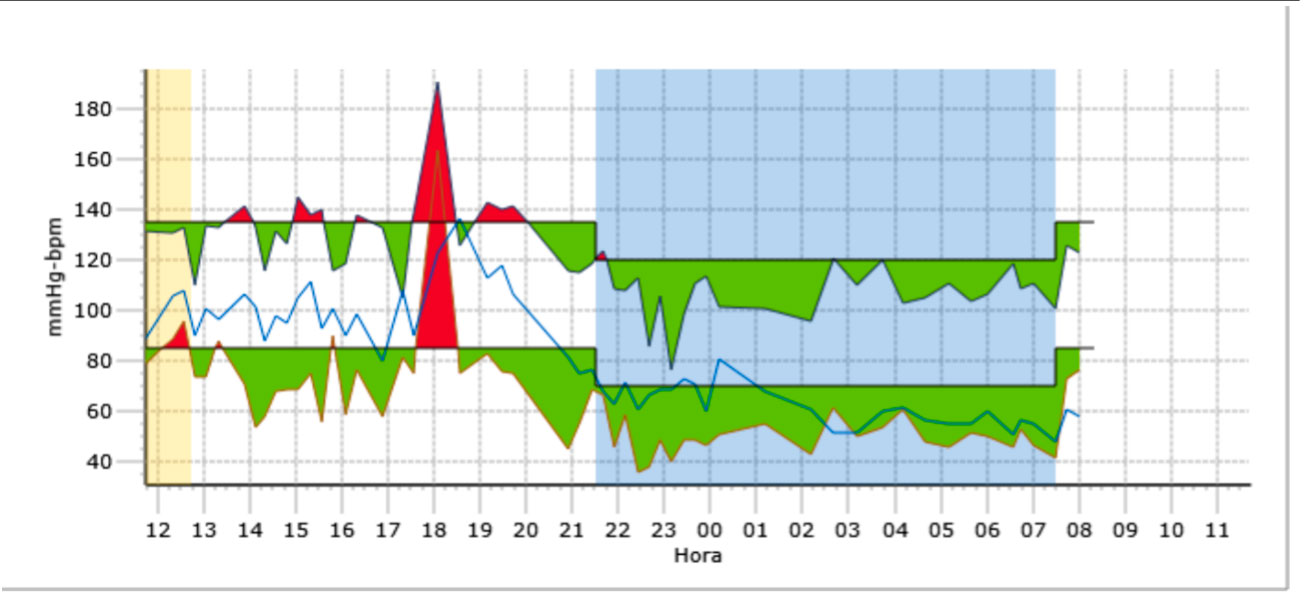
La presencia de una disfunción del sistema nervioso autónomo puede ponerse de manifiesto mediante la prueba de bipedestación activa o mesas basculantes
La presencia de una disfunción del sistema nervioso autónomo puede ponerse de manifiesto mediante la prueba de bipedestación activa o, en centros especializados, mediante mesas basculantes. En la prueba de bipedestación activa se toma la TA y la FC tras mantenerse en decúbito supino o en sedestación durante al menos 5 minutos. Posteriormente se pide al paciente que se ponga de pie, pudiendo apoyarse en la pared con los pies separados de esta, unos 5-15 cm.
Se determina la FC y la TA al minuto y a los 3,5 y 10 minutos y se comunican los posibles síntomas que aparezcan. Se pueden considerar los siguientes diagnósticos:
- Taquicardia postural: incremento de la FC en más de 40 latidos por minuto desde la situación basal o una FC de más de 120 latidos por minuto en bipedestación.
- Hipotensión ortostática: disminución de la TA sistólica en más de 20 mmHg o de la TA diastólica en más de 10 mmHg en los primeros 3 minutos en bipedestación, acompañado o no de síntomas.
- Hipotensión neuromediada: disminución de la TA sistólica en más de 25 mmHg sin incremento de la FC, asociado a la presencia de manifestaciones presincopales.
Pruebas complementarias
Por el momento, no hay ninguna prueba complementaria que sea diagnóstica de síndrome de fatiga crónica (SFC) / encefalomielitis miálgica (EM)
Por el momento, no hay ninguna prueba complementaria que sea diagnóstica de SFC/EM. Deben excluirse de forma razonable otras patologías, no siendo necesario un exceso de pruebas complementarias, pero disponiendo al menos de hemograma, VSG, proteína C reactiva, bioquímica completa con CPK, un estudio del hierro, vitamina B12, ácido fólico y 25OH vitamina D, sedimento de orina, hormonas tiroideas, marcadores de celiaquía y serología de VEB y citomegalovirus. También son aconsejables una radiografía de tórax y un ECG. El resto de las pruebas deben ser individualizadas en función de cada caso concreto.
Criterios de clasificación y diagnóstico diferencial
El SFC en niños y adolescentes puede ser definido según los criterios establecidos por el Institute of Medicine (actualmente, Academia Nacional de Medicina, EE. UU.), por los criterios de consenso canadienses o los criterios establecidos por Rowe et al. en 2017 (Tabla II)(1,8). Es importante tener en cuenta que la mayoría de las personas con fatiga persistente no tienen un SFC, sino que tienen manifestaciones causadas por otras enfermedades ya conocidas o incipientes, alteraciones importantes en el estado emocional o un estilo de vida predisponente.
Entre las enfermedades en las que la fatiga puede ser una manifestación principal se incluyen enfermedades inflamatorias crónicas (enfermedad inflamatoria intestinal, artritis idiopática juvenil, conectivopatías), endocrinológicas (hipo o hipertiroidismo, diabetes mellitus, enfermedad de Addison), cardiacas (cardiopatías descompensadas), pulmonares o neurológicas (miastenia gravis, esclerosis múltiple). También habrá que tener en cuenta alteraciones nutricionales (anemias, anorexia nerviosa) y trastornos psiquiátricos graves (depresión mayor). La presencia de pérdida de peso no intencionada, febrícula prolongada, elevación de reactantes de fase aguda, alteraciones significativas en exploración física o ideación suicida deben hacer descartar un SFC/EM.
El SFC/EM comparte muchas manifestaciones con la fibromialgia, en la que predominaría el dolor musculoesquelético generalizado sobre la fatiga, y la COVID-19 persistente o presencia de signos y síntomas que se desarrollan durante o hasta 3 meses después de la infección aguda por el virus SARS-CoV-2 y que se mantienen de forma continua o fluctuante durante más de 8 semanas. En este último caso puede documentarse una infección previa por SARS-CoV-2, que puede ser asintomática o con síntomas leves(9,10). La aproximación terapéutica en ambos casos puede ser similar al SFC/EM.
La depresión puede detectarse porque, aunque no tengan ganas de hacer ejercicio, se sienten mejor después de hacerlo, al contrario que suele ocurrir en el SFC/EM. Tanto depresión y ansiedad deben valorarse específicamente. En el rechazo escolar los adolescentes se niegan a volver a su centro educativo, mientras que en el SFC/EM los adolescentes aseguran que quieren ir, pero no tienen la energía suficiente.
Abordaje terapéutico
En la actualidad no existen fármacos aprobados para el síndrome de fatiga crónica (SFC)/ encefalomielitis miálgica (EM) ni terapias ampliamente aceptadas
En la actualidad no existen fármacos aprobados para el SFC/EM ni terapias ampliamente aceptadas. Aunque un estudio doble ciego con inmunoglobulinas intravenosas en adolescentes ofreció resultados prometedores, no ha podido ser replicado por otros grupos y los estudios en adultos no han sido concluyentes. Tampoco el uso de antivirales o rituximab (un anticuerpo monoclonal anti CD20) han conseguido resultados significativos.
Por tanto, el abordaje del SFC se basa fundamentalmente en intervenciones no farmacológicas como la programación supervisada de actividades y ejercicio, psicoterapia y una correcta higiene del sueño. La terapia cognitivo conductual es la intervención psicológica que presenta más evidencia de eficacia (limitada) en pacientes con SFC/EM no grave. Sin embargo, aunque algunos pacientes refieren una menor fatiga, su actividad física general no aumenta, lo que sugiere una adaptación a la enfermedad más que una recuperación real. Así pues, aunque estas intervenciones no farmacológicas pueden beneficiar a un subgrupo de pacientes con SFC/EM, no parecen revertir la enfermedad ni ofrecen una recuperación completa(11,12).
Dada la heterogeneidad en la presentación clínica, el tratamiento debe ser individualizado para atender a distintas comorbilidades como alteraciones del estado de ánimo o dolor crónico.
En estas situaciones puede ser útil asociar fármacos para contribuir a la mejoría clínica.
Educación sobre la enfermedad y psicoterapia
Debe reconocerse la fatiga, ya que no son simuladores, y evitar comentarios acerca de que el origen sea psicológico (no se trata de una enfermedad enteramente psicosomática)
La información apropiada a adolescentes y padres es fundamental para un éxito terapéutico. Se debe resaltar lo positivo de la ausencia de una lesión objetiva en la exploración física y en las pruebas complementarias, y que se descarte otro tipo de enfermedades potencialmente más graves como enfermedades autoinmunes o neoplasias. Aunque saber que existe una entidad conocida que engloba las manifestaciones que padecen, el diagnóstico de SFC/EM no excluye que en el seguimiento puedan aparecer otras manifestaciones que sugieran la presencia de comorbilidades asociadas (p.ej., síndrome del intestino irritable, ansiedad o depresión leves) u otros diagnósticos. También debe reconocerse la fatiga que padece el paciente, ya que no son simuladores, y evitar comentarios acerca de que el origen sea psicológico, ya que no se tratan de una enfermedad enteramente psicosomática. Es importante identificar cual es el síntoma más problemático para evitar el uso de muchos fármacos simultáneamente.
La terapia cognitivo conductual pretende contrarrestar los comportamientos y los pensamientos que perpetúan las manifestaciones clínicas, desviando la atención sobre la fatiga y colaborando en la programación supervisada de actividades. Debe explicarse que el objetivo no es que los pacientes no vuelvan a sentirse cansados, sino que vuelvan a realizar las actividades que precisen hacer, aunque puedan seguir presentando fatiga.
Programación supervisada de actividades y ejercicio físico
Consiste en establecer un objetivo (p.ej., acudir a diario al colegio) y un nivel basal de actividad después de recoger información acerca del tiempo que dedicaba el adolescente a estudios, deberes escolares, relaciones con amigos, actividades de ocio… Se debe planificar cuáles son las actividades que hay que realizar a lo largo del día o la semana, y organizarlo de manera que haya tiempo para realizarlas, pero también para descansar, resaltando cuáles son actividades prioritarias y cuáles pueden esperar. Puede ser necesario hablar con el centro escolar para facilitar un regreso gradual al mismo y clases de refuerzo para disminuir la ansiedad escolar, pero no se recomienda la educación en domicilio.
Al realizar cualquier actividad se debe intentar no llegar a un esfuerzo máximo o superar un umbral que provoque un deterioro de los síntomas y evitar las fluctuaciones en la actividad que presentan estos pacientes
Los periodos de descanso son importantes, siendo lo ideal descansar cuando aún se conserva algo de energía. Al realizar cualquier actividad se debe intentar no llegar a un esfuerzo máximo o superar un umbral que provoque un deterioro de los síntomas y evitar las fluctuaciones en la actividad que presentan estos pacientes, realizando un exceso de tareas y ocupaciones en los “días buenos” que repercute negativamente en los días posteriores, disminuyendo notablemente su funcionamiento. Para este fin puede ser útil la escala de Borg de percepción del esfuerzo (0 reposo; 2 muy ligero; 4 algo pesado; 6 más pesado; 8 muy, muy pesado; 10 extremo). Lo ideal es mantenerse entre 3-4 y parar cuando la actividad empieza a ser pesada.
Una vez que se ha acordado un nivel basal de actividades y se ha mantenido durante un mes, se aumenta el número e intensidad de actividades de forma gradual y acordada con el adolescente hasta llegar al objetivo marcado.
El ejercicio físico es necesario para prevenir el desacondicionamiento físico, que puede empeorar la sensación de cansancio y malestar post-ejercicio. Puede seguirse una estrategia similar al resto de actividades, con un programa gradual y adaptado a cada paciente, siendo de especial ayuda la valoración por fisioterapeutas. Se establece un nivel de ejercicio físico basal de baja intensidad que debe mantenerse durante una semana con un incremento progresivo del nivel de actividad.
Puede iniciarse con ejercicio aeróbico como paseos a un ritmo tranquilo (40-50 % de frecuencia cardiaca máxima) durante 15 minutos al menos 3-5 veces por semana. Una vez que el paciente consigue caminar 30 minutos a diario puede aumentarse el ritmo y la intensidad del paseo hasta un 50-70 % de frecuencia cardiaca máxima. Es conveniente avisar a padres y pacientes de la posibilidad de un incremento transitorio de los síntomas al aumentar la intensidad del ejercicio. Puede ser útil la utilización de dispositivos que permitan la medición de frecuencia cardiaca para controlar la progresión de los pacientes.
Además de ejercicio aeróbico, cuando sea posible, deben incluirse ejercicios de fuerza 2-3 veces por semana, con 2-3 series, según tolerancia, de 8-10 repeticiones, y realizar estiramientos globales al terminar la pauta de ejercicios.
Higiene del sueño
Una buena calidad del sueño tiene efectos beneficiosos sobre la fatiga y el resto de las manifestaciones del SFC/EM. Son importantes las medidas higiénicas del sueño
Una buena calidad del sueño tiene efectos beneficiosos sobre la fatiga y el resto de las manifestaciones del SFC/EM. Por ello, debe recomendarse establecer un horario de sueño fijo y regular adaptado a la edad y necesidades de cada persona evitando más de una hora de variación entre los días escolares y los días festivos. No es aconsejable un exceso de horas de sueño y, en el caso de que se hagan siestas, no deben ser muy largas ni cerca de la hora de acostarse. Es conveniente limitar el uso teléfonos móviles y otras pantallas en la cama, así como el consumo de sustancias estimulantes como chocolate o café por la tarde. Tampoco debe realizarse ejercicio físico importante en las dos horas previas a acostarse. En el caso de que no se consiga conciliar el sueño en menos de 30 minutos, puede ayudar levantarse y realizar una actividad tranquila como leer un libro. Esforzarse por dormir y mirar la hora con frecuencia puede ser contraproducente.
Puede valorarse el uso de remedios no farmacológicos como valeriana o manzanilla, o melatonina si existen problemas para la conciliación del sueño, comenzando con 2 mg 30-60 minutos antes de la hora deseada una vez que el paciente esté en la cama. La dosis puede incrementarse gradualmente hasta los 6 mg, pero si no es eficaz a esta dosis probablemente no lo será a dosis superiores. Cuando presentan despertares frecuentes puede emplearse amitriptilina 10-25 mg al día por la noche. El uso de benzodiazepinas debe ser el último recurso y de manera puntual, pudiendo utilizarse clonazepam 0,5-1 mg al acostarse si existe ansiedad importante o un síndrome de piernas inquietas asociado.
Tratamiento del dolor
En los pacientes que asocian dolor crónico pueden ser útiles las mismas recomendaciones que para los pacientes con fibromialgia, incluyendo ejercicio físico suave y una higiene del sueño adecuada. Paracetamol y antiinflamatorios no esteroideos suelen prescribirse al inicio de la enfermedad, pero son habitualmente inefectivos para controlar el dolor. Por ello no se recomienda su administración de forma continuada, pudiendo ser útil la administración intermitente “a demanda” durante periodos de 7-10 días y para controlar el dolor musculoesquelético originado por osteocondrosis o lesiones deportivas. Los opioides deben evitarse por su pobre eficacia y el posible desarrollo de una dependencia a los mismos.
Antiepilépticos como gabapentina y pregabalina han demostrado una disminución estadísticamente significativa pero clínicamente modesta del dolor en adultos con fibromialgia, por lo que puede considerarse su uso en adolescentes teniendo en cuenta posibles efectos secundarios como somnolencia, mareo y ganancia de peso. Los antidepresivos tricíclicos (amitriptilina) a dosis bajas pueden disminuir el dolor de forma transitoria, disminuyendo la respuesta inicial con su uso prolongado. Se recomienda iniciar el tratamiento con dosis bajas e ir aumentando dosis según respuesta.
Otras intervenciones
Para el manejo de la intolerancia ortostática se recomienda incrementar la ingesta de líquidos y el consumo de sal, así como el uso de medias de compresión (20-30 mmHg) e incrementar el tono muscular de extremidades inferiores. En el caso de que estas medidas no fueran suficientes, se han utilizado fármacos para modificar las fluctuaciones en la frecuencia cardiaca y la tensión arterial (p.ej., beta-bloqueantes), aunque debe consultarse con un cardiólogo antes de indicar su uso(13).
Cuando coexistan alteraciones graves del estado de ánimo o ansiedad será necesario la valoración por psicólogos y/o psiquiatras infantiles y la instauración de un tratamiento con psicofármacos. Hay que tener en cuenta que en este grupo de pacientes podemos encontrar tanto dificultades para la alimentación como obesidad por una inmovilización prolongada, por lo que debe controlarse el peso y realizar una valoración nutricional durante el seguimiento. No está demostrado que dietas de exclusión (gluten, proteínas de leche de vaca) sean beneficiosas, al igual que el uso de suplementos de magnesio o vitaminas (B1, B2, B6, B12, C, D).
Pronóstico
El pronóstico de niños y adolescentes con SFC se considera mejor que en adultos, mostrando los estudios una recuperación buena o completa de los síntomas en el 54-94 %
El pronóstico de niños y adolescentes con SFC se considera mejor que en adultos, mostrando los estudios una recuperación buena o completa de los síntomas en el 54-94 %. La evolución en forma de remisiones y recaídas es frecuente si no se siguen las recomendaciones indicadas y un tercio de los pacientes deben modificar el número e intensidad de actividades para mantener la mejoría(14).
Un estudio reciente con seguimiento a largo plazo de 784 jóvenes con SFC/EM demostró una duración media de la enfermedad de 5 años(1-15), con un 68 % de recuperación a los 10 años. Aunque todos mejoraron funcionalmente, un 5 % seguían encontrándose mal. No se han detectado claros factores predictores de recuperación presentes al inicio de la enfermedad. Sin embargo, la asociación durante el seguimiento con ansiedad, depresión y, en menor medida, dolor, dificultan la recuperación. Por el contrario, el apoyo de los profesionales sanitarios, la permanencia en el sistema educativo (cuando es lo suficientemente flexible para adaptarse a la enfermedad) y la aplicación de un tratamiento individualizado, en el que el adolescente esté implicado activamente en la gestión de sus actividades académicas, deportivas y sociales, aumenta las probabilidades de recuperación completa(15).
Tablas y figuras
Tabla I. Fenotipos de síndrome de fatiga crónica en niños
|
Fenotipo |
Descripción y puntos clave |
|
Musculoesquelético |
|
|
Migraña |
|
|
Dolor de garganta |
|
Tabla II. Criterios diagnósticos para el síndrome de fatiga crónica
|
Criterios del Institute of Medicine |
|
Síntomas requeridos:
Al menos uno de los siguientes síntomas:
|
|
Criterios para el diagnóstico pediátrico (Rowe et al. 2017) |
|
Síntomas requeridos:
Además, se requieren 2 de los siguientes 3 grupos de síntomas:
Para el diagnóstico es necesario que:
|
Bibliografía
- Rowe PC, Underhill RA, Friedman KJ, Gurwitt A, Medow MS, Schwartz MS, et al. Myalgic encephalomyelitis/chronic fatigue syndrome diagnosis and management in young people: A primer. Vol. 5, Frontiers in Pediatrics. Frontiers Media S.A.; 2017.
- Jason LA, Katz BZ, Sunnquist M, Torres C, Cotler J, Bhatia S. The Prevalence of Pediatric Myalgic Encephalomyelitis/Chronic Fatigue Syndrome in a Community-Based Sample. Child Youth Care Forum. 2020 Aug 1;49(4):563–79.
- Fluge Ø, Tronstad KJ, Mella O. Pathomechanisms and possible interventions in myalgic encephalomyelitis/chronic fatigue syndrome (ME/CFS). Vol. 131, Journal of Clinical Investigation. American Society for Clinical Investigation; 2021.
- Gravelsina S, Vilmane A, Svirskis S, Rasa-Dzelzkaleja S, Nora-Krukle Z, Vecvagare K, et al. Biomarkers in the diagnostic algorithm of myalgic encephalomyelitis/chronic fatigue syndrome. Front Immunol. 2022 Oct 10;13.
- Das S, Taylor K, Kozubek J, Sardell J, Gardner S. Genetic risk factors for ME/CFS identified using combinatorial analysis. J Transl Med. 2022 Dec 1;20(1).
- May M, Emond A, Crawley E. Phenotypes of chronic fatigue syndrome in children and young people. Arch Dis Child. 2010 Apr;95(4):245–9.
- Jason LA, Sunnquist M. The development of the DePaul Symptom Questionnaire: Original, expanded, brief, and pediatric versions. Front Pediatr. 2018;6.
- Nacul L, Authier FJ, Scheibenbogen C, Lorusso L, Helland IB, Martin JA, et al. European Network on Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (EUROMENE): Expert Consensus on the Diagnosis, Service Provision, and Care of People with ME/CFS in Europe. Medicina (Kaunas). 2021 May 19;57(5).
- Morrow AK, Malone LA, Kokorelis C, Petracek LS, Eastin EF, Lobner KL, et al. Long-Term COVID 19 Sequelae in Adolescents: the Overlap with Orthostatic Intolerance and ME/CFS. Vol. 10, Current Pediatrics Reports. Springer Science and Business Media, LLC; 2022. p. 31–44.
- Gatell Carbó A, López Segura N, Domènech M, Méndez Hernández M, Rius Gordillo N, Soriano-Arandes A. Recomendaciones para el manejo clínico de la COVID-19 persistente en la infancia y adolescencia. Pediatr Integral. 2021;XXV(8):445.e1-445.e11.
- Rowe K. Chronic Fatigue Syndrome/Myalgic Encephalomyelitis (CFS/ME) in Adolescents: Practical Guidance and Management Challenges. Adolesc Health Med Ther. 2023 Jan;Volume 14:13–26.
- Brigden A, Loades M, Abbott A, Bond-Kendall J, Crawley E. Practical management of chronic fatigue syndrome or myalgic encephalomyelitis in childhood. Arch Dis Child. 2017 Oct 1;102(10):981–6.
- Kizilbash SJ, Ahrens SP, Bruce BK, Chelimsky G, Driscoll SW, Harbeck-Weber C, et al. Adolescent fatigue, POTS, and recovery: A guide for clinicians. Vol. 44, Current Problems in Pediatric and Adolescent Health Care. Mosby Inc.; 2014. p. 108–33.
- Gregorowski A, Simpson J, Segal TY. Child and adolescent chronic fatigue syndrome/ myalgic encephalomyelitis: Where are we now? Vol. 31, Current Opinion in Pediatrics. Lippincott Williams and Wilkins; 2019. p. 462–8.
- Rowe KS. Long term follow up of young people with chronic fatigue syndrome attending a pediatric outpatient service. Front Pediatr. 2019;7(FEB).