Epilepsia en el adolescente
Epilepsia en el adolescente
P. Tirado Requero.
Médico adjunto. Servicio Neurología. Hospital Universitario Infantil La Paz.
Fecha de recepción: 28 de enero 2018
Fecha de publicación: 28 de febrero 2018
Adolescere 2018; VI (1): 44-50
Resumen
|
La adolescencia es una edad estrechamente relacionada con la epilepsia, tanto por la desaparición de algunos síndromes epilépticos (Epilepsia Ausencia de la infancia y la Epilepsia Rolándica Benigna de la Infancia), como por el debut de otros (Epilepsia Mioclónica Juvenil y Epilepsia Ausencia Juvenil). La respuesta global a los fármacos antiepilépticos es buena, hasta un 70% lograrán un control completo de las crisis (58% con un solo fármaco), similar a la población general, pero con peores respuestas en el sexo femenino y una alta tasa de incumplimiento terapéutico (hasta el 35%).Es muy frecuente la comorbilidad psiquiátrica y social, presentando hasta un tercio de los pacientes Trastorno por Déficit de Atención e Hiperactividad. Además algunos síndromes epilépticos, como la Epilepsia Mioclónica Juvenil, se asocia con otras patologías psiquiátricas. Los síntomas ansiosos y depresivos, así como la percepción de peor calidad de vida, guarda estrecha relación con la forma en que la familia enfoca y vive la enfermedad del paciente. Palabras clave: Adolescente, Epilepsia, Epilepsia Mioclónica Juvenil (EMJ), Trastorno por Déficit de Atención e Hiperactividad, ansiedad, depresión. |
Abstract
|
Adolescence is a crucial age for epilepsy, as it marks the disappearance of some epileptic syndromes (Childhood Absence Epilepsy and Benign Rolandic Epilepsy of Childhood), as well as the onset of others (Juvenile Myoclonic Epilepsy and Juvenile Absence Epilepsy). The overall response to antiepileptic drugs is good, as up to 70% will achieve complete control of seizures (58% with a single drug), similar to the general population, but with worse response in the female sex and with a high rate of noncompliance to therapy (up to 35%). Psychiatric and social comorbidities are very common, as up to a third of patients will also present Attention Deficit Hyperactivity Disorder. In addition, some epileptic syndromes, such as Juvenile Myoclonic Epilepsy, are associated with other psychiatric disorders. Symptoms of anxiety and depression, as well as the perception of worse quality of life, are closely related to the way in which the family deals with the patient’s illness. Key words: Adolescent, Epilepsy, Juvenile Myoclonic Epilepsy (JEM), Attention Deficit Hyperactivity Disorder, anxiety, depression. |
Introducción
La adolescencia es una edad estrechamente relacionada con la epilepsia, tanto por la desaparición de algunos síndromes epilépticos, como por el debut de otros
La epilepsia es común en niños y adolescentes con una prevalencia de 3.2-5.5 / 1000. El conocimiento de los síndromes de epilepsia que remiten antes de la adolescencia, persisten durante la adolescencia o comienzan en la adolescencia es fundamental para el tratamiento de este grupo de edad.
Poco se sabe sobre el efecto intrínseco de la pubertad en la etiopatogenicidad de la epilepsia, pero se han podido observar relaciones con los cambios hormonales en los individuos, como la asociación de las crisis con el ciclo menstrual durante muchos años. En general, no se cree que la pubertad influya en la frecuencia de las convulsiones. Sin embargo, si se piensa que el estrógeno aumenta la actividad epileptiforme; así como la testosterona y la progesterona disminuyen las descargas epileptiformes. Estos efectos están mediados por la transmisión del ácido gammaaminobutírico (GABA)(1).
Independientemente de los factores biológicos que determinen el inicio de algunos síndromes epilépticos en la adolescencia, ó el final de otros típicos de la infancia, la presencia de esta enfermedad en esta etapa tan vulnerable del desarrollo físico y emocional del individuo, exige al médico responsable un conocimiento profundo de la evolución de la enfermedad, respuesta esperada al tratamiento, dificultades en la adherencia y posible aparición de síntomas cognitivos, atencionales, emocionales y sociales.
Los síndromes que más frecuentemente debutan en la infancia y desaparecen en la adolescencia son la Epilepsia Ausencia de la infancia y la Epilepsia Rolándica Benigna de la Infancia
A continuación vamos a exponer las características de la epilepsia en la adolescencia siguiendo el esquema:
• Epilepsia de nueva aparición en la adolescencia
• Evolución de las epilepsias infantiles en la adolescencia
• Epilepsia y TDAH
• Efectos cognitivos de la medicación y adherencia al tratamiento
• Marco psicológico
Epilepsia de nueva aparición en la adolescencia
Por el contrario, es frecuente el debut de otros que pueden perdurar en la edad adulta, los más representativos de los cuales son la Epilepsia Mioclónica Juvenil y Epilepsia Ausencia Juvenil
Existen síndromes específicos de epilepsia que característicamente comienzan durante la adolescencia y pueden implicar una carga neurológica significativa. El conocimiento de estos síndromes es importante en el tratamiento e implicaciones pronosticas, que generalmente se extienden hasta la edad adulta.
Las epilepsias idiopáticas generalizadas son el grupo más frecuente con inicio en la adolescencia. Estos son probablemente de origen poligénico y representan un continuo biológico. La epilepsia mioclónica juvenil (EMJ) es la forma más común. Otras relevantes que detallamos a continuación son: epilepsia ausencia juvenil, epilepsia con ausencias mioclónicas y epilepsias focales frecuentes como la Epilepsia occipital de la infancia de tipo tardío (tipo Gastaut) y la Epilepsia frontal nocturnas autosómica dominante.
Epilepsia mioclónica juvenil: es la más frecuente. Se inicia entre los 12-18 años de edad(2) y se caracteriza por crisis a los pocos minutos de despertar, de tipo mioclónico y de predominio en hombros y manos, sin alteración de conciencia. La gran mayoría de los pacientes presentan crisis tónico-clónicas generalizadas en relación con la privación de sueño, alcohol o la menstruación. Algunos asocian también ausencias.
El EEG ictal muestra actividad de base normal con paroxismos generalizados punta onda y polipunta onda a 3-5 Hz.
Aproximadamente 5-15% fueron diagnosticados previamente de Epilepsia Ausencia de la Infancia que remitió completamente, y hasta un tercio tienen antecedentes familiares de epilepsia.
Está demostrada la alta asociación de algunos síndromes de epilepsia presentes a esta edad (Epilepsia Ausencia Infantil, Epilepsia focal no lesional y Epilepsia Mioclónica juvenil) con comorbilidad psiquiátrica y social
Se ha considerado durante muchos años como un trastorno de por vida con una alta tasa de recurrencia al retirar los fármacos antiepilépticos(3) sin embargo, hasta un 25 % puede permanecer libre de crisis tras la retirada(4). Además, las convulsiones mioclónicas a menudo pueden disminuir o desaparecer en la cuarta década. Sin embargo, se observa un curso farmacorresistente hasta en el 15%.
Está demostrada la existencia de comorbilidad asociada y efectos sociales negativos sin relación directa con las crisis. Su naturaleza puede ser conductual, cognitiva, y psiquiátrica, produciendo consecuentemente problemas escolares y sociales tempranos.
En la edad adulta(5) se han observado mayor prevalencia de trastornos psiquiátricos, dificultades para mantener relaciones sociales y de pareja, embarazo no deseado y desempleo.
Esta afectación neuropsicológica y social se ha observado también en la Epilepsia Ausencia de la Infancia y en la Epilepsia focal no lesional.
Epilepsia de ausencia juvenil: inicio en torno a los 10 años, pero puede darse desde los 5 hasta los 20 años. Cursa con ausencias típicas, menos frecuentes que las de la infancia. Además, hay otros tipos de crisis asociadas: tónico-clónicas (80% de los casos) y mioclónicas (20%). El EEG ictal se caracteriza por una punta-onda lenta generalizada a más de 3 Hz.
La tasa de remisión a los 5 años es de 56-65%(6,7) generalmente ocurre de 3 a 8 años después del inicio de las crisis. Sin embargo, en un tercio restante, las crisis persisten, o evolucionan a Epilepsia Mioclónica Juvenil en el 5-15%.
Es importante hacer un diagnóstico diferencial con otras epilepsias de diferente pronóstico como la epilepsia mioclónica, epilepsia con mioclonía palpebral (síndrome de Jeavon), mioclonía perioral con ausencia, así como ausencias asociadas con enfermedad metabólica específica (deficiencia del transportador de glucosa) o anomalías cromosómicas (anillo cromosoma 20, microdeleción 15q13.3).
Las dificultades neurocognitivas leves se presentan con relativa frecuencia(8) e incluyen déficits cognitivos sutiles y dificultades lingüísticas, TDAH o trastornos afectivos / de ansiedad. Parece haber un riesgo mayor con la duración más larga de la enfermedad y una frecuencia de crisis más alta.
Epilepsia occipital de la infancia de tipo tardío (tipo Gastaut): inicio en torno a los 8 años con crisis frecuentes que se caracterizan por una clínica visual con alucinaciones, amaurosis, desviación ocular…, puede haber generalización secundaria y, en algunos casos, queda una cefalea residual migrañosa. El EEG interictal se suele encontrar alterado con complejos punta-onda en regiones occipitales o temporales posteriores activados con el cierre ocular. Se recomienda tratamiento con carbamacepina o clobazam(9).
Epilepsia frontal nocturna autosómico dominante: crisis nocturnas distónicas, muy frecuentes por las noches, con manifestaciones al despertar de expresión de terror, automatismos o hiperquinetismo. Pueden generalizarse. Para diagnosticarlas es necesario hacer un EEG de sueño, en el que se objetiva alteraciones epileptiformes y crisis de origen frontal.
Evolución de las epilepsias de la infancia en el adolescente
A continuación expondremos los síndromes epilépticos de inicio en la infancia, y su evolución en la adolescencia: epilepsia benigna con puntas centrotemporales ó epilepsia rolándica benigna de la infancia (ERBI), epilepsia focal no lesional en niños normales (NLFN) y la epilepsia ausencia de la infancia (EAI).
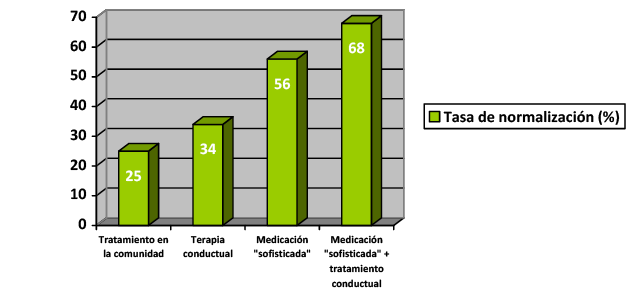
La respuesta global a los fármacos antiepilépticos es buena, hasta un 70% lograrán un control completo de las crisis (58% con un solo fármaco)
ERBI es un síndrome epiléptico que en la mayoría de los casos evoluciona a la remisión antes de la edad adulta, generalmente en la adolescencia. También un porcentaje alto (65%) de los pacientes con epilepsia de ausencia infantil (EAI) logran la remisión completa. Sin embargo, el 15% de los pacientes con EAI que remiten inicialmente durante sus años de infancia más tarde desarrollan epilepsia mioclónica juvenil (EMJ) como adolescentes(10).
Una minoría significativa de NLFN (~ 35%) y la mayoría de los pacientes con Epilepsia mioclónica juvenil (EMJ) continúan teniendo epilepsia activa en la edad adulta. Además, los pacientes con EAI, EMJ y NLFN corren el riesgo de sufrir una serie de resultados sociales adversos significativos que requieren asesoramiento y asesoramiento continuo.
Epilepsia Ausencia Infantil: aparición de crisis de ausencia muy breves y repetidas a partir de los 3 años de edad, con un pico de incidencia entre los 5-7 años, en niños con desarrollo piscomotor previo normal.
En ocasiones resulta complicado hacer el diagnóstico diferencial con la Epilepsia Ausencia Juvenil, puesto que en ambas el tipo de crisis más frecuente son las ausencias. Además del punto de corte de la edad en 10 años, otras características que las diferencian son la mayor frecuencia de crisis tónico clónica generalizadas y mioclonías en la EAJ con respecto a la EAI, y la menor frecuencia de ausencias (en la EAI son diarias). En el EEG de ambas aparece la punta onda generalizada, en la infantil a un ritmo de 3 Hz, en la juvenil más lenta(10).
El fármaco de elección es VPA ó ESM. Las crisis se controlan en un 90%, con un riesgo de recurrencia en la retirada del 16%. Los casos que no remiten suelen evolucionar a Epilepsia Mioclónica Juvenil.
Epilepsia rolándica benigna de la infancia (ERBI): se caracteriza principalmente por convulsiones nocturnas al inicio del sueño o justo antes del despertar. En el 75% de los casos, el trastorno comienza entre los 7 y 10 años de edad. Durante la fase activa, se pueden observar dificultades cognitivas, lingüísticas y de comportamiento de intensidad mínima a moderada. En todos los casos, la asistencia médica, educativa y psicológica (si es necesaria) con apoyo a los pacientes y las familias es importante y debe revisarse periódicamente durante la infancia.
Menos del 2% de los pacientes tienen un curso más severo asociado con dificultades para controlar las crisis, y de forma excepcional evolucionan a una encefalopatía epiléptica (Punta onda continua durante el sueño lento). La remisión ocurre generalmente dentro de los 3-4 años del inicio y casi siempre antes de los 16 años(11) . El pronóstico es excelente, independientemente del tratamiento antiepiléptico. Además, un reciente estudio poblacional encontró que 30 años después del diagnóstico inicial de ERBI, todos los pacientes estaban en remisión completa sin medicamentos antiepilépticos (12). Las variables sociales de educación, empleo, pobreza, trastornos psiquiátricos, aislamiento, matrimonio y divorcio eran similares a los de la población general. Aunque las dificultades cognitivas ocasionales fueron evidentes durante la fase activa de su epilepsia en la infancia, estas no parecen tener efectos significativos a largo plazo. En general, los neurólogos o psiquiatras no siguen ni tratan a los adultos jóvenes con ERBI por problemas sociales o médicos relacionados con la epilepsia.
Epilepsia focal no lesional en niños sin discapacidad intelectual (NLFN) Este grupo de epilepsia se presenta con crisis focales (tanto en la semiología como en el electroencefalografía [EEG]) sin alteración ni lesión en la neuroimagen, con un examen neurológico y una inteligencia normal. Los jóvenes con NLFN representan del 20 al 30% de los niños con epilepsia(13-14).
Después del seguimiento a largo plazo (>10 años después del diagnóstico inicial), dos tercios alcanzarán la remisión total (definida como al menos 5 años sin necesidad de medicamentos antiepilépticos)(13-14). En los que permanecen las crisis, la mitad pueden llegar a ser farmacorresistentes. El curso de la epilepsia puede seguir a menudo un patrón recurrente y remitente. Cuando existe una lesión y / o causa conocida, la evolución y el pronóstico es peor. La diferencia en la probabilidad de remisión a largo plazo es de alrededor del 65% frente al 35%(5).
Al igual que EAI y EMJ, las complicaciones sociales no relacionadas con los ataques y las comorbilidades se observan con frecuencia en el NLFN(15-16). Estos problemas pueden preceder al diagnóstico inicial de epilepsia u ocurrir temprano en el curso de la patología, e incluyen problemas escolares tempranos(14-17-18) y problemas conductuales, cognitivos, psiquiátricos y psiquiátricos.
Estos problemas a menudo persisten en la adolescencia media y hasta el 67% tienen mayores dificultades en la edad adulta(5) incluyendo la imposibilidad de graduación en secundaria, un trastorno psiquiátrico diferente del trastorno de déficit de atención (ADHD), dificultades para mantener relaciones sociales y de pareja, embarazo no deseado y desempleo.
La epilepsia del lóbulo temporal asociada con la esclerosis del hipocampo. La historia clínica característica, la semiología de las convulsiones y los hallazgos de la resonancia magnética han permitido establecer un síndrome de epilepsia. La aplicación de estos mismos criterios a niños y adolescentes revela que la esclerosis del hipocampo es la lesión más común responsable de su epilepsia del lóbulo temporal intratable. La esclerosis del hipocampo probablemente esté infradiagnosticada en niños. La seguridad y eficacia de la cirugía de epilepsia en el grupo de edad es excelente.
Epilepsia y TDAH
El Trastorno por Déficit de Atención e hiperactividad es muy frecuente en la población adolescente epiléptica, hasta un tercio de estos pacientes presentarán síntomas compatibles
Alrededor de un tercio de los niños y adolescentes con epilepsia también tienen trastorno de hiperactividad / impulsividad con déficit de atención (TDAH). La posible relación entre epilepsia y TDAH aún no está clara, y los síntomas de TDAH (como falta de atención, hiperactividad, trastornos del comportamiento) se consideran con frecuencia como efectos adversos de los fármacos antiepilépticos (FAE).
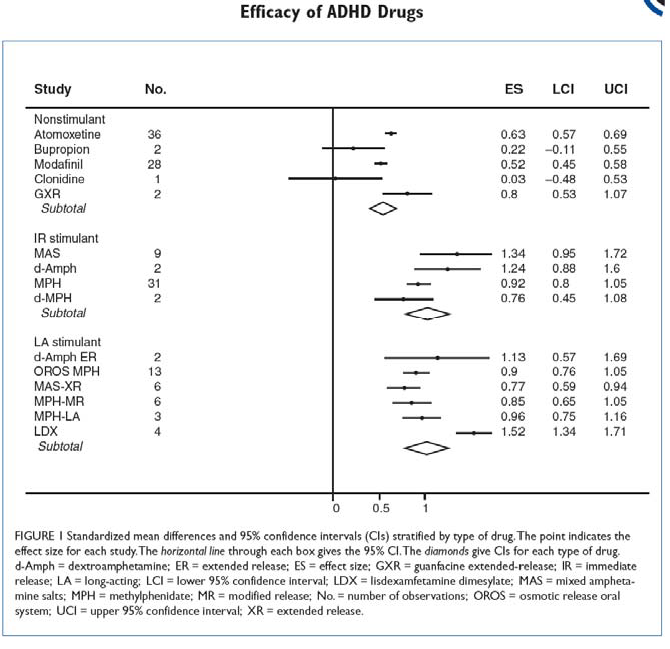
Debido a que el TDAH afecta significativamente la calidad de vida de los pacientes con epilepsia, el manejo clínico de este trastorno neuropsiquiátrico debe ser una prioridad(19). El metilfenidato es eficaz en la mayoría de los niños y adolescentes con síntomas de TDAH y epilepsia comórbida, sin un aumento significativo del riesgo de convulsiones, aunque los datos son todavía limitados con pocos ensayos controlados.
Otro factor importante en el manejo de un adolescente con epilepsia y TDAH es la influencia de los Fármacos antiepilépticos en los síntomas atencionales, conductuales ó cognitivos(20).
A continuación enumeramos los más relevantes:
Si el paciente asocia TDAH con epilepsia, estaría indicado el tratamiento con psicoestimulantes, con un control más estrecho de la epilepsia y de los fármacos antiepiléptico, algunos de los cuales pueden exacerbar los síntomas conductuales y atencionales
El fenobarbital es el medicamento reportado con mayor frecuencia como inductor de los síntomas de TDAH, seguido de topiramato, ácido valpróico y fenitoína en menor grado. El perampanel puede conducir a una alta incidencia de comportamiento hostil / agresivo, que aumenta con dosis más altas.
Otros medicamentos que pueden ejercen efectos favorables sobre el comportamiento son la lacosamida, Carbamazepina y lamotrigina; estos 2 últimos también pueden mejorar la concentración.
La gabapentina y la vigabatrina tienen efectos adversos limitados sobre la cognición.
Terapia antiepiléptica en el adolescente
Es difícil hacer una aproximación al perfil de respuesta al tratamiento en un adolescente con epilepsia, puesto que esto va a depender del tipo de epilepsia, del fármaco empleado y de las características físicas emocionales y sociales.
Sin embargo se han realizado estudios en diferentes series de pacientes que debutaron con epilepsia entre los 12 y los 16 años y se han observado patrones evolutivos significativos en el primer año de seguimiento.
Hasta un 58 % de los pacientes se controlaron con una sola medicación en el primer año y 13% necesitaron al menos dos medicamentos para controlar las convulsiones.
El 16% de los pacientes tuvieron al menos 1 ataque el año anterior. Se observó una alta asociación a un diagnóstico de epilepsia mioclónica juvenil, la presencia de convulsiones ó crisis mioclónicas coexistentes, la edad <o = 14.5 años en el momento del diagnóstico inicial y la presencia de problemas de cumplimiento(1).
El sexo femenino y la presencia de problemas de cumplimiento se asociaron con mayor probabilidad de aparición de crisis. Hasta un 35% de los adolescentes en tratamiento con fármacos antiepilépticos reconocieron no haber tomado el tratamiento en el mes previo a la visita.
Las peores respuestas se observan en el sexo femenino y en los pacientes que no mantienen una buena adherencia al tratamiento (hasta el 35% de los adolescentes reconocen no haber tomado en alguna ocasión el tratamiento en el último mes)
Por lo general, se puede esperar un buen resultado para la epilepsia de inicio en la adolescencia a corto plazo.
Marco psicológico
Los adolescentes refieren síntomas ansiosos y depresivos en relación al padecimiento de la epilepsia, así como peor calidad de vida
La epilepsia durante la adolescencia puede impedir el desarrollo de la independencia psicosocial y los procesos biológicos típicos de maduración. En los estudios psicológicos realizados a adolescentes y familiares, se ha observado que la patología que prevalece en los pacientes es la ansiedad y la depresión, y que está íntimamente ligado a la percepción de enfermedad de la familia. Además los adolescentes refieren una calidad de vida significativamente peor en comparación con otros adolescentes que no padecen la enfermedad.
En estudios que examinaron en paralelo las experiencias y percepciones de pacientes adolescentes con epilepsia y sus cuidadores, se observó que informaron de manera similar en casi todos los dominios(21), condiciones comórbidas, adherencia a las terapias, productividad, uso estimado de los tratamientos de rescate y relación con el médico. Estos resultados nos arrojan información muy valiosa de la trascendencia de la vivencia familiar en el adolescente. Aunque el paciente haya traspasado la niñez, el peso de la emoción familiar sigue siendo la clave en su percepción de la enfermedad.
Estos síntomas guardan una estrecha relación con la forma en que la familia enfoca y vive la enfermedad del paciente
La presencia de la epilepsia durante la adolescencia, sea de inicio en este periodo ó presente desde la infancia, está relacionado con un incremento significativo de la depresión y la ansiedad en el paciente y la familia(22) .La ansiedad social es el síntoma de ansiedad predominante, mientras que el estado de ánimo irritable y la desesperación son los síntomas más frecuentes de la depresión. Los síntomas depresivos se asocian a la mayor preocupación de los padres sobre la condición del niño y su futuro, así como menor bienestar de la familia. La gravedad y la duración de la epilepsia y la polifarmacia están asociadas con la preocupación de los padres y el bienestar de la familia, pero no con la ansiedad y la depresión en los niños.
Los estudios neuropsicológicos de la adolescencia recomiendan el desarrollo de programas de manejo de la epilepsia centrado en los adolescentes para ayudar a aliviar las preocupaciones del paciente y también a controlar de forma independiente su epilepsia a medida que pasan a la edad adulta.
Bibliografía
1. A profile of adolescent-onset epilepsy. Simard-Tremblay E1, Shevell M. J Child Neurol. 2009 Oct;24(10):1243-9. doi: 10.1177/0883073809334381. Epub 2009 Aug 11.
2. Kasteleijn-Nolst Trenit e DG, Schmitz B, Janz D, et al. Consensuson diagnosis and management of JME: from founder’sobservations to current trends. Epilepsy Behav 2013;28(Suppl. 1):S87–S90.17.
3. Geithner J, Schneider F, Wang Z, et al. Predictors for long-termseizure outcome in juvenile myoclonic epilepsy: 25–63 years offollow-up. Epilepsia 2012;53:1379–1386.18.
4. Baykan B, Altindag EA, Bebek N, et al. Myoclonic seizures subside inthe fourth decade in juvenile myoclonic epilepsy. Neurology2008;70:2123–2129.19.
5. Camfield CS, Camfield PR. Adult outcome childhood onset, causeunknown (cryptogenic) MRI-negative, focal epilepsy. In Arts W,Arzimanoglou A, Brouwer OF, Camfield C, Camfield P (Eds)Progress in epileptic disorders; Vol 12: outcome of childhoodepilepsies. Montrouge, France: John Libbey Eurotext, 2013:173–179.6.
6. Wirrell EC, Camfield CS, Camfield PR, et al. Long-term prognosis oftypical childhood absence epilepsy. Neurology 1996;47:912–918.13.
7. Trinka E, Baumgartner S, Unterberger I, et al. Long-term prognosisfor childhood and juvenile absence epilepsy. J Neurol 2004.
8. Caplan R, Siddarth P, Stahl L, et al. Childhood absence epilepsy: behavioral, cognitive, and linguistic comorbidities. Epilepsia 2008;19:1838–1846. 15.
9. Tirado Requero P., Alba Jiménez M. Epilepsia en la infancia y la adolescencia. Pediatría Integral Vol. XIX, nº 9. Noviembre 2015.
10. Transition issues for benign epilepsy with centrotemporal spikes, nonlesional focal epilepsy in otherwise normal children, childhood absence epilepsy, and juvenile myoclonic epilepsy. Camfield CS1, Berg A, Stephani U, Wirrell EC. Epilepsia. 2014 Aug;55 Suppl 3:16-20. doi: 10.1111/epi.12706.
11. Bouma PA, Bovenkerk AC, Westendorp RG, et al. The course of benign partial epilepsy of childhood with centrotemporal spikes: ameta-analysis. Neurology 1997;48:430–437.2.
12. Camfield CS, Camfield PR. Rolandic epilepsy has little effect on adultlife 30 years later: a population-based study. Neurology 2014;82:1162–1169.3.
13. Wirrell EC, Grossardt BR, So EL, et al. A population-based study oflong-term outcomes of cryptogenic focal epilepsy in childhood:cryptogenic epilepsy is probably not symptomatic epilepsy. Epilepsia2011;52:738–745.
14. Berg AT, Testa FM, Levy SR. Complete remission in nonsyndromicchildhood-onset epilepsy. Ann Neurol 2011;70:566–573.5.
15. Wirrell EC, Camfield CS, Camfield PR, et al. Long-term psychosocialoutcome in typical absence epilepsy. Sometimes a wolf in sheeps’clothing. Arch Pediatr Adolesc Med 1997;151:152–158.8.
16. Camfield CS, Camfield PR. Juvenile myoclonic epilepsy 25 yearsafter seizure onset: a population-based study. Neurology2009;73:1041–1045.9.
17. Fastenau PS, Johnson CS, Perkins SM, et al. Neuropsychologicalstatus at seizure onset in children: risk factors for yearly cognitivedeficits. Neurology 2009;18:526–534.10.
18. Speechley KN, Ferro MA, Camfield CS, et al. Quality of life inchildren with new-onset epilepsy. Neurology 2012;79:1548–1555.11.
19. The Challenge of Pharmacotherapy in Children and Adolescents with Epilepsy-ADHD Comorbidity.Verrotti A1, Moavero R2,3, Panzarino G1, Di Paolantonio C1, Rizzo R4, Curatolo P5. Clin Drug Investig. 2018 Jan;38(1):1-8. doi: 10.1007/s40261-017-0585-1.
20. Psychiatric and Behavioural Disorders in Children with Epilepsy (ILAE Task Force Report): Adverse cognitive and behavioural effects of antiepileptic drugs in children.Aldenkamp A1, Besag F2, Gobbi G3, Caplan R4, Dunn DW5, Sillanpää M6. Epileptic Disord. 2016 May 16. [Epub ahead of print]
21. Adolescent and caregiver experiences with epilepsy. Asato MR1, Manjunath R, Sheth RD, Phelps SJ, Wheless JW, Hovinga CA, Pina-Garza JE, Haskins LS, Zingaro WM. J Child Neurol. 2009 May;24(5):562-71. doi: 10.1177/0883073809332396.
22. Symptoms of anxiety and depression and family’s quality of life in children and adolescents with epilepsy. Cianchetti C1, Bianchi E2, Guerrini R3, Baglietto MG4, Briguglio M5, Cappelletti S6, Casellato S7, Crichiutti G8, Lualdi R9, Margari L10, Romeo A11, Beghi E2; TASCA Study Group. Epilepsy Behav. 2017 Dec 28;79:146-153. doi: 10.1016/j.yebeh.2017.11.030. [Epub ahead of print]