Urgencias médicas en la adolescencia
M.J. Martín Díaz. Pediatra de la Sección de Urgencias del Hospital Infantil Universitario Niño Jesús de Madrid.
Adolescere 2021; IX (2): 116-127
Resumen
|
Los adolescentes que consultan en los servicios de urgencias a menudo suponen un reto para los pediatras o médicos de otras especialidades que los atienden. Pueden presentar patologías frecuentes también en edades pediátricas más tempranas, pero con características más cercanas al adulto, como la cefalea. En otras ocasiones el pediatra de urgencias se enfrenta a entidades casi exclusivas del adolescente y el adulto, como las infecciones de transmisión sexual. También hay cuadros cuyo abordaje es similar en todas las edades, pero presentan diferencias importantes entre los niños y los adolescentes: las intoxicaciones por ejemplo, que en los adolescentes suelen ser intencionadas y los fármacos y las drogas de abuso suelen ser los tóxicos implicados, cuando en los niños suelen ser accidentales y producidas por otro tipo de tóxicos.
Palabras clave: Urgencias; Cefalea; Dolor; Infección; Transmisión sexual; Tóxicos; Benzodiacepinas; Intoxicación; Sobredosis.
|
Abstract
|
Adolescents visiting the emergency department often pose a challenge to pediatricians or physicians from other specialties who care for them. They can present pathologies frequently found in younger pediatric ages, but with manifestations closer to those of adults, such as headache. On other occasions, the emergency pediatrician faces entities that are almost exclusive to adolescents and adults, such as sexually transmitted infections. There are also conditions whose approach is similar in all ages, but they present important differences between children and adolescents: poisonings, for example, which in adolescents are usually intentional where medications and drugs of abuse are usually the toxins involved, whereas in children they are usually accidental and produced by other types of toxins.
Key words: Emergencies; Headache; Pain; Infection; Sexual transmission; Toxic; Benzodiazepines; Intoxication; Overdose.
|
Cefalea
La cefalea es un motivo de consulta frecuente en los servicios de urgencias pediátricos. La mayoría de las veces es de origen benigno, bien por cuadros primarios como la migraña, o por procesos agudos benignos como las infecciones virales
La cefalea es un motivo de consulta frecuente en los servicios de urgencias pediátricos. La mayoría de las veces es de origen benigno, bien por cuadros primarios como la migraña, o por procesos agudos benignos como las infecciones virales. Aun así, es frecuente que tengan una repercusión importante en la calidad de vida y la funcionalidad del paciente y supongan una preocupación de los padres por la causa del dolor, sobre todo si piensan en la posibilidad de un tumor intracraneal. Por ello es importante un cuidadoso abordaje.
El dolor de cabeza suele ser un síntoma asociado a otros en los pacientes que consultan en urgencias: fiebre, dolor de garganta, vómitos, dolor de cuello, etc. El objetivo principal es no pasar por alto los casos secundarios a una patología intracraneal importante, que precisen tratamiento temprano para no poner en peligro la vida del paciente: fundamentalmente procesos que pueden causar hipertensión intracraneal (tumores intracraneales, meningitis, patología vascular o abscesos cerebrales). Esto puede ser difícil, sobre todo teniendo en cuenta la limitación de tiempo que se tiene en urgencias y el ambiente de tensión. Por otro lado, en los casos que se diagnostican de cefalea primaria, es importante llegar a un tratamiento efectivo para acabar con los síntomas, así como evitar ingresos innecesarios en los casos que no son graves. Una historia clínica y una exploración física detalladas y cuidadosas son los elementos básicos para cumplir este objetivo.
El objetivo principal es no pasar por alto los casos secundarios a una patología intracraneal importante
Una historia clínica y una exploración física detalladas y cuidadosas son los elementos básicos para cumplir este objetivo
Como siempre, en la atención de un paciente que consulta en urgencias, comenzaremos con la evaluación de su estabilidad: triángulo de evaluación pediátrica, ABCD y constantes vitales (con especial atención en la temperatura y la tensión arterial) con las medidas terapéuticas necesarias. Una vez estabilizado, continuamos con la historia clínica detallada. El patrón temporal de la cefalea es una buena guía para realizar el diagnóstico diferencial (Tabla I): cefalea aguda; cefalea aguda recurrente o episódica; cefalea crónica progresiva; cefalea crónica no progresiva.
Aunque siempre hay que tener presente la posibilidad de un proceso subyacente, el segundo y el cuarto grupo normalmente son debidos a cefaleas primarias. La cefalea crónica progresiva es la más preocupante y suele precisar la realización de pruebas de neuroimagen. Los episodios aislados y cortos de cefalea aguda suelen estar desencadenados por procesos benignos (migraña e infecciones virales los más frecuentes), aunque hay procesos graves que pueden producir cefalea aguda, normalmente intensa.
Además del patrón temporal, es fundamental caracterizar bien el episodio para llegar a una aproximación diagnóstica (Tabla II). A continuación se realizará la exploración física, con el objetivo principal de identificar signos que indiquen organicidad (Tabla III).
Además del patrón temporal, es fundamental caracterizar bien el episodio para llegar a una aproximación diagnóstica
Los estudios publicados en la literatura acerca de la etiología de la cefalea en niños y adolescentes, encuentran que todos los casos de cefalea debida a una patología importante, tienen alteraciones neurológicas en la historia o la exploración física. Sin embargo hay que tener en cuenta que las patologías que causan hipertensión intracraneal (HTIC) pueden producir síntomas intermitentes en las primeras fases, por lo que una única exploración neurológica normal no las excluye, y es importante un buen seguimiento y reevaluación de los pacientes.
La mayoría de los pacientes con procesos intracraneales importantes presentan alteraciones en la exploración neurológica
La cefalea aguda es un único episodio en un paciente que no ha tenido otros previos. La mayoría de los casos de cefalea aguda no traumática son consecuencia de procesos autolimitados que pueden ser tratados sintomáticamente, como infecciones de vías respiratorias altas o sinusitis. La fiebre causa dolor de cabeza, pero también procesos intracraneales importantes (meningitis, encefalitis, abscesos intracraneales) pueden producir dolor de cabeza y fiebre, por lo que es importante evaluar el estado mental y los signos meníngeos en los pacientes que presentan estos dos síntomas. Como ya se ha mencionado, la mayoría de los pacientes con procesos intracraneales importantes presentan alteraciones en la exploración neurológica, siendo las más frecuentes: alteración de la consciencia, rigidez de nuca, alteración de los movimientos oculares, ataxia, papiledema, hemiparesia. En estos casos es prioritario realizar una prueba de neuroimagen con carácter urgente. Hay que tener en cuenta la patología vascular dentro de las patologías intracraneales con riesgo vital. De especial importancia es reconocer los procesos isquémicos lo antes posible para que puedan recibir tratamiento en el período crítico si son candidatos a ello. Los síntomas más frecuentes en los accidentes isquémicos son: debilidad focal de extremidades, debilidad facial y alteraciones del habla. La mayoría de los pacientes presentan un nivel de consciencia normal o levemente alterado (Glasgow 14 o 15) y focalidad en la exploración neurológica. El dolor de cabeza, así como los vómitos y la alteración del nivel de consciencia son más frecuentes en los accidentes vasculares cerebrales hemorrágicos. La cefalea de inicio brusco que se refiere como “la cefalea peor de su vida”, o en “trueno”, especialmente si ha sido desencadenada por esfuerzos, debe alertar sobre la posibilidad de una hemorragia subaracnoidea.
La cefalea de inicio brusco que se refiere como “la cefalea peor de su vida”, o en “trueno”, especialmente si ha sido desencadenada por esfuerzos, debe alertar sobre la posibilidad de una hemorragia subaracnoidea
La cefalea aguda recurrente son episodios repetidos de cefalea, con las mismas características, separados por intervalos libres de síntomas. La cefalea tensional y la migraña (con o sin aura) son los más frecuentes. El dolor de la migraña es típicamente unilateral, pulsátil, de intensidad moderada o grave, empeora con la actividad física y se acompaña de náuseas y/o foto y sonofobia. Las crisis de migraña pueden acompañarse de síntomas autonómicos (enrojecimiento, sudoración, palidez, visión borrosa, mareo, dolor epigástrico) y de alodinia cutánea. La migraña con aura se caracteriza por síntomas neurológicos focales transitorios, que aparecen antes o junto con el dolor de cabeza.
La cefalea crónica no progresiva se define por la presencia de 4 horas de dolor en al menos 15 días al mes, durante más de 4 meses consecutivos. Los dolores de cabeza diarios son muchas veces discapacitantes y son un reto diagnóstico. Los casos de aparición reciente, con cambios en el patrón de la cefalea o con alteraciones neurológicas deben hacer pensar en una patología seria subyacente. En los casos primarios hay que centrarse en evitar los desencadenantes y encontrar medicación de mantenimiento para evitar o minimizar los brotes. Muchos casos que no responden al tratamiento se deben a una sobredosificación de analgésicos; en estos casos hay que interrumpir estos, pautar un tratamiento de transición para controlar el dolor, y buscar una buena pauta como profilaxis a largo plazo. La depresión y la ansiedad pueden ser la causa de los casos de cefalea crónica no progresiva.
La cefalea crónica progresiva son episodios de cefalea recurrentes con un incremento progresivo de la frecuencia y la intensidad del dolor. Hay que sospechar una patología preocupante subyacente cuando el paciente presenta: dolor de predominio nocturno o matutino que va empeorando; dolor que lo despierta por la noche; cambios de comportamiento o vómitos a primera hora de la mañana; alteraciones en la exploración neurológica.
Hay que sospechar una patología preocupante subya-cente cuando el paciente presenta: dolor de predominio nocturno o matutino que va empeorando; dolor que lo despierta por la noche; cambios de comportamiento o vómitos a primera hora de la mañana; alteraciones en la exploración neurológica
Los pacientes que necesitan ampliar el estudio con pruebas complementarias son una minoría. La actuación debe ir guiada por la sospecha diagnóstica
Los pacientes que necesitan ampliar el estudio con pruebas complementarias son una minoría. La actuación debe ir guiada por la sospecha diagnóstica. Aunque las guías y consensos existentes establecen signos de alarma (ver Tabla IV), no establecen reglas de decisión diagnóstica. De hecho, varios estudios demuestran que algunos de los signos de alarma son inespecíficos y conducen a realizar pruebas de imagen a pacientes que no las precisan (en especial el dolor que despierta por la noche, el dolor a primera hora de la mañana o el dolor que va aumentando en frecuencia, duración e intensidad). La tomografía computerizada (TC) craneal es la prueba disponible generalmente en urgencias, pero expone al paciente a una dosis de radiación importante. La resonancia magnética (RM) es una técnica más precisa, pero también más cara y en la edad pediátrica, sobre todo por debajo de los 6 años, requiere con frecuencia sedación profunda.
Las pruebas analíticas suelen tener poca utilidad en la evaluación de un paciente con cefalea. Podrían estar indicadas en función de la sospecha diagnóstica:
- Análisis de sangre: cuando se sospeche una infección, disfunción tiroidea, enfermedad celíaca, anemia, ferropenia, enfermedades autoinmunes;
- Punción lumbar: si se sospecha infección del sistema nervioso central (en ausencia de signos de HTIC), HTIC idiopática, o hemorragia subaracnoidea;
- Si en la exploración física se detecta hipertensión arterial, se realizará una bioquímica sérica con función renal e iones, electrocardiograma y análisis de orina;
- Si hay sospecha de intoxicación: carboxihemoglobina, plomo en sangre, despistaje de tóxicos en orina, dependiendo del contexto;
- Derivación a consultas para estudio de sueño si hay datos de apnea obstructiva del sueño.
El tratamiento dependerá del diagnóstico: si se sospecha una cefalea secundaria, el tratamiento debe ser etiológico. En los pacientes estables salvo por el dolor, con sospecha de cefalea primaria, la primera medida a tomar es llevar al paciente a un lugar oscuro, silencioso y cómodo. Si están en un lugar donde pueden dormir, hay que intentar que lo hagan, porque el sueño suele terminar con el episodio.
Hay varias medidas ambientales que pueden aconsejarse: sueño suficiente y apropiado; dieta sana en horarios ordenados; actividad física ni excesiva ni escasa; considerar técnicas de relajación; identificar y evitar los desencadenantes.
El objetivo del tratamiento analgésico farmacológico es hacer desaparecer el dolor, lo cual ayuda o consigue mitigar los síntomas acompañantes (náuseas, vómitos, foto y sonofobia). La mayoría de los fármacos son más eficaces si se aplican cuando el dolor es leve, casi siempre al inicio del episodio. En los casos en que los vómitos impiden la administración oral de analgésicos habrá que valorar la vía intravenosa en el servicio de urgencias. Los fármacos a utilizar de primera elección son el paracetamol (10-15 mg/kg/dosis) y el ibuprofeno (10 mg/kg/dosis). Con frecuencia el paciente ha recibido ya alguno de estos analgésicos cuando consulta en urgencias, por lo que es importante comprobar la dosis administrada y la frecuencia. Cuando no han sido efectivos se pueden utilizar otros analgésicos (metamizol, naproxeno, etc.), aunque tienen mecanismos de acción similares a los anteriores y es probable que tampoco sean efectivos. El sumatriptán está aprobado para el tratamiento de la migraña a partir de los 12 años de edad; la vía oral es igual de eficaz que la intranasal pero mejor tolerada. Los pacientes con migrañas prolongadas o en estatus migrañoso pueden requerir la atención en urgencias. Los antagonistas de los receptores de dopamina (clorpromazina, metoclopramida), pueden ser una opción terapéutica en este grupo, pues pueden eliminar tanto el dolor como las náuseas y los vómitos, aunque hay que tener en cuenta que pueden producir reacciones extrapiramidales y sedación como efectos secundarios.
El sumatriptán está aprobado para el tratamiento de la migraña a partir de los 12 años de edad; la vía oral es igual de eficaz que la intranasal pero mejor tolerada
Los opioides están contraindicados en la cefalea primaria, porque podrían empeorar la fisiopatología del proceso. Actualmente no se consideran una línea de tratamiento de la cefalea en niños y se ha encontrado asociación entre su uso y un mayor tiempo de hospitalización en pacientes pediátricos con cefalea.
Infecciones de transmisión sexual en adolescentes
El desarrollo psicosocial de los adolescentes normalmente implica un deseo de autonomía que conlleva una tendencia a adoptar conductas de riesgo. Por ello son una población especialmente expuesta a las infecciones de transmisión sexual (ITS)
El desarrollo psicosocial de los adolescentes normalmente implica un deseo de autonomía que conlleva una tendencia a adoptar conductas de riesgo. Por ello son una población especialmente expuesta a las infecciones de transmisión sexual (ITS). La edad media del comienzo de las relaciones sexuales coitales está en torno a los 16 años en EE.UU., pero hay poblaciones en las que se adelanta incluso varios años. En la adolescencia tardía se completa la transición a la edad adulta y aumenta la actividad sexual; es la edad donde se está más expuesto a las ITS. Se estima que un 50% de los casos de ITS ocurren en adolescentes y jóvenes de menos de 24 años. Además, la reinfección es frecuente: hasta un 40% de los casos de ITS son en pacientes que han tenido otras previas. A su vez, esto es un factor de riesgo para adquirir la infección por el virus de la inmunodeficiencia humana (VIH).
Se estima que un 50% de los casos de ITS ocurren en adolescentes y jóvenes de menos de 24 años
Las ITS son asintomáticas muchas veces, lo cual hace plantearse si sería rentable realizar screening en pacientes de riesgo
Las ITS son asintomáticas muchas veces, lo cual hace plantearse si sería rentable realizar screening en pacientes de riesgo. Los médicos de urgencias participan en estas labores mucho menos que los médicos de otros ámbitos: la falta de tiempo, de seguimiento del paciente, de un buen ambiente para dar consejos, son barreras que dificultan la búsqueda de estas enfermedades en los servicios de urgencias. Pero por otro lado es frecuente que los adolescentes no consulten con el médico de atención primaria y en su lugar busquen atención médica en urgencias. Además, a partir de los 14 años no hay programadas visitas de control del paciente sano en atención primaria, lo que dificulta las labores preventivas y de detección precoz. Los adolescentes que consultan en urgencias son pacientes con más conductas de riesgo que los que lo hacen en atención primaria. Es decir, las urgencias son un ámbito en el que hay que tener un alto índice de sospecha de las ITS en los pacientes adolescentes.
Es importante conocer los factores de riesgo de adquisición de ITS, porque así será más fácil detectar los casos:
- Factores comportamentales: edad de la primera relación sexual (en el primer año después de la primera relación sexual ya suele darse la primera ITS); actividad sexual en la adolescencia temprana y media (sobre todo para la infección por C. trachomatis); múltiples parejas, parejas nuevas, o parejas que tienen múltiples parejas; sexo con varones en varones o mujeres transgénero; uso inconstante del condón; consumo de alcohol u otras drogas (aunque este factor de riesgo puede ser un factor de confusión asociado a un uso inadecuado de los condones y a tener múltiples parejas); enemas o duchas anales antes de realizar el coito rectal.
- Factores biológicos: la inmadurez del epitelio del ectocérvix, que cambia de columnar a escamoso en el proceso de madurez sexual hace más proclives a estas infecciones a las mujeres adolescentes; la microbiota cervical y vaginal, que cambia con la madurez y también con la primera relación sexual.
- Otros factores de riesgo son: vivir en centros institucionales, haber sido víctima de abusos en la infancia (maltrato o abuso sexual), trastornos del ánimo (predisponen al abuso de sustancias ilegales).
Aunque el diagnóstico y el tratamiento de las ITS en adolescentes es igual que en adultos, hay aspectos que merecen un trato especial: confidencialidad, violencia, embarazo y grupos minoritarios
Aunque el diagnóstico y el tratamiento de las ITS en adolescentes es igual que en adultos, hay aspectos que merecen un trato especial en estos pacientes:
- Confidencialidad. Es fundamental recoger de forma adecuada la historia sexual del paciente que consulta con una posible ITS. Para ello hay que asegurar la confidencialidad, hacer preguntas directas, sin juicios de valor, limitándose a dar consejos acerca de la prevención de estas patologías.
- Embarazo. En ocasiones, la preocupación acerca de un posible embarazo es lo que hace consultar por una posible ITS y al contrario.
- Grupos minoritarios. Homosexuales, bisexuales, transgénero.
- Violencia. Aunque las conductas violentas en las parejas son un problema evidente, es muy raro que los adolescentes lo consulten con los médicos. Es importante detectar signos de violencia en la valoración médica.
El espéculo y la exploración pélvica bimanual en mujeres pueden causar incomodidad y dolor y no son necesarios
Además, hay que realizar una exploración física y pruebas complementarias dirigidas por la sospecha diagnóstica:
- Exploración física. Debe ser completa, porque alguna de estas infecciones tiene manifestaciones extragenitales que pueden ser la pista diagnóstica. De especial importancia es la exploración genital y ano/ rectal en busca de lesiones propias de la infección por el virus herpes, la sífilis o el virus papiloma humano (VPH). El espéculo y la exploración pélvica bimanual en mujeres pueden causar incomodidad y dolor y no son necesarios. Se recomienda limitarlos a los siguientes casos: dolor abdominal y/o pélvico, obtención de muestras para detección microbiológica (aunque la orina y el exudado vaginal suelen ser válidos, y las adolescentes los prefieren generalmente), alteraciones menstruales asociadas (amenorrea no provocada por gestación, sangrado uterino anormal), sospecha de cuerpo extraño vaginal.
Aparte de la cuestión discutible de cuándo realizar detección precoz en los casos asintomáticos o paucisintomáticos, debemos tener presentes los motivos de consulta que deben hacer descartar una ITS. Se pueden agrupar en patrones de signos y síntomas que pueden guiar la sospecha diagnóstica:
Las características de la secreción son poco fiables para sospechar una etiología concreta
- Secreción uretral o vaginal y disuria. Son característicos de las siguientes infecciones: gonorrea, infecciones por Chlamydia, Trichomonas, vaginosis bacteriana, candidiasis. En adolescentes y adultos jóvenes se ven cada vez más casos de secreción genital debida a ITS por Mycobacterimun genitalium. El virus herpes simple (VHS) puede causar disuria y secreción uretral mucosa, pero casi siempre asociadas a lesiones genitales. Las características de la secreción son poco fiables para sospechar una etiología concreta.
La infección genital ulcerosa se puede ver en el VHS, sífilis primaria, en el contexto de infecciones sistémicas virales (p. ej. virus Epstein Barr), de enfermedad de Chrönh, vasculitis o el síndrome de Bechet
- Infección genital ulcerosa. Las características clínicas de las infecciones que se manifiestan así son superponibles y además hasta un 10% de los casos tienen coinfección, lo cual hace muy difícil el diagnóstico clínico. El VHS es la causa más frecuente en adolescentes (el tipo 2 es más frecuente pero el tipo 1 causa un porcentaje importante). La sífilis primaria es otra causa a tener en cuenta ante úlceras genitales, sobre todo en varones que practican sexo con otros varones, en los que tienen contacto con la prostitución y en los consumidores de metanfetamina y cocaína. Las úlceras genitales no siempre están producidas por ITS; pueden ocurrir en el contexto de infecciones sistémicas virales (p. ej. virus Epstein Barr), de enfermedad de Chrönh, vasculitis, el síndrome de Bechet.
La enfermedad inflamatoria pélvica, es una secuela relativamente frecuente de la gonorrea y la infección por Chlamydia
- Enfermedad inflamatoria pélvica. Engloba las entidades que producen una infección del aparato genital interno femenino, cuyas manifestaciones pueden ser diversas y por ello es difícil de diagnosticar. Hay que sospecharla en adolescentes sexualmente activas que se quejan de molestias persistentes en la zona pélvica, aunque hay muchos casos paucisintomáticos. Es una secuela relativamente frecuente de la gonorrea y la infección por Chlamydia.
- Síndromes dermatológicos. El más común son las verrugas anogenitales del condiloma acuminado (virus del papiloma humano: VPH). Hay otras ITS que pueden cursar con exantemas cutáneos: la sífilis secundaria; la infección gonocócica diseminada; la pediculosis pubis y la escabiosis. De especial interés es la sífilis secundaria, que cursa con manifestaciones cutáneas fundamentalmente: exantema maculopapular eritematoso generalizado (afecta palmas y plantas), lesiones mucocutáneas, adenopatías.
- Manifestaciones orales. El chancro de la sífilis primaria suele ser genital, pero puede aparecer en los labios, la lengua y las amígdalas. Los condilomas de la sífilis secundaria son placas extensas, blancogrisáceas, erosivas, que afectan a áreas húmedas como la mucosa oral o el periné. La sífilis secundaria en adolescentes es rara, afectando sobre todo a los grupos de mayor riesgo, como los que participan en el sexo comercial y los consumidores de metanfetamina y cocaína; implica que no se ha tratado el chancro primario. La faringitis gonorreica se adquiere normalmente por la práctica de sexo oral. Suele ser asintomática, aunque puede cursar con dolor de garganta, exudado amigdalar y linfadenopatía cervical.
En general, en urgencias se buscan las ITS en pacientes sintomáticos. Tras completar la historia y la exploración, hay que tomar siempre muestras para realizar el diagnóstico microbiológico. Las pruebas diagnósticas de las principales ITS son:
La amplificación del DNA por PCR, o el cultivo viral (menos sensible), son las técnicas de elección para diagnosticar la infección por virus herpes simple (es importante hacerlo para diferenciar entre el tipo 1 y el tipo 2)
- La amplificación del DNA por PCR, o el cultivo viral (menos sensible), son las técnicas de elección para diagnosticar la infección por virus herpes simple (es importante hacerlo para diferenciar entre el tipo 1 y el tipo 2).
- La infección urogenital por Chlamydia en mujeres puede diagnosticarse recogiendo la primera orina de la mañana o un frotis cervical o vaginal (se prefiere el frotis, recogido por personal médico o por la propia paciente). En varones, con la primera orina de la mañana (de elección) o un frotis uretral. Las pruebas más sensibles, de elección, son las pruebas de amplificación de ácidos nucleicos.
- El diagnóstico de la infección por Neisseria gonorrhoeae también debe hacerse por técnicas de amplificación de ácidos nucleicos, en secreciones cervicales/ vaginales o uretrales en varones, o en la primera orina de la mañana.
Los test serológicos siguen siendo los métodos de elección, siendo los más conocidos los test treponémicos y no treponémicos
- La sífilis es una enfermedad sistémica provocada por la infección por Treponema pallidum. Se divide en 3 etapas en función de sus manifestaciones clínicas: sífilis primaria (úlceras o chancro en el lugar de infección), sífilis secundaria (manifestaciones cutáneas) y sífilis terciaria (manifestaciones cardiacas, neurológicas, lesiones gomatosas). La detección directa del treponema en la fase primaria sería diagnóstica, pero no hay pruebas comerciales disponibles. Se utilizan para su diagnóstico las pruebas serológicas: pruebas no treponémicas (VDRL, RPR), y pruebas treponémicas (FTA-ABS, TP-PA, encimoinmunoensayos, quemoluminiscencia, inmunoblots). Se requiere la positividad de una prueba no treponémica y una treponémica para su diagnóstico (en la primera fase de la enfermedad podría haber falsos negativos con una sola prueba treponémica negativa, y puede haber falsos positivos solo con una prueba no treponémica positiva). En una persona con una prueba no treponémica positiva hay que confirmarlo con una prueba treponémica. Si esta es negativa, hay que realizar de nuevo una prueba no treponémica, con un antígeno diferente a la primera. Si la prueba es positiva, hay que tratar (excepto en los casos que tengan historia de sífilis tratada).
Las técnicas de amplificación de ácidos nucleicos y los cultivos dan un diagnóstico diferido, por lo que el médico de urgencias debe intentar hacer un diagnóstico sindrómico y en función de ello, indicar un tratamiento empírico. Debe enviarse a los pacientes a la consulta especializada en ITS de referencia, para asegurar que se completa su evaluación si no ha podido hacerse en urgencias y planificar su seguimiento. Está indicado realizar despistaje de las ITS más importantes (VIH, sífilis, gonorrea, Chlamydia) en los pacientes con cualquier infección urogenital de transmisión sexual, por el alto riesgo de coinfección.
Está indicado realizar despistaje de las ITS más importantes (VIH, sífilis, gonorrea, Chlamydia) en los pacientes con cualquier infección urogenital de transmisión sexual, por el alto riesgo de coinfección
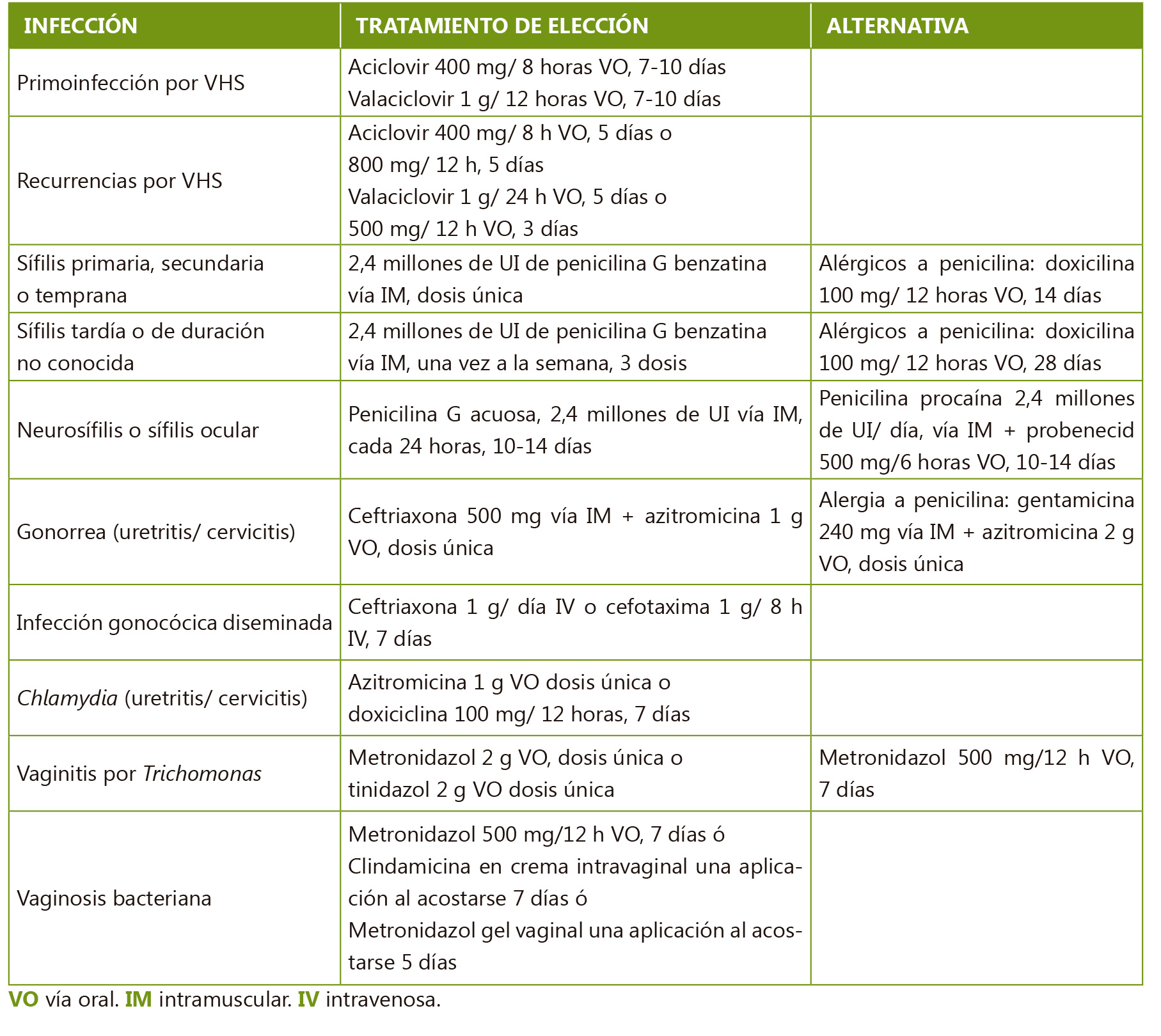
Los protocolos de tratamiento de las ITS en adolescentes se derivan de los estudios realizados con adolescentes y adultos jóvenes (pocos estudios incluyen pacientes menores de 16 años, y en general se dispone de pocos datos con pacientes menores de 18 años). Se resumen en la Tabla V.
Los adolescentes deben ser aconsejados adecuadamente sobre las prácticas de sexo seguro. Debe recomendarse abstinencia sexual hasta que se conozcan los resultados de las pruebas diagnósticas, aunque se haya realizado tratamiento empírico. Si se confirma alguna de estas infecciones (salvo VIH), debe tratarse también la pareja y no deben tener relaciones con coito hasta que ambos completen el tratamiento. En la infección por Chlamydia y por gonococo, está indicado realizar una prueba diagnóstica 3 meses después del tratamiento pues aunque hay un alto índice de erradicación tras el tratamiento, es frecuente la reinfección. Las parejas de los 60 días previos deben ser evaluadas y tratadas. Hay que evitar el coito hasta 7 días después de completado el tratamiento del paciente y la pareja para evitar la reinfección.
Intoxicación por fármacos
La atención de un paciente intoxicado debe ser sistemática y protocolizada. La historia clínica y la exploración física son los pilares de la evaluación del paciente
Los analgésicos son los fármacos más frecuentemente implicados en la intoxicación, pero las benzodiacepinas, los antidepresivos y los antipsicóticos tienen un papel importante
Los adolescentes que toman una cantidad tóxica de medicamentos de forma intencionada se ven con frecuencia en urgencias en los países occidentales. La mayoría tienen una patología psiquiátrica subyacente. Los analgésicos son los fármacos más frecuentemente implicados, pero las benzodiacepinas, los antidepresivos y los antipsicóticos tienen un papel importante.
La atención de un paciente intoxicado debe ser sistemática y protocolizada. Los síntomas y los hallazgos clínicos pueden ser muy diversos, dependiendo del tóxico ingerido, el tiempo que ha transcurrido desde la ingesta, la medicación de base que pueda tomar el paciente y si la ingesta ha sido de un solo tóxico o de varios. La historia clínica y la exploración física son los pilares de la evaluación del paciente. El tratamiento se basa en: la estabilización inicial, la disminución de la absorción del tóxico y en casos concretos, el uso de antídotos y técnicas para acelerar la eliminación del tóxico.
La evaluación inicial comienza con una historia clínica y una exploración básicas, incluyendo la evaluación y estabilización del ABCD. En la anamnesis hay que preguntar lo que ha sucedido y cuándo, los síntomas, las patologías concomitantes y los medicamentos que el paciente toma de forma crónica, la última vez que comió y si tiene alguna alergia; además hay que averiguar los fármacos accesibles al paciente y comprobar cuántos faltan, incluyendo drogas de abuso, fármacos fuera de prescripción médica, productos de herbolario y suplementos dietéticos. Lo referido por el paciente debe intentarse corroborar por la familia o cuidadores. Es importante también recoger adecuadamente la información de los servicios de emergencias si son los que han traído al paciente a urgencias.
En la exploración física la evaluación de los signos vitales, el estado mental y el tamaño y reacción pupilar son los signos más útiles. Hay que tomar las constantes vitales: temperatura, frecuencia cardíaca, frecuencia respiratoria, tensión arterial, saturación de oxígeno y glucemia. Se recomienda pulsioximetría continua y monitorización electrocardiográfica hasta que se compruebe la estabilidad del paciente. Debe realizarse un ECG en todos los pacientes expuestos a drogas potencialmente cardiotóxicas o si hay duda de ello. Hay que desnudar al paciente para completar la exploración y detectar signos de traumatismo, autolesiones, infección, etc.
Una historia fiable que revela qué tóxico ha sido el ingerido simplifica el manejo del paciente
Una historia fiable que revela qué tóxico ha sido el ingerido simplifica el manejo del paciente. Para intentar confirmar el diagnóstico se utilizan los inmunoensayos para detectar drogas de abuso en orina, que son rentables por su bajo coste y su rapidez. En todo caso, el resultado no descarta ni confirma rotundamente el diagnóstico: puede haber falsos negativos porque el tóxico no alcanza la concentración necesaria para su detección, por realizarse la prueba antes o después del pico de concentración; puede haber falsos positivos por reacciones cruzadas (p. ej. la difenhidramina puede dar positivo para antidepresivos tricíclicos); también puede encontrarse una sustancia que se consumió días antes y no es la responsable de la intoxicación.
En cuanto a otras pruebas complementarias, deben ir guiadas por el tóxico implicado. En los pacientes sintomáticos con una historia inconsistente o desconocida, debe realizarse al menos: análisis de orina, glucosa, urea, creatinina e iones. En los pacientes graves es recomendable: osmolaridad plasmática, cetonemia, creatín kinasa, pruebas de función hepática, calcio iónico, magnesio, lipasa. En mujeres en edad fértil es recomendable realizar prueba de embarazo. En los casos de intoxicación intencionada en que no pueda excluirse la ingesta de paracetamol hay que solicitar niveles.
El manejo óptimo del paciente depende del tóxico implicado, la gravedad de los síntomas presentes y la que se espera y el tiempo transcurrido desde la ingesta. El tratamiento debe ser de soporte, realizando si procede descontaminación intestinal, administración de antídotos y técnicas para acelerar la eliminación del tóxico.
El carbón activado es el método de descontaminación recomendado actualmente en la mayoría de los casos de intoxicación por fármacos
El carbón activado es el método de descontaminación recomendado actualmente en la mayoría de los casos. Beneficia al paciente sobre todo si el tóxico está todavía en el estómago (se considera que en la primera hora tras la ingesta, aunque no puede excluirse su eficacia si se administra más tarde). No debe utilizarse en ciertas situaciones:
- Alteración del nivel de consciencia sin protección de la vía aérea (por el riesgo de aspiración). La administración del carbón no debe ser nunca la única indicación para intubar a un paciente.
- Presentación tardía (es muy probable que el tóxico no esté en el estómago).
- Riesgo de aspiración y de aumentar su gravedad por la administración del carbón (por ejemplo, ingesta de hidrocarburos).
- Necesidad de realizar una endoscopia (por ejemplo, ingesta de cáusticos).
- Tóxicos que no se adsorben al carbón activado: metales como el hierro y el litio, alcoholes, álcalis, hidrocarburos, corrosivos (ácidos o álcalis), aceites esenciales.
- Obstrucción intestinal (contraindicación absoluta) o probable disminución del peristaltismo (contraindicación relativa).
Los antídotos están indicados cuando: existe antídoto para el tóxico implicado, la gravedad del caso precisa su uso, los beneficios terapéuticos esperados superan los riesgos y no hay contraindicaciones. En las intoxicaciones por varias drogas es más fácil que el uso de antídotos sea perjudicial.
En las intoxicaciones por varias drogas, es más fácil que el uso de antídotos sea perjudicial
Las técnicas para potenciar la eliminación del tóxico (forzar la diuresis, atrapamiento iónico en orina, hemodiálisis, hemofiltración, hemoperfusión y recambio transfusional) están indicadas en casos seleccionados.
Después de la evaluación y estabilización inicial, el tratamiento y un período breve de observación, se decidirá la ubicación del paciente, en función de la gravedad de los síntomas presentados y esperados. Los pacientes con manifestaciones leves pueden permanecer en observación en urgencias unas horas, hasta comprobarse su estabilidad y ser dados de alta. Los demás casos deben ingresar para realizar una monitorización adecuada (en la Unidad de Cuidados Intensivos en los casos más graves). Todos los pacientes con intoxicación intencionada deben ser valorados por el psiquiatra antes de ser dados de alta.
Intoxicación por benzodiacepinas
Las benzodiacepinas son fármacos sedantes, hipnóticos, relajantes musculares y anticonvulsivantes que se utilizan desde la década de 1960. Actúan modulando la acción de los receptores A del ácido gamma aminobutírico (GABA). El aumento de la incidencia de los casos de intoxicación por estos fármacos, a menudo voluntaria en pacientes adolescentes y adultos, refleja el uso creciente de estos medicamentos.
Las benzodiacepinas ingeridas vía oral en sobredosis sin otro tóxico acompañante, raramente causan toxicidad importante
Las benzodiacepinas ingeridas vía oral en sobredosis sin otro tóxico acompañante, raramente causan toxicidad importante. La presentación típica es depresión del sistema nervioso central (SNC) con signos y constantes vitales normales. Los pacientes sintomáticos suelen presentar un habla torpe, ataxia y alteración del nivel de consciencia. Muchos pacientes pueden despertarse y se les puede hacer una historia del episodio detallada. Los pacientes con toxicidad grave pueden presentarse estuporosos o comatosos. La depresión respiratoria es muy rara; se presenta si se han consumido otros depresores del SNC como alcohol o los opiodes (esto es más típico de adultos que de adolescentes), y en los casos en que se administran varias dosis de benzodiacepinas en procedimientos médicos que requieren sedación (casi siempre vía intravenosa, propiciando un aumento rápido de su concentración en el SNC). Las dosis con riesgo de producir depresión respiratoria son difíciles de concretar, pues dependen de muchos factores (tolerancia, edad, peso, coingestiones, genética).
Las pruebas de detección de tóxicos en orina no detectan las benzodiacepinas en sí, sino alguno de sus metabolitos. Los metabolitos urinarios pueden ser detectados desde 3 horas después de la ingesta y permanecen detectables hasta 2 semanas después
Las pruebas de detección de tóxicos en orina no detectan las benzodiacepinas en sí, sino alguno de sus metabolitos, por ello hay alguna que puede dar falsos negativos: clonazepam, alprazolam, midazolam, lorazepam. La cantidad de droga ingerida, la coingesta de otras drogas y el peso del paciente pueden alterar la farmacocinética y también la prueba de detección en orina. En general, los metabolitos urinarios pueden ser detectados desde 3 horas después de la ingesta y permanecen detectables hasta 2 semanas después.
El flumazenil es el antídoto de las benzodiacepinas: es un antagonista no competitivo del receptor que bloquea estos fármacos
El flumazenil es el antídoto de las benzodiacepinas: es un antagonista no competitivo del receptor que bloquea estos fármacos. Cuando surgió el flumazenil, se creía que no tenía ninguna actividad intrínseca y se utilizaba no solo para revertir la sedación por sobredosis de benzodiacepinas, sino también como herramienta diagnóstica en los pacientes en coma de causa desconocida en los servicios de urgencias. Sin embargo, su uso durante años ha demostrado efectos adversos importantes como arritmias y convulsiones (puede precipitar convulsiones por abstinencia en personas con uso crónico de benzodiacepinas que han desarrollado tolerancia; también si ha habido coingesta de drogas proconvulsivantes). Actualmente su uso está casi relegado al tratamiento de las complicaciones por el uso iatrogénico de benzodiacepinas en procedimientos de sedación. En niños la dosis inicial es 0,01 mg/ kg administrada vía IV en 15-30 segundos (máximo 0,2 mg, que es la dosis de adulto). Puede repetirse la dosis (o la mitad de dosis) a intervalos de 1-3 minutos hasta 4 veces. La dosis total no debe superar 1 mg (o 0,05 mg/kg). El efecto del flumacenil es muy corto (de 0,7 a 1,3 horas); el efecto de las benzodiacepinas de vida media larga o una dosis alta pueden superar su duración de acción y puede reaparecer la sedación. Podría repetirse hasta 3 veces la pauta anterior, sin superar la administración de 3 mg en una hora.
Los pacientes con depresión respiratoria o que han ingerido otras drogas potencialmente graves pueden requerir ingreso en la unidad de cuidados intensivos. La mayoría de los pacientes con ingesta únicamente de benzodiacepinas están asintomáticos después de un período de observación de 4-6 horas y pueden ser valorados por psiquiatría. Hay que asegurar que el paciente tiene una marcha normal antes de ser dado de alta. Si después de 6 horas continúa con síntomas de intoxicación, habrá que continuar la monitorización hasta la completa resolución de la clínica.
Tablas y figuras
Tabla I. Causas de la cefalea según el patrón temporal
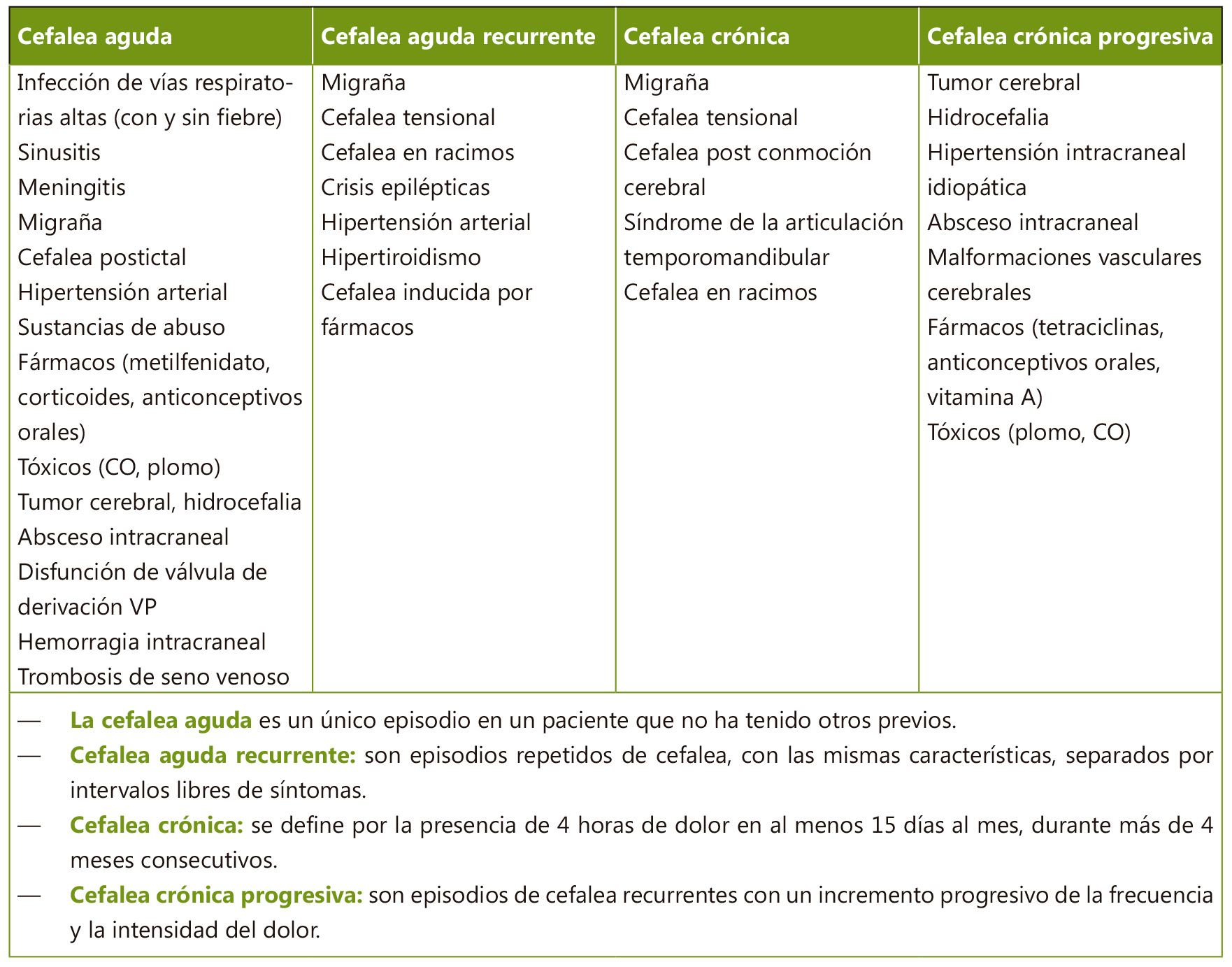
Tabla II. ¿Qué hay que preguntar para caracterizar bien el dolor de cabeza?

Tabla III.
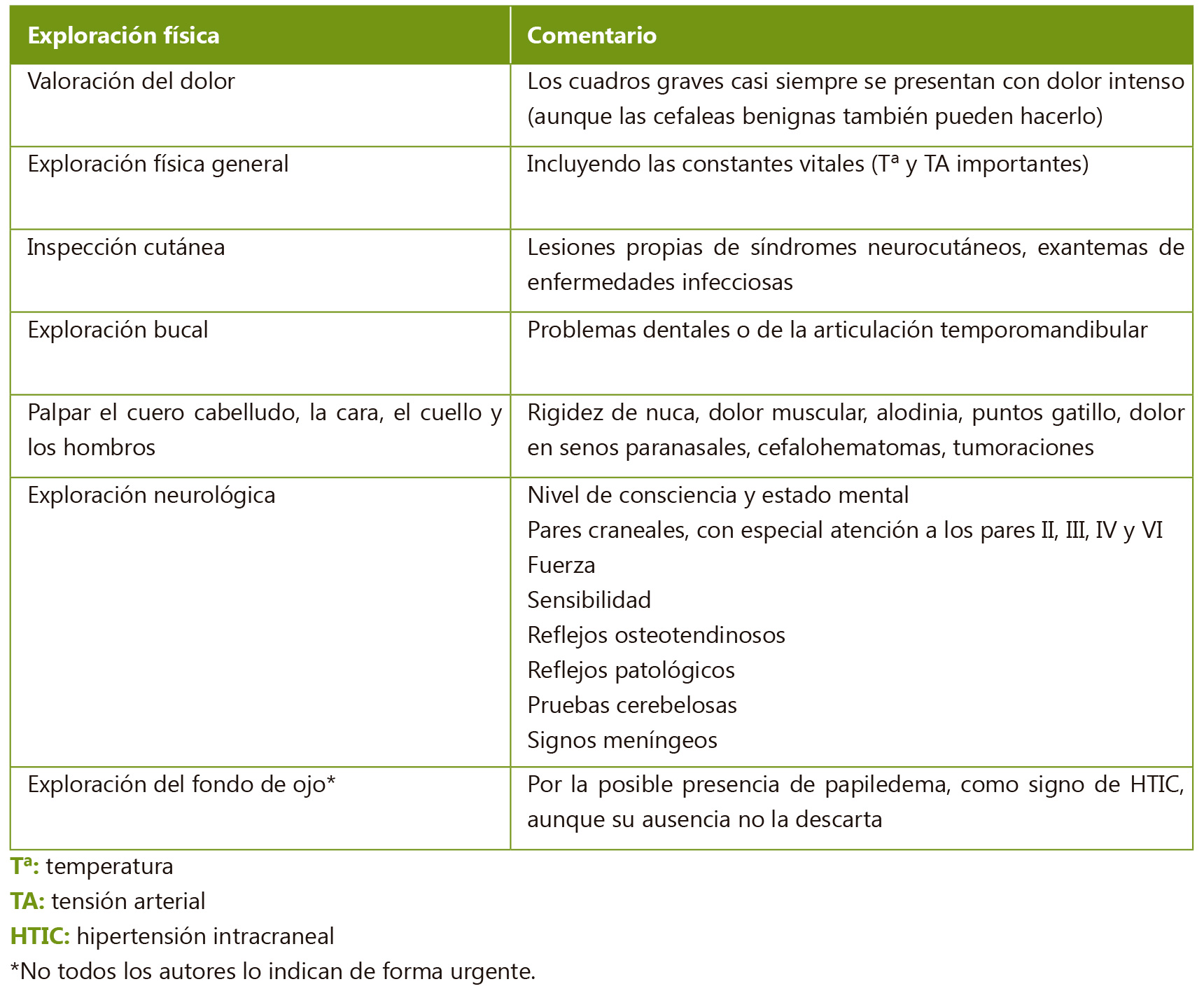
Tabla IV.

Tabla V.
Bibliografía
- Raucci U, Della Vecchia N, Ossella C, Paolino MC, Villa MP, Reale A, Parisi P. Management of Childhood Headache in the Emergency Department. Review of the Literature. Front Neurol. 2019 Aug 23;10:886. doi: 10.3389/fneur.2019.00886. eCollection 2019.
- Papetti L, Capuano A, Tarantino S, Vigevano F, Valeriani M. Headache as an Emergency in Children and Adolescents. Curr Pain Headache Rep. 2015 Mar;19(3):3. doi: 10.1007/s11916-015-0480-5.
- Dao JM, Qubty W. Headache Diagnosis in Children and Adolescents. Curr Pain Headache Rep. 2018 Feb 23;22(3):17. doi: 10.1007/s11916-018-0675-7.
- Schobitz E, Qureshi F, Lewis D. Pediatric Headaches in the Emergency Department. Curr Pain Headache Rep. 2006 Oct;10(5):391-6.
- Blume HK. Childhood Headache: A Brief Review. Pediatr Ann. 2017;46(4):e155-e165.
- Hilbert SM, Reno HEL. Management of Patients with Sexually Transmitted Infections in the Emergency Department. Emerg Med Clin N Am 36 (2018) 767–776.
- Wangu Z, Burstein GR. Adolescent Sexuality: Updates to the Sexually Transmitted Infection Guidelines. Pediatr Clin N Am 64 (2017) 389–411.
- Bonar EE, Walton MA, Caldwell MT, Whiteside LK, Barry KL, Cunningham RM. Sexually Transmitted Infection History among Adolescents Presenting to the Emergency Department. J Emerg Med. 2015 November ; 49(5): 613–622.
- Workowski KA, Bolan GA; Centers for Disease Control and Prevention. Sexually Transmitted diseases treatment guidelines, 2015. MMWR Recomm Rep. 2015 Jun 5;64(RR-03):1-137.
- Lowry JA, Burns M, Calello DP. Pediatric Pharmaceutical Ingestions. Pediatr Ann. 2017 Dec 1;46(12):e459-e465.
- Fadum EA, Stanley B, Qin P, Diep LM, Mehlum L. Self-poisoning with medications in adolescents: a national register study of hospital admissions and readmissions. Gen Hosp Psychiatry. 2014 Nov-Dec;36(6):709-15.
- Penninga EI, Graudal N, Ladekarl MB, Jürgens G. Adverse Events Associated with Flumazenil Treatment for the Management of Suspected Benzodiazepine Intoxication – A Systematic Review with Meta-Analyses of Randomised Trials. Basic Clin Pharmacol Toxicol. 2016 Jan;118(1):37-44.
- Mangus CW, Canares TL. Toxic Ingestions: Initial Management. Pediatr Rev. 2018 Apr;39(4):219-221. doi: 10.1542/pir.2017-0119.














