Sesión I Actualización: El adolescente cansado. Caso clínico: Adolescente con astenia/cansancio y abdominalgia
Sesión I Actualización: El adolescente cansado.
Caso clínico: Adolescente con astenia/cansancio y abdominalgia
Í. de Noriega(1), R. Martino Alba(2), B. Herrero Velasco(3)
(1)Pediatra-Unidad de Atención Integral Paliativa Pediátrica. HIU Niño Jesús, Madrid. (2)Jefe de Sección-Unidad de Atención Integral Paliativa Pediátrica. HIU Niño Jesús, Madrid. Doctor en Medicina, Universidad Autónoma de Madrid (UAM). (3)Pediatra-Servicio de Hematología y Oncología. HIU Niño Jesús Madrid. Doctora en Medicina, Universidad Autónoma de Madrid (UAM).
Adolescere 2023; XI (2): 18-24
Resumen
|
La astenia en la adolescencia es un síntoma frecuente e inespecífico, en el que no siempre es posible llegar a un diagnóstico etiológico. Para el pediatra es importante conocer los signos de alarma que deben implicar la realización de pruebas complementarias de cara a llegar a un diagnóstico de certeza. Su manejo en el paciente con enfermedad grave presenta una importancia capital al ser un limitante importante para actividades que puede querer realizar el paciente. Se presenta el caso clínico de un adolescente con astenia y distintos signos a lo largo de su evolución que finalmente llevan al diagnóstico de una enfermedad grave.. Palabras clave: Medicina del Adolescente; Astenia; Fatiga. |
Abstract
|
Asthenia in adolescence is a frequent and non-specific symptom, and it is not always possible to reach an etiological diagnosis. It is important for the pediatrician to know the warning signs that should imply the performance of complementary tests in order to reach a diagnosis of certainty. Its management in patients with severe disease is of paramount importance as it is an important limiting factor for activities that the patient may wish to carry out. We present the clinical case of an adolescent with asthenia and different signs throughout his progress that finally lead to the diagnosis of a severe disease. Key words: Adolescent Medicine; Asthenia; Fatigue. |
Introducción
Jorge es un paciente de 14 años, que recibe seguimiento habitual por su pediatra de atención primaria. Como antecedentes de interés presenta alergia estacional a pólenes y trastorno por déficit de atención e hiperactividad (TDAH). Recibe tratamiento con metilfenidato, así como dexclorfeniramina oral y budesónida nasal en las épocas en las que presenta síntomas alérgicos.
En una consulta telefónica, su madre refiere que han avisado desde el colegio porque en las últimas semanas presta menos atención, está más distraído y con una gran tendencia al sueño. La madre, que se había mostrada reacia en otras ocasiones a mantener el metilfenidato, relaciona estos síntomas con una reciente subida de dosis pautada por su neurólogo. La madre le pregunta que si puede volver a la dosis anterior y si se puede solicitar un análisis de sangre para comprobar que “está todo bien”,
¿cuál sería su actitud?
La astenia puede definirse como una “sensación de cansancio intensa, debilitante y mantenida en el tiempo que limita la capacidad para realizar actividades de la vía diaria incluyendo actividades laborales”
La astenia constituye un síntoma de consulta frecuente en pediatría. La Real Academia de la Lengua la define como “debilidad o fatiga general que dificulta o impide a una persona realizar tareas que en condiciones normales hace fácilmente”. Desde un punto de vista médico, podría definirse de manera más precisa como una “sensación de cansancio intensa, debilitante y mantenida en el tiempo que limita la capacidad para realizar actividades de la vía diaria incluyendo actividades laborales”(1).
Algunos estudios han estimado que hasta un 30 % de los pacientes adolescentes pueden referir astenia(2). En su abordaje como síntoma, el pediatra debe tener en consideración varios aspectos.
En primer lugar, la astenia rara vez es descrita como tal por los pacientes o sus padres, empleándose más frecuentemente los términos “cansado”, “débil” o “fatigado”. Estos términos pueden enmascarar diferentes problemas médicos, desde astenia propiamente dicha hasta disnea o náuseas.
Una vez excluidos otros síntomas, la sensación de astenia puede referirse a tres escenarios distintos fundamentalmente que pueden estar o no relacionados entre sí:
- Sensación de debilidad física y somnolencia.
- Cambios emocionales como falta de motivación, síntomas depresivos o labilidad.
- Cansancio mental, con falta de concentración y pérdida de memoria u otros síntomas cognitivos.
La presencia de astenia como tal debe alertarnos cuando la sensación de cansancio a) no se alivie con el reposo b) no sea proporcional al grado de actividad del paciente c) sea una fuente de preocupación para el propio paciente
Como cualquier síntoma, su vivencia tiene un fuerte componente individual y depende en gran medida de la interferencia que suponga para el día a día del paciente. En este sentido es importante contar con la perspectiva, su perspectiva particular, dado que por mucho que terceras personas refieran cansancio, debe ser él mismo el que describa, no sólo la presencia sino también la intensidad y la repercusión que el síntoma tiene en su vida. La presencia de astenia como tal debe alertarnos cuando la sensación de cansancio a) no se alivie con el reposo b) no sea proporcional al grado de actividad del paciente c) sea una fuente de preocupación para el propio paciente.
La astenia como síntoma, ya sea en su presentación aislada o en presencia de otros síntomas puede formar parte de una miríada de problemas, síndromes y enfermedades(3). La mayoría van a corresponderse con problemas leves y fácilmente identificables por el pediatra tras una correcta anamnesis y exploración física. Sin embargo, algunas enfermedades y problemas graves pueden presentar la astenia como único síntoma en sus primeras fases. Por lo tanto, es necesario realizar un abordaje estricto, excluyendo potenciales causas graves y realizando un seguimiento temporal estrecho en caso de no identificar una etiología clara.
Abordaje inicial en el paciente adolescente con astenia
Por su naturaleza inespecífica, existen pocas recomendaciones sobre el abordaje de la astenia en pediatría. Inicialmente debe realizarse con una correcta anamnesis y exploración física. Se debe realizar una caracterización lo más precisa posible de lo que el paciente refiere como astenia para distinguirla de otros síntomas como alteraciones anímicas, disnea, cansancio muscular, etc. En el paciente adolescente, debe realizarse una entrevista con preguntas lo más abiertas posible en el que se dé la misma relevancia a los aspectos físicos que a los psicológicos y sociales(2). Algunos aspectos importantes que considerar en la población adolescente son:
En el paciente adolescente, debe realizarse una entrevista con preguntas lo más abiertas posible en el que se dé la misma relevancia a los aspectos físicos que a los psicológicos y sociales
- Presencia de otros síntomas, especialmente de síntomas de afectación sistémica.
- Valoración del patrón de sueño: muy relevante, teniendo en cuenta el alto porcentaje de adolescentes con alteraciones del sueño(2). Debe recabarse información sobre horas insuficiente de sueño acordes a la edad, presencia de insomnio, presencia de signos sugestivos de síndrome de apnea/hipopnea del sueño, etc.
- Valoración del estado de ánimo incluyendo presencia de estresores en distintos ámbitos (escolar, familiar, amigos…), cambios recientes, etc.
- Aumento de la actividad física habitual: preguntando por un posible aumento de la intensidad/frecuencia de la actividad, especialmente en pacientes con actividad física intensa.
- Valoración del patrón nutricional habitual, con valoración de la dieta habitual del paciente que debe contar con una cantidad y composición adecuada de nutrientes tanto a lo largo del día como a lo largo del tiempo.
- Excluir la posibilidad de consumo de tóxicos (alcohol, cannabis…).
- En mujeres, valorar el patrón menstrual, identificando aquellas con presencia sangrado excesivo. También se debe considerar la posibilidad de embarazo.
Si no se identifica una causa clara, se debe considerar la evolución temporal del cuadro o su asociación a procesos intercurrentes. El número de problemas clínicos que pueden subyacer tras el síntoma de astenia es prácticamente inabarcable, por lo que en aquellos pacientes que presenten una astenia llamativa sin causa clara, en experiencia de los autores, se recomienda buscar específicamente como síntomas de alarma, otros síntomas sistémicos genéricos como pérdida de peso, anorexia o febrícula/fiebre mantenida de cara a establecer la posible gravedad inicial del cuadro, signos o síntomas por aparatos y sistemas que permitan un abordaje diagnóstico dirigido y valorar la repercusión global que tiene la astenia en la vida diaria del paciente. Estos síntomas pueden no estar presentes inicialmente, por lo que puede que los pacientes requieran seguimiento a lo largo del tiempo. En ausencia de otros síntomas y en el caso de mantenerse en el tiempo, debe considerarse también el diagnóstico de síndrome de fatiga crónica o fibromialgia, siendo este un diagnóstico de exclusión que requiere previamente haber descartado otras causas(4).
La exploración física debe de ser completa, prestando atención a los siguientes aspectos:
- Toma de constantes: incluyendo tensión arterial (con cambios ortostáticos), frecuencia cardiaca y valoración antropométrica en el contexto de las curvas de crecimiento del paciente y glucemia capilar.
- Exploración cardiopulmonar: incluyendo auscultación y valoración de pulsos periféricos.
- Exploración cutáneo-mucosa: presencia de palidez (anemia), hiperpigmentación (enfermedad de Addison) u otros estigmas sugestivos de enfermedad sistémica (exantemas en lupus eritematoso, dermatomiositis…). Debe realizarse una búsqueda activa de adenias patológicas en todos los grupos ganglionares accesibles a la exploración.
- Exploración abdominal: debe descartarse la presencia de hepatoesplenomegalia o de masas pélvicas.
- Exploración osteoarticular: incluyendo valoración de eventual inflamación de articulaciones o presencia de dolor óseo.
- Exploración neurológica: incluyendo a ser posible fondo de ojo y prestando atención a la valoración de la fuerza y de la marcha.
En el caso que nos corresponde, antes de realizar cambios en la medicación o solicitar pruebas complementarias es necesario realizar una entrevista con el paciente que nos permita analizar todos los aspectos mencionados y contar con su propia visión sobre el problema clínico referido.
Le indica a la madre de Jorge que es conveniente solicitar una cita presencial para hablar con él y poder orientar mejor el diagnóstico y la actitud a seguir. Acude a consulta Jorge con su madre, explicando que, efectivamente se encuentra más cansado, con menos fuerza y con limitación física para realizar actividades que antes hacía a lo largo del día. No nota sensación de dificultad respiratoria ni otros síntomas actualmente. Refiere que el proceso empezó con lo que creyeron que era un catarro leve hace un mes por el que tuvo fiebre de hasta 39º y dolor de garganta durante 2-3 días que luego desapareció. Desde entonces nota sólo que sigue teniendo dolor de tripa en el lado izquierdo con algunos movimientos y algo de mucosidad, por lo que él empezó a tomar dexclorfeniramina, pensando que era su alergia. De hecho, como otras veces esta medicación le había dado bastante sueño, él le echo la culpa (no al metilfenidato como sugería su madre) y dejó de tomarlo, a pesar de lo cual, le parece que el cansancio va cada vez a más.
En la exploración física se observa un buen estado general, con buena hidratación y con buena coloración de piel y mucosas. Auscultación cardiopulmonar normal. Abdomen blando y depresible, dolor en flanco izquierdo donde se palpa esplenomegalia con borde de polo inferior a unos tres traveses de parrilla costal. Sin hepatomegalia. Orofaringe con leve hipertrofia amigdalar sin exudación.
Jorge nos explica que está preocupado porque el cansancio está empezando a interferir con las actividades básicas de su vida diaria. No puede realizar los entrenamientos con su equipo de fútbol, ni estudiar adecuadamente para los exámenes. ¿Cuál sería su actitud?
En este caso, la anamnesis y la exploración física nos aportan información adicional imprescindible para el correcto abordaje del paciente. Al interrogar al propio paciente el foco se desplaza del ajuste de medicación para su TDAH al antecedente de un cuadro infeccioso reciente. Los síntomas que presenta el paciente, con el antecedente de un cuadro de probable infección faríngea, la astenia persistente y la presencia de esplenomegalia en la exploración plantean la presencia de un cuadro de mononucleosis infecciosa como primera opción, causa frecuente de astenia en población adolescente en nuestro medio, pudiendo tener un curso sintomatológico bifásico en la presentación de sus síntomas(5). Además, es cierto que el empleo de antihistamínicos puede producir cierto grado de somnolencia. Sin embargo, esta debería haber desaparecido al suspenderla y, en cualquier caso, se observa una repercusión importante y en aumento en la actividad diaria del paciente.
Si bien el diagnóstico de la mononucleosis infecciosa es eminentemente clínico, en nuestro caso, la gravedad de los síntomas aconseja realizar el diagnóstico de confirmación con las pruebas de laboratorio, así como excluir otras causas posibles.
Tras la exploración se acuerda solicitar un análisis de sangre y ecografía abdominal. Recibe los resultados del análisis de sangre a los 7 días, donde se observa un hemograma con leucocitosis a expensas de linfocitosis moderada, función hepática con leve elevación de transaminasas y resto de parámetros bioquímicos sin alteración, TSH normal, inmunoglobulinas normales, leve elevación de reactantes de fase aguda con resultado positivo en IgM y negativo en IgG de virus de Epstein-Barr. La ecografía está pendiente de cita. Realiza una consulta telefónica con la madre de Jorge que refiere que se mantiene más cansado. Continúa presentando dolor abdominal que en este caso refiere al centro del abdomen, sin otros síntomas digestivos, salvo sensación nauseosa, asociando además picos de febrícula de predominio nocturno de hasta 37,8º. Acuerdan darle una nueva cita presencial para control.
En la consulta llama la atención la presencia de palidez cutánea, además de aumento de la esplenomegalia preexistente hasta situarse a cinco traveses de dedo y dolor difuso a la palpación abdominal sin otros hallazgos. Se decide derivar a urgencias al paciente para descartar malignidad. En urgencias se realiza análisis de sangre que muestra anemia junto con LDH de 2219 UI/L y PCR de 7,2 mg/dL como principales hallazgos. Ante la sospecha de patología maligna se realiza ecografía abdominal con hallazgo de esplenomegalia y varios adenopatías abdominales de gran tamaño.
Jorge ingresa, confirmándose el diagnóstico de linfoma de Burkitt e inicia tratamiento con quimioterapia según protocolo. ¿Cómo abordaría la astenia de aquí en adelante?
La presencia de astenia progresiva y mantenida en el tiempo, asociando otros signos de malignidad (la palidez y la esplenomegalia progresiva), deben llevar siempre a descartar una patología oncológica
La presencia de astenia progresiva y mantenida en el tiempo, asociando otros signos de malignidad (en este caso la palidez y la esplenomegalia progresiva), deben llevar siempre a descartar una patología oncológica como origen de los síntomas. Estas manifestaciones no aparecen siempre en el momento inicial y pueden solaparse con distintos procesos intercurrentes, incluyendo otros que produzcan astenia, dada su alta frecuencia, y confundir el diagnóstico.
Astenia en el paciente con enfermedad grave
En los pacientes con enfermedades graves, la astenia es un síntoma frecuente e inhabilitante. Ha sido descrita con una frecuencia de hasta el 50 % en pacientes con cáncer en distintos estadios evolutivos(6–8). En otras enfermedades graves, la frecuencia de la astenia parece que puede situarse entre el 70 y el 96 %(1,8). En el periodo de final de vida, la astenia ha sido descrita como el síntoma más frecuente, alcanzando a más del 90 % de los pacientes.
En aquellos pacientes en los que la astenia suponga un síntoma importante, debe realizarse un abordaje específico, incluyendo la búsqueda de distintas etiologías, la graduación del síntoma y la planificación de posibles estrategias terapéuticas a seguir.
Abordaje diagnóstico integral del paciente que refiere astenia
En el diagnóstico inicial es importante considerar todos aquellos factores que puedan estar jugando un papel en la presencia de la astenia. Se ha propuesto que la astenia forma parte de una agrupación de síntomas (síntomas “cluster”) en el que varios problemas clínicos acaban produciendo un único síntoma(9). De ahí que sea importante realizar una valoración integral del paciente, analizando de manera conjunta todos los problemas físicos y las alteraciones en otras esferas.
- Esfera física: debe considerarse, en primer lugar, si la propia enfermedad puede jugar un papel en el desarrollo de la astenia, dado que en ese caso la evolución del síntoma puede ir en paralelo a la de la misma y depender de la posibilidad de contar con un tratamiento etiológico o no. También debe tenerse en cuenta la posible relación de los tratamientos que reciba el paciente con la astenia (corticoides, quimioterapia…). El abordaje diagnóstico debe incluir todos aquellos aspectos que se han considerado en el paciente pediátrico general, teniendo en cuenta las particularidades según la enfermedad. Así, por ejemplo, los pacientes con enfermedades neuromusculares pueden presentar con frecuencia síndrome de apnea/hipopnea del sueño que puede producir astenia, en los pacientes con cáncer, la anemia puede aparecer secundariamente a la anemia, etc.
- Otras esferas: especialmente importante es distinguir la presencia de alteraciones anímicas, como síntomas depresivos que se solapen con los problemas físicos. A este respecto, se debe tener en cuenta que los pacientes con astenia suelen presentar deseo de realizar actividades que se ve alterado por la presencia del síntoma, mientras que, en los pacientes con sintomatología depresiva, el paciente puede presentar un grado variable de abulia.
En pacientes con enfermedad grave se debe valorar la afectación de las áreas sociales y espirituales (aislamiento debido a la enfermedad, dificultad para la interacción por pares), tanto como causantes de malestar para el paciente como en la repercusión que la astenia tenga sobre estos aspectos.
La valoración de la astenia, de manera similar a la del dolor debe incluir la graduación de su gravedad mediante escalas
La valoración de la astenia, de manera similar a la del dolor debe incluir la graduación de su gravedad, de manera que se pueda intentar realizar un seguimiento adecuado de las intervenciones posibles que se realizan. En población adulta se han empleado varias escalas(9). En pediatría, se han propuesto distintas escalas, como el módulo de astenia de la escala PedsQLTM o el módulo para astenia de la escala “Memorial symptom assessment scale” (MSAS) dentro del estudio PediQUEST(10,11).
Tratamiento de la astenia
El abordaje terapéutico de la astenia debe realizarse idealmente con un abordaje interdisciplinar y a varios niveles
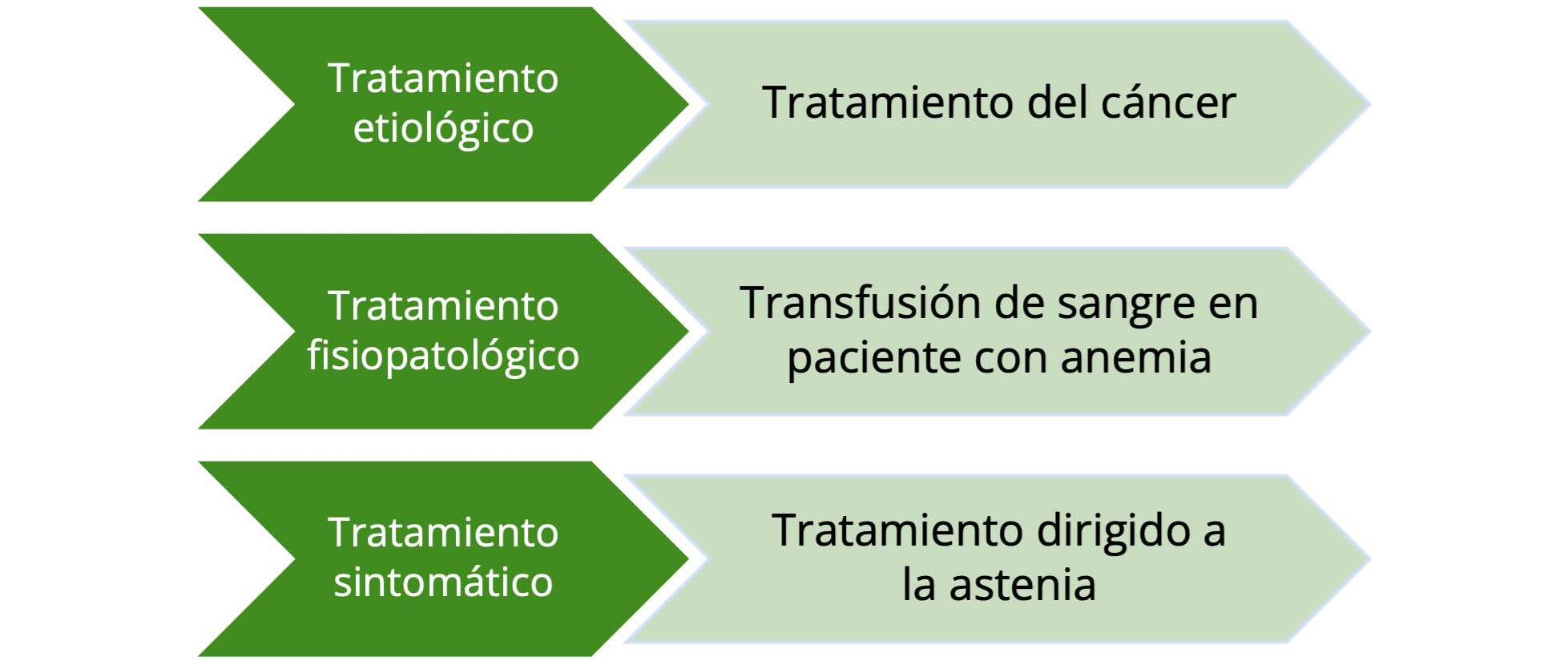
El abordaje terapéutico de la astenia debe realizarse idealmente con un abordaje interdisciplinar y a varios niveles. Para ello se debe establecer un diagnóstico claro de la situación que permita identificar las distintas posibilidades terapéuticas. Así, por ejemplo, en un paciente con patología oncológica que presente astenia se debe valorar si la astenia se debe al propio cáncer, en cuyo caso, el tratamiento definitivo pasaría por el tratamiento contra la enfermedad (tratamiento etiológico), si se debe a la presencia de anemia, en cuyo caso estaría indicada la administración de transfusiones de sangre (tratamiento fisiopatológico) o si este no es posible, si se decide abordar con tratamientos farmacológicos o medidas no farmacológicas (tratamiento sintomático; Figura 1).
Sobre este último punto, a pesar de su alta prevalencia en pacientes con enfermedades graves, la astenia es uno de los síntomas con una menor evidencia en su manejo terapéutico. Las intervenciones que cuentan con un mayor grado de evidencia son las no farmacológicas(1). En primer lugar, deben intentar corregirse aquellos aspectos que puedan contribuir a la falta de actividad física como el decondicionamiento físico. Para ello, se puede recurrir a actividad física aeróbica leve-moderada adaptada a cada paciente (andar, bicicleta estática…). Deben incorporarse estrategias como la terapia de grupo o terapia cognitiva no sólo como prevención de alteraciones emocionales, sino también centradas en el manejo cognitivo de la propia disnea.
En los tratamientos farmacológicos, la evidencia es escasa y la aplicación de distintas modalidades derivan de datos extraídos de adultos o de población sana(1). Se ha propuesto el metilfenidato en dosis similares a las empleadas para el TDAH como medicación estimulante. El modafinilo, estimulante empleado en la narcolepsia también podría constituir una alternativa. Los corticoides pueden revertir parcialmente la astenia, si bien asocian efectos secundarios importantes(9). También se ha propuesto que el déficit de carnitina podría jugar un papel en la astenia. No obstante, ante el bajo nivel de evidencia de los datos disponibles, se recomienda realizar un abordaje que prime las medidas no farmacológicas desde un abordaje preventivo.
Jorge inicia tratamiento con distintos ciclos de quimioterapia. Se incorpora al programa de actividad física de su hospital, siendo una actividad que le motiva. Debido a la quimioterapia, presenta una aplasia con anemia secundaria, por el que requiere transfusiones con las que se observa mejoría importante de su astenia. Recibe además seguimiento por parte de psicología, donde se facilitan pautas de adaptación a su situación clínica, dado que para Jorge pasar tanto tiempo ingresado es frustrante.
A lo largo de su evolución presenta dos recaídas refractarias al tratamiento. Se acuerda inicio de atención domiciliaria por parte del equipo de atención paliativa tras informar al paciente y a su familia.
En la primera entrevista Jorge pregunta por la posibilidad de mantener transfusiones de hematíes para mantenerse “lo más activo posible”. Presenta además un dolor óseo de difícil control que ha requerido de inicio de fentanilo transdérmico con rescates sublingual que actualmente no está bien controlado, ¿está indicado mantener las transfusiones?
En el periodo de final de vida de una enfermedad letal se suele acompañar de una importante astenia progresiva que no va a ser siempre posible tratar
Finalmente, en aquellos pacientes que fallecerán a causa de su enfermedad, debe señalarse que el periodo de final de vida de una enfermedad letal se suele acompañar de una importante astenia progresiva que no va a ser siempre posible tratar. Debe explicarse esto tanto al paciente adolescente como a sus padres de cara a evitar intervenciones innecesarias (controles de sangre, transfusiones, tratamientos…) como para que puedan anticipar todas aquellas actividades que sean importantes para ellos a nivel social o espiritual.
En nuestro caso, se debe explicar que las transfusiones paliarían parcialmente la astenia que se deba a la anemia, pero no la debida a la evolución progresiva de la enfermedad. Además, las transfusiones pueden prolongar la vida de Jorge en la etapa de final de vida donde pueden presentarse síntomas graves que produzcan sufrimiento al paciente. Se debe explicar esto al paciente y realizar una adecuación dinámica de medidas: mientras tratar la astenia y/o prolongar la vida del paciente sirva al bien superior de Jorge, facilitando actividades importantes para él, estará indicado mantenerlas. En el momento en el que la astenia se deba mayoritariamente a la enfermedad, sin obtener mejoría a las transfusiones y estas dejen de servir a su bien, estará indicado su retirada para permitir la muerte natural del paciente(12).
Tablas y figuras
Figura 1. Abordaje en varios niveles del tratamiento de la astenia como síntoma
Fuente: Elaboración propia.
Bibliografía
1. Bogetz J, Hauer J. 23. Neurological and neuromuscular conditions and symtoms. Hain R, Rapoport A, Meiring M, Goldman A, editors. Oxford textbook of palliative care for children 3e. 3rd ed. New York: Oxford University Press; 2021. p. 244–54. (Oxford textbooks).
2. Findlay SM. The tired teen: A review of the assessment and management of the adolescent with sleepiness and fatigue. Paediatrics & Child Health. 2008 Jan;13(1):37–42.
3. Castellano Barca G. El adolescente cansado. Adolescere. VI(1):6–11.
4. Villa Grifol M. Fibromialgia. Fatiga crónica. Abordaje terapéutico. Implicación desde el Servicio de Salud Mental. Adolescere. 2022;X(3):53–9.
5. Martín Ruano J, Lázara Ramos J. Mononucleosis infecciosa en la infancia. Pediatr Integral. 2014;XVIII(3):141–52.
6. Wolfe J, Grier HE, Klar N, Levin SB, Ellenbogen JM, Salem-Schatz S, et al. Symptoms and Suffering at the End of Life in Children with Cancer. N Engl J Med. 2000 Feb 3;342(5):326–33.
7. de Noriega Í, García-Salido A, Martino R, Herrero B. Palliative home-based care to pediatric cancer patients: characteristics and healthcare delivered. Support Care Cancer. 2022 Jan;30(1):59–67.
8. Drake R, Frost J, Collins JJ. The symptoms of dying children. J Pain Symptom Manage. 2003 Jul;26(1):594–603.
9. San-Miguel Arregui MT, Bruera E. Evaluación multidimensional de la astenia relacionada con el cáncer. Medicina Paliativa. 2014 Jan;21(1):21–31.
10. Varni JW, Burwinkle TM, Katz ER, Meeske K, Dickinson P. The PedsQL in pediatric cancer: reliability and validity of the Pediatric Quality of Life Inventory Generic Core Scales, Multidimensional Fatigue Scale, and Cancer Module. Cancer. 2002 Apr 1;94(7):2090–106.
11. Ullrich CK, Dussel V, Orellana L, Kang TI, Rosenberg AR, Feudtner C, et al. Self-reported fatigue in children with advanced cancer: Results of the PediQUEST study. Cancer. 2018 Sep 15;124(18):3776–83.
12. de Noriega I, Martino Alba R, Herrero Velasco B. Toma de decisiones en la atención al final de la vida en pacientes adolescentes, desde el enfoque paliativo. Adolescere. X(2):76–83.