Adolescencia y vacunas
Situación actual de la gripe y la COVID-19 en la población infanto-juvenil
Situación actual de la gripe y la COVID-19 en la población infanto-juvenil
R.Ortiz de Lejarazu Leonardo, I. Sanz Muñoz.
Centro Nacional de Gripe de Valladolid
Adolescere 2024; XII (2): 136-146
Resumen
|
La aparición del virus SARs-COV-2 que provocó la pandemia del COVID ha producido cambios en los sistemas de salud de los diferentes países, culturas y economías. Por un lado, las medidas no farmacológicas (MNF) como el aislamiento social y el uso generalizado de mascarillas, evitó la circulación de otros virus respiratorios y cambios en la presencia de diferentes linajes víricos. Uno de los efectos mas destacados son los cambios en los virus de la gripe circulantes y la incidencia del VRS en lactantes. España es uno de los países mundiales que se ha sumado a la iniciativa de la recomendación de la vacunación gripal pediátrica postulada por la OMS hace ya 12 años. La recomendación en España fue hecha en primer lugar por Asociación Española de Pediatría en 2021, seguida después por la recomendación oficial desde el Ministerio de Sanidad. En la actualidad, cuatro años después, la epidemiología de los virus respiratorios va restableciéndose poco a poco. El nuevo virus SARS-COV-2 no se ha estacionalizado todavía lo que complica la estrategia vacunal. La posibilidad de coadministración de vacunas de virus respiratorios debe ayudar a mejorar las coberturas de la gripe en población infanto-juvenil. Palabras clave: Gripe; COVID; SARS-COV-2; Vacunación; Epidemiología. |
Abstract
|
The eruption of SARs-COV-2 virus that led to the COVID pandemic has produced changes in the health systems of various countries, cultures and economies. On the one hand, non-pharmacological measures (NPM) such as social isolation and the generalized use of masks prevented the circulation of other respiratory viruses and changes in the presence of different viral lineages. One of the most outstanding effects are the shifts in circulating influenza viruses and the incidence of RSV in infants. Spain is one of the countries in the world that has joined the initiative of the recommendation of pediatric influenza vaccination postulated by the WHO 12 years ago. The recommendation in Spain was first made by the Spanish Association of Pediatrics in 2021, later followed by the official recommendation from the Ministry of Health. At present, four years later, the epidemiology of respiratory viruses is gradually being restored. The new SARS-COV-2 virus has not yet been seasonalized, which complicates the vaccination strategy. The possibility of co-administration of respiratory virus vaccines should help to improve influenza coverage in children and adolescents. Key words: Influenza; COVID; SARS-COV-2; Vaccination; Epidemiology. |
Introducción
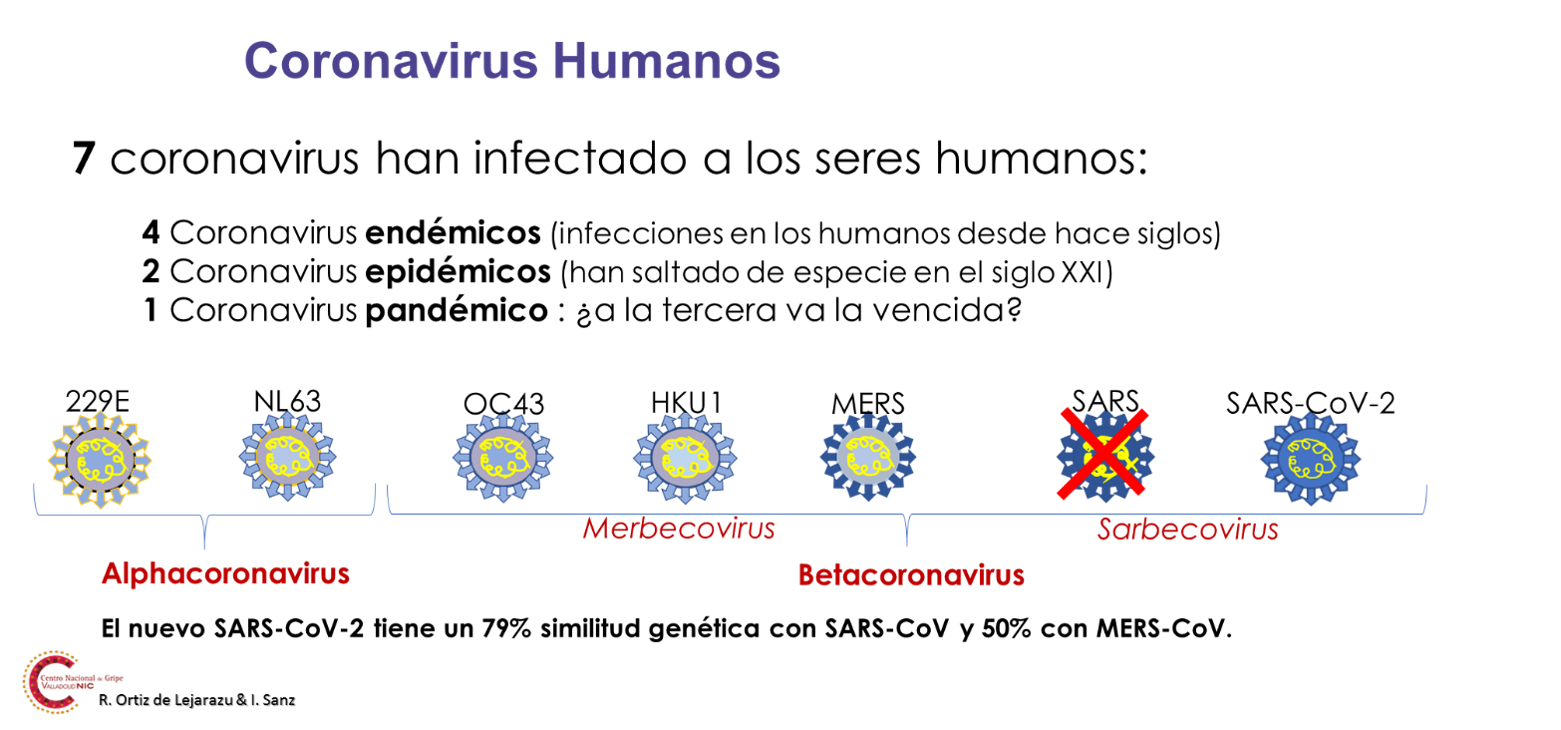
La emergencia del virus SARS-CoV-2 a finales de 2019 ha supuesto un antes y un después en la epidemiología clásica de algunos virus respiratorios de alta incidencia (Gripe, VRS)
La emergencia del virus SARS-CoV-2 a finales de 2019 ha supuesto un antes y un después en la epidemiología clásica de algunos virus respiratorios de alta incidencia (Gripe, VRS). La población pediátrica protagonista de muchas de esas viriasis respiratorias ha sufrido las consecuencias de esa alteración epidémica y ha puesto en valor alguna de las medidas recientemente aprobadas e implementadas como la recomendación de vacunar de gripe a todos los niños sanos de 6 a 59 meses o la administración de Nirsevimab a lactantes(1,2).
Tras la aparición del nuevo coronavirus humano SARS-CoV-2 y su difusión pandémica en los meses siguientes, el mundo se paró. Algunos titubeos y negaciones de la realidad sanitaria que protagonizaron algunos gobernantes chocaron en pocas semanas con la tozuda realidad y, casi todos los gobiernos de los países occidentales de recursos económicos altos, pusieron en marcha planes de contención de la pandemia ante la ausencia de tratamientos específicos o vacunas, basados en las denominadas medidas no farmacológicas (MNF).
Las medidas no farmacológicas, consiguieron además del efecto de contención sobre el nuevo virus, otros efectos colaterales nada desdeñables sobre otros virus de transmisión respiratoria
Entre las MNF que lograron modificar en parte la intensidad de la primera onda cabe destacar por su efectividad, los confinamientos masivos, algunos como el español largos y crueles para algunos colectivos poblacionales y especialmente la población pediátrica. Las restricciones de la movilidad geográfica, la prohibición de aglomeraciones y eventos multitudinarios, las restricciones en espacios públicos, el cierre de bares, colegios y universidades y el uso masivo de mascarillas en los lugares de gran afluencia pública, consiguieron además del efecto de contención sobre el nuevo virus, otros efectos colaterales nada desdeñables sobre otros virus de transmisión respiratoria(3).
Gripe: Tres temporadas atípicas y una casi típica
Una de las primeras consecuencias que ha condicionado la situación actual de la gripe fue la ausencia total de epidemia estacional en 2020-21(3), típica en el hemisferio norte en los meses invernales. Dicha temporada se caracterizó por un número muy bajo de casos de gripe en España y en todo el mundo y, como consecuencia, hubo un número muy bajo de aislamientos de virus gripales. Este hecho es muy relevante porque la selección de virus candidatos para la vacuna necesita muestras de virus que permitan el diseño de la vacuna para la siguiente estación gripal y, en el primer año post-pandémico, el número de virus disponibles para dicho cometido disminuyó un logaritmo.
Las temporadas 21-22 y 22-23 fueron atípicas en cuanto a la gripe, sucediendo estas en dos picos epidémicos en que predominó la circulación del A(H3), siendo esta la primera vez en cincuenta años
Las dos temporadas siguientes de gripe, 2021-22 y 2022-23, fueron también atípicas. En ambas se produjeron dos ondas de gripe separadas por 4-6 semanas entre ambos picos epidémicos. En 2021-22 hubo una dominancia casi exclusiva del subtipo A(H3) en los dos picos epidémicos. Esta ha sido la primera vez que ocurría dicho fenómeno en los últimos cincuenta años, e hizo que la epidemia de gripe fuera más larga de lo habitual, aunque más repartida en el tiempo, ya que la máxima incidencia estuvo por debajo de los picos únicos epidémicos habituales en el periodo prepandémico COVID-19. La epidemia de gripe repartida en dos picos epidémicos tan separados ejerció menor presión sobre el sistema sanitario ya que fue una forma de sufrir la epidemia invernal “en dos plazos” en lugar del único pico agudo, de ascenso violento de la incidencia que caracteriza los perfiles epidémicos de la Gripe (Figura 1).
En la epidemia de 2022-23 se volvió a repetir el fenómeno de dos picos epidémicos separados por un espacio de cuatro semanas, pero esta vez en el primero las cepas dominantes pertenecían, por tercera vez consecutiva en un año, al subtipo A(H3), siendo el virus dominante en el segundo pico epidémico el virus B del linaje Victoria (Figura 2). Como dato de interés; durante todo el periodo interepidémico no hubo un descenso basal de casos similar a las temporadas prepandémicas, dándose casos graves en meses de verano y otoño. De hecho, al inicio del periodo de vigilancia de gripe (semana 40 a la 20 del siguiente año) la tasa de incidencia estaba cerca de los 40 casos/100.000. Finalmente, la actual temporada 2023-2024 ha tenido un perfil habitual, con un predominio del subtipo A(H1) aunque el subtipo A(H3) causó un número significativo de casos, pero solapándose a la circulación de A(H1).
Los niños nacidos en el 2020 y 2023, han tenido la oportunidad de una primoinfección con el subtipo A(H3), lo cual tendrá relevancia clínica en el futuro
Desde la óptica pediátrica eso ha hecho que la cohorte de los niños nacidos durante 2020 a 2023 hayan tenido más oportunidades de tener una primoinfección e imprinting por subtipo A(H3). Este hecho puede tener importancia futura, ya que esta cohorte de niños responderá mejor frente a este virus y a otros subtipos del grupo filogenético 2 al cual pertenece la hemaglutinina H3, fenómeno que tardará años en apreciarse, pero que tiene su relevancia epidémica y clínica.
En la pirámide poblacional actual las epidemias de A(H3) tienden a generar más casos graves entre la cohorte de nacidos antes de 1957 ya que esas personas sufrieron un imprinting por un virus A(H1) que fue el subtipo de virus A dominante desde la pandemia de Gripe Española de 1918 hasta la de gripe Asiática en 1957, en la que los virus A(H1) fueron sustituidos por el subtipo A(H2) de la pandemia Hong Kong. La cohorte de niños nacidos antes de 1957 sufre ahora las consecuencias de aquella primoinfección cuando se infectan por el subtipo A(H3), que, sin embargo, estuvieron más protegidos durante la pandemia de 2009. De igual forma la mayoría de niños nacidos entre 2020 a 2023 infectados por el subtipo A(H3) por primera vez, tendrán consecuencias similares al enfrentarse a virus con hemaglutininas del grupo filogenético 1 cuando sean mayores.
Menos clados de H3
Otra de las consecuencias de la baja incidencia de gripe durante los tres primeros años de la pandemia ha sido la reducción de clados de todos los subtipos y linajes, y especialmente los del subtipo A(H3) responsable frecuente del mismatch o discordancia antigénica de la vacuna(6).
En principio, este fenómeno puede ser debido a la menor presión de los humanos sobre el virus al haber menos infecciones durante ese periodo largo y ello podría facilitar la selección de clados a incluir en la vacuna al haber un número menor de ellos. Sin embargo, el comportamiento de los clados del subtipo A(H3) que han “resistido” a la anomalía pandémica, parecen haberse “repartido el pastel” de la dominancia epidémica haciendo que la decisión sobre la selección de cepas candidatas a la vacuna tenga parecidas dificultades. Hay que tener en cuenta que la tasa de variabilidad del subtipo A(H3) es casi 18 veces mayor que la del subtipo H1 y 5-6 veces más que el tipo B de gripe(7). De hecho, es la cepa de la vacuna que origina más mismatch o discordancia antigénica con los virus que realmente circulan 8 meses después de la selección de cepas vacunales por la OMS.
Desaparición de un virus: El fin del linaje Yamagata del tipo B de la gripe
El linaje B/Yamagata de la gripe B, componente de las vacunas cuadrivalentes de gripe, se considera de forma oficial desaparecido de la circulación gripal
En la actualidad el linaje B/Yamagata de la gripe B, componente de las vacunas cuadrivalentes de gripe, se considera de forma oficial desaparecido de la circulación gripal. La temporada de gripe 2017-18 del hemisferio Norte fue la última en la que se aislaron de forma mayoritaria virus B del linaje Yamagata, precisamente en una de las estaciones de mayor intensidad y gravedad del último decenio(8). Sin embargo, como si de un “canto del cisne” se tratara, este linaje no ha vuelto a aislarse desde entonces (Figura 3).
En ese espacio de tiempo se notificaron solo aislamientos esporádicos de ese linaje que, al ser debidamente secuenciados y caracterizados genéticamente, la mayoría de ellos han resultado ser similares a B/Phuket/3073/2013, cepa recomendada en las vacunas atenuadas e inactivadas; sin poderse excluir la posibilidad de la vacuna viva atenuada contra la gripe (LAIV). La OMS formuló en 2022 un requerimiento invitando a todos los NICs (National Influenza Centres) del GISRS (Global Influenza Surveillance and Response System) a realizar un esfuerzo concertado para identificar y caracterizar detalladamente el linaje de los virus B aislados para determinar si seguía en circulación alguno del linaje B/Yamagata que no estuviera relacionado con la vacuna atenuada. En las tres últimas temporadas han aparecido esporádicamente virus B/Yamagata, todos ellos identificados como consecuencia de la transmisión pediátrica de virus atenuados procedentes de la vacuna intranasal(9).
La OMS ha recomendado en 2023 la eliminación de la cepa del linaje B Yamagata de las vacunas de gripe en el menor tiempo posible
A la vista de esta circunstancia, la OMS ha recomendado en 2023 la eliminación de la cepa del linaje B Yamagata de las vacunas de gripe en el menor tiempo posible(10,11). La compañía que produce la vacuna intranasal atenuada se ha comprometido a realizarlo con las vacunas de 2024-25. La razón de este ruego es evitar que virus vivos, aunque atenuados, del linaje B/Yamagata vacunal, puedan recombinar o reordenarse con otros virus “salvajes” del tipo B, dando lugar a una reintroducción de linajes diferentes al B/Victoria. Ante esta circunstancia futura, se han propuesto distintas aproximaciones que se comentarán más adelante en el apartado de vacunas de gripe. Todas ellas implican la substitución del antiguo linaje B Yamagata por nuevas dianas víricas vacunales.
Vacunas de gripe en la edad pediátrica
España es uno de los países mundiales que se ha sumado a la iniciativa de la recomendación de la vacunación gripal pediátrica postulada por la OMS hace ya 12 años
España es uno de los países mundiales que se ha sumado a la iniciativa de la recomendación de la vacunación gripal pediátrica postulada por la OMS hace ya 12 años. La recomendación en España fue hecha en primer lugar por la AEP (Asociación Española de Pediatría) en 2021(12), seguida después por la recomendación oficial desde el Ministerio de Sanidad(13) en el año 2022, indicando la vacunación para la población pediátrica de 6 meses a menos de 5 años de edad, en línea con lo indicado por la OMS en su “Position Paper” de 2012(14) sobre vacunación gripal. Esta indicación de edad entre 6 y 59 meses es tardía y poco ambiciosa. La mayoría de países europeos con indicaciones pediátricas de indicación de vacunación gripal lo son hasta los 14 años de edad, un horizonte a tener en cuenta para modificaciones futuras de la vacunación infanto-juvenil de gripe.
La indicación formulada por el Ministerio ha sido implementada de distinta manera en las comunidades autónomas (CCAA) en el sentido de utilizar algunas de ellas, solo vacunas inactivadas o de subunidades inyectables mientras que otras CCAA, han administrado las inactivadas únicamente desde los seis meses a los menores de dos años y, a partir de esta edad, han usado las atenuadas inhaladas (Figura 4). Los resultados muestran diferencias en el perfil epidémico de la primera y segunda onda estacional que deben interpretarse con cautela dada la peculiaridad epidémica de esa temporada gripal. Cada vez más la recomendación de vacuna inhalada para niños de 24 a 59 meses se ha ido imponiendo en la mayoría de las CCAA, lo cual sin duda debe favorecer los aumentos de coberturas vacunales en la población pediátrica, máxime si se puede combinar con una administración a través de escuelas y colegios como la CCAA de Murcia.
Nuevas dianas víricas vacunales de gripe, vacunas en desarrollo
Como consecuencia de la desaparición del linaje B Yamagata desde el año 2020, la OMS recomendó en el año 2023 la retirada, lo antes posible, de las cepas B del linaje Yamagata. Es posible que algunas vacunas hayan ya retirado esta cepa B para la temporada 2024-2025. La eliminación de este linaje podría permitir la inclusión de otras nuevas dianas víricas o dos clados de virus del subtipo A/H3, la cepa que da lugar a un mayor mismatch o discordancia antigénica vacunal por temporadas.
Dadas las coberturas vacunales de España, debe seguir el ejemplo de Francia e Inglaterra, implementando la vacunación infantil de la gripe
Varios países europeos han implementado recientemente la recomendación de vacunación infantil. Sin embargo, debemos diferenciar muy bien aquellos que tienen recomendaciones – “ideales para la vacunación”, pero en los que sus coberturas en todas las poblaciones diana, están muy por debajo de las cifras recomendadas por la OMS (Austria, Lituania, Letonia, Estonia, etc.). Uno de los países con razonables coberturas de vacunación que ha implementado la vacunación infantil ha sido Francia y, al igual que Inglaterra, la ha recomendado en el grupo de mayores de 6 meses hasta los 14 años. Este ejemplo debe seguir España ya que, como comentamos al inicio de este artículo, la mayor incidencia y hospitalización por gripe es máxima en la población infanto-juvenil.
Al igual que otras vacunas frente a virus respiratorios, las vacunas de gripe tienen una efectividad subóptima. Las propuestas de incluir dianas víricas vacunales además de la hemaglutinina pueden facilitarse con la tecnología de las nuevas plataformas vacunales. A este respecto, las vacunas basadas en Virus-Like-Particles (VLPs) o las de células presentadoras de antígeno y las basadas en ARNm están especialmente concebidas para incluir varios epítopos diferentes del virus gripal en el producto vacunal. Los antígenos nuevos que se han propuesto son variados; nucleoproteína (NP), proteína M (matriz), proteína M2, tallo de la hemaglutinina o la neuraminidasa. Todos ellos exhiben una propiedad constante común que es la menor variabilidad evolutiva temporal de esos antígenos, se trata en todos los casos de antígenos muy conservados a lo largo de la variación del virus de la gripe. Algunos como la región externa de la M2 permanecen inalterados desde hace más de 50 años. En otros casos los antígenos que se han diseñado son aproximaciones para desarrollar una vacuna más universal de gripe frente a los 17 subtipos que tienen un origen aviar (H1-16 y la propuesta reciente de H19).
Para aumentar la efectividad de las vacunas de la gripe, se han propuesto incluir varios epítopos diferentes, así como la coadministración con otras vacunas COVID o anticuerpos anti VRS
Otra área de desarrollo de las vacunas de virus respiratorios y de gripe es la combinación de diferentes virus en una sola vacuna, al igual que sucede con las vacunas penta o hexavalentes pediátricas. Aunque en la mayoría de casos no existe contraindicación para la coadministración de vacunas de gripe y COVID o anticuerpos anti VRS, la posibilidad de tener presentaciones de vacuna que permitan la vacunación en una sola aplicación facilitaría la protección ampliada y alcanzar mayores coberturas vacunales frente a varios de los virus respiratorios principales.
Beneficios colaterales inesperados de la vacunación antigripal infantil
La vacunación antigripal en niños contribuye a la prevención de patología infecciosa general y respiratoria en particular
Algún estudio observacional ha descrito que los picos de mayor incidencia de gripe estacional se acompañan de clústeres de enfermedad meningocócica invasiva y meningitis infantil. Podría ser una consecuencia indirecta del estado de inmunocompromiso temporal que originan casi todas las viriasis respiratorias. Por otra parte, los servicios de salud del UK publicaron en la temporada 2022-23 un aumento general de los casos de escarlatina en su población infantil. Sin embargo, las cifras de casos fueron significativamente inferiores entre los niños y adolescentes que habían sido vacunados con la vacuna intranasal atenuada de Gripe, demostrándose una vez más que como si una “aspirina” de las vacunas se tratara, la vacunación antigripal en niños contribuye a su prevención de patología infecciosa general y respiratoria en particular.
Los niños vacunados de gripe con vacuna intranasal atenuada, desarrollan una inmunidad local en la mucosa respiratoria de las vías altas que dificulta mucho la transmisión del virus, aspecto difícil de evaluar en los trabajos observacionales de vida real. De forma similar dicha población pediátrica tiende a padecer menos infecciones respiratorias al igual que lo observado en los lactantes protegidos pasivamente frente al VRS con el ac monoclonal de larga duración.
Un virus emergente, SARS-CoV-2: tres hitos fundamentales
Evolución del SARS-CoV-2 desde su emergencia
Desde la aparición del SARS-CoV-2 en el año 2019 el virus causante de la COVID-19 ha sufrido una rápida y continua evolución desde sus variantes más graves al comienzo de la pandemia, (variantes ancestrales) hasta las más leves y moderadas observadas tras la aparición del linaje ómicron en 2022. El linaje ancestral, primer linaje del virus original, circuló de forma mayoritaria desde el comienzo de la pandemia hasta la aparición de la primera variante, denominada como D614G(15) por ser la primera mutación detectada en la proteína S (Spike) de este virus. Esta mutación surgida a los tres meses de difusión mundial del virus, estabilizó la proteína S incrementando de forma notable la infectividad del virus. Las posteriores variantes que aparecieron, como Alpha, Beta, Gamma y Delta surgieron por la constante deriva genética y antigénica del virus, traduciéndose en un aumento constante de la infecciosidad y en ocasiones, como en el caso de la variante Beta, a un notable escape inmune.
El virus continúa su evolución adaptándose al ser humano, incrementando su transmisibilidad y una menor virulencia, que se traduce en que la mayor parte de las infecciones cursen de forma asintomática, leve o moderada en las personas sin factores de riesgo”
En el mes de noviembre de 2021 se detectó por primera vez la variante Omicron (B.1.1.529)(16), la cual, a través de múltiples cambios aminoacídicos en la proteína S y otras proteínas estructurales, dio un salto cualitativo en la infecciosidad y transmisibilidad del virus SARS-CoV-2. Sin embargo, estos cambios conllevaron aparejada una reducción apreciable de la virulencia, comenzando una lenta pero constante reducción de la gravedad de la patología causada por la infección SARS-CoV-2 hasta la aparición de las variantes actuales de este linaje. En concreto, durante los años 2023 y 2024 han surgido diferentes sublinajes derivados de Omicron, como son los linajes BA.1, BA.2, BA.4/5, variantes como XBB1.5., EG.5, y la variante JN.1 dominante en la actualidad (Figura 5). El virus continúa así su camino evolutivo adaptándose cada vez más al ser humano, incrementando su transmisibilidad a la vez que mantiene una virulencia en niveles bajos, que se traduce en que la mayor parte de las infecciones cursen de forma asintomática, leve o moderada en casi todas las personas sin factores de riesgo. Sin embargo, estos cambios no han sido inocuos, ya que han afectado de forma importante a la antigenicidad y especificidad de las vacunas, reduciendo en algunos casos la efectividad de las mismas y obligando a su actualización.
Patogenicidad del SARS-CoV-2 en niños
Una de las grandes diferencias del SARS-CoV-2 con otros virus de infecciones respiratorias en humanos es la escasa virulencia demostrada en niños
Una de las grandes diferencias del SARS-CoV-2 con otros virus drivers de infecciones respiratorias en humanos, como la gripe o el VRS, es la escasa virulencia demostrada en niños desde el inicio de la pandemia. A pesar de que el virus ha ido variando de forma continua, ello no se ha
traducido en una forma grave de la infección en las personas más jóvenes. Este hecho aún no ha sido explicado con detalle, pero entre los factores que se han postulado están la inmadurez del sistema inmunitario de los niños, el cual, a través de una menor respuesta inflamatoria, ejerza un control del virus menos inmunopatogénico. Adicionalmente, la acumulación de las vacunaciones en el periodo infantil puede haber tenido un efecto positivo, ya que el mantenimiento de un estatus activado del sistema inmune se ha demostrado como protector frente a la gravedad de algunas infecciones. Por otro lado, la estructura del epitelio respiratorio es diferente entre los niños y los adultos. En el caso del epitelio nasal, los niños poseen menos densidad de células ciliadas que el de las personas de edad avanzada, mientras que los niños expresan una mayor cantidad de células secretoras de mucinas. Estos factores podrían estar relacionados con un aclaramiento más eficaz del virus, reduciendo la infecciosidad del mismo. Algunos autores han demostrado que la mayor densidad de células ciliadas proporciona receptores específicos para el SARS-CoV-2, por lo que podría incrementar la capacidad infecciosa del virus. Adicionalmente, las células aisladas del epitelio respiratorio superior de los niños muestran una mayor producción de interferón, que reduce significativamente la capacidad infecciosa del virus(18,19). Las consecuencias de que la infección siga siendo leve en niños es que las cohortes infanto-juveniles, infectadas muy tempranamente van a ser las que mediante su imprinting y las sucesivas reinfecciones sean responsables de la domesticación del virus en el futuro para la especie humana(20).
La diferente respuesta al coronavirus en niños, se puede deber a la diferente estructura del epitelio respiratorio con menor número de receptores al virus y mayor presencia interferón en el moco
Vacunación de COVID-19 en los niños
Se debe recomendar la vacunación de COVID-19 para los niños que tienen patologías de base, más vulnerables a la infección por SARS-CoV-2
La vacunación tiene un claro objetivo, reducir la incidencia de la enfermedad grave y la mortalidad. Es por tanto un dilema si debemos o no vacunar a los niños frente a la COVID-19 ya que en general, la infección se comporta de forma leve o muy leve en ellos. Una de las justificaciones de la vacunación es el beneficio individual del niño. Aunque hay comunicada cifras de muertes en niños, su incidencia es menor que en otras infecciones respiratorias prevenibles. Cuando se estudian en detalle, se observa que la mortalidad en niños por COVID-19 ocurren preferentemente en niños con patologías subyacentes. Por lo tanto, se debe recomendar la vacunación de COVID-19 para los niños que tienen patologías de base, más vulnerables a la infección por SARS-CoV-2. Por tanto la decisión de incluir la vacunación rutinaria de COVID-19 en la edad pediátrica es compleja de tomar y depende de diversos factores, tanto éticos, como económicos, políticos y epidemiológicos(21), que tiene que tener en cuenta el riesgo/beneficio del acto vacunal.
Repercusión de la pandemia sobre otros virus respiratorios
Como consecuencia de la anomalía pandémica, otros virus respiratorios típicamente estacionales sufrieron una importante alteración durante el primer año pandémico. El VRS fue uno de los virus que sufrió alteraciones epidémicas como consecuencia de las MNF
Como consecuencia de la anomalía pandémica, otros virus respiratorios típicamente estacionales sufrieron una importante alteración durante el primer año pandémico. Se debe resaltar que no todos los virus respiratorios experimentaron los cambios notables referidos en gripe. Es el caso de rinovirus, adenovirus, virus parainfluenza y coronavirus endémicos que, aunque aislados con significativa menor frecuencia, mantuvieron su patrón estacional característico a lo largo de todo el año. Sin embargo, el virus respiratorio sincitial (VRS) fue uno de los virus que sufrió alteraciones epidémicas como consecuencia de las MNF. Los pediatras españoles observaron por primera vez un pico epidémico de infecciones por VRS entre la primavera y el verano de 2021. Un hecho similar se había producido en Australia, y algunos autores habían anticipado esa posibilidad epidemiológica(22). La ausencia de circulación del VRS durante un periodo de más de un año entre la población infantil provocó que aumentara la población pediátrica susceptible y el cese de los confinamientos, unido a la normalidad social (apertura de colegios, parques, etc.) hizo el resto. Los datos procedentes del hemisferio sur se confirmaron también en Europa. Aunque en las epidemias desestacionalizadas postpandémicas de VRS hubo una mayor incidencia que en las prepandémicas, las tasas de hospitalización y los casos graves fueron menores en aquellas primeras ondas epidémicas desestacionalizadas, debido a que la media de edad de la cohorte de niños infectados fue más alta y, por consiguiente, la maduración inmune y pulmonar mucho más adelantada.
Conclusiones
- La normalización de la epidemiología de los virus respiratorios va restableciéndose paulatinamente, tras dos años de pandemia aguda de COVID-19, aunque no se pueden descartar que se den algunas de las anomalías observadas en años recientes.
- El nuevo virus SARS-CoV-2 no se ha estacionalizado todavía, lo que, unido a la evanescencia de los anticuerpos con el tiempo, complica la estrategia vacunal en población infanto-juvenil debiendo aplicarse a los niños con comorbilidades.
- La posibilidad de coadministración de vacunas respiratorias debe ayudar a mejorar las coberturas de gripe en niños. Todas estas medidas junto a otras de protección pasiva específicas para VRS, redundarán en una menor incidencia de consultas, hospitalizaciones y muertes pediátricas.
- La asunción por los pediatras de estas premisas y la fuerza de la recomendación de la vacunación son los elementos claves para una mejor profilaxis de las infecciones respiratorias en población infanto-juvenil, dada las sinergias que comparten entre ellas.
Tablas y figuras
Figura 1.Circulación epidémica de los virus gripales desde la temporada prepandémica 2015-2016 hasta la actual temporada 2023-2024
Se observan dos ondas estacionales en las temporadas 2021-2022 y 2022-2023 y mayor duración que en época prepandémica.
Modificado de: FluNet(4).
Figura 2. Perfil de la epidemia de gripe 2022-2023 en España con dos picos epidémicos separados y una distribución de casos en un periodo más largo de tiempo
Se observa en la semana 40 del 2022 al inicio de casos una tasa de 40/100.000 casi en el límite del umbral de alerta epidémica.
Modificado de: ISCIII, Instituto de Salud Carlos III(5).
Figura 3. Circulación mundial de linajes de gripe B desde la temporada de gripe 2017-2018
Circulación mundial de linajes de gripe B (Victoria y Yamagata) desde la temporada de gripe 2017-2018, en la que se identificaron por última vez linajes circulantes de gripe B/Yamagata.
Modificado de: FluNet(4).
Figura 4. Perfil de la epidemia estacional de gripe de 2022-2023
Perfil de la epidemia estacional de gripe de 2022-2023 en España y en otras CCAA que iniciaron la vacunación estacional pediátrica y tipos de vacunas empleadas(5).
Figura 5. Evolución genética de las variantes y subvariantes de SARS-CoV-2
Desde su emergencia en el año 2020 hasta la aparición de la variante de interés (VOI) JN.1 a finales del año 2023(17).
Bibliografía
- CAV-AEP. Vacunación antigripal 2023-24: Recomendaciones del CAV-AEP [Internet]. 2023 [citado 24 de abril de 2024]. Disponible en: https://vacunasaep.org/profesionales/noticias/vacunacion-antigripal-recomendaciones-CAV-2023-24.
- CAV-AEP. Ministerio de Sanidad: Recomendaciones de uso de Nirsevimab contra el VRS en la temporada 2023-24 [Internet]. 2023 [citado 24 de abril de 2024]. Disponible en: https://vacunasaep.org/profesionales/noticias/vrs-nirsevimab-ministerio-de-sanidad-jul2023.
- Ortiz de Lejarazu Leonardo R, Sanz Muñoz I. El año que “no tuvimos” gripe. Pediatr Integral 2022; XXVI (6): 382.e1 – 382.e7 [Internet]. [Citado 24 de abril de 2024]. Disponible en: https://www.pediatriaintegral.es/publicacion-2022-09/el-ano-que-no-tuvimos-gripe/.
- OMS. Flunet [Internet]. 2024 [citado 6 de mayo de 2024]. Disponible en: https://app.powerbi.com/view?r=eyJrIjoiZTkyODcyOTEtZjA5YS00ZmI0LWFkZGUtODIxNGI5OTE3YjM0IiwidCI6ImY2MTBjMGI3LWJkMjQtNGIzOS04MTBiLTNkYzI4MGFmYjU5MCIsImMiOjh9.
- SIVIRA, ISCIII. Vigilancia centinela de Infección Respiratoria Aguda en Atención Primaria (IRAs) y en Hospitales (IRAG): Gripe, COVID-19 y VRS CNE-CNM. ISCIII. Informe no 168. Semana 05/2024 (del 29 de enero al 4 de febrero del 2024) [Internet]. 2024 [citado 9 de febrero de 2024]. Disponible en: https://docsivira.isciii.es/Informe_semanal_SiVIRA_202405_n168.html.
- Dhanasekaran V, Sullivan S, Edwards KM, Xie R, Khvorov A, Valkenburg SA, et al. Human seasonal influenza under COVID-19 and the potential consequences of influenza lineage elimination. Nat Commun. 2022;13:1721.
- Neher RA, Bedford T, Daniels RS, Russell CA, Shraiman BI. Prediction, dynamics, and visualization of antigenic phenotypes of seasonal influenza viruses. Proceedings of the National Academy of Sciences. 2016;113:E1701-9.
- Vajo Z, Torzsa P. Extinction of the Influenza B Yamagata Line during the COVID Pandemic—Implications for Vaccine Composition. Viruses. 2022;14:1745.
- Paget J, Caini S, Del Riccio M, van Waarden W, Meijer A. Has influenza B/Yamagata become extinct and what implications might this have for quadrivalent influenza vaccines? Euro Surveill. 2022;27:2200753.
- OMS. Recommended composition of influenza virus vaccines for use in the 2024 southern hemisphere influenza season [Internet]. 2023 [citado 24 de abril de 2024]. Disponible en: https://cdn.who.int/media/docs/default-source/influenza/who-influenza-recommendations/vcm-southern-hemisphere-recommendation-2024/202309_recommendation.pdf?sfvrsn=2c2cbebd_8&download=true.
- The Lancet Infectious Diseases. Influenza vaccine shake-up. Lancet Infect Dis. 2023 Dec;23(12):1323.
- AEP. El Comité Asesor de Vacunas de la AEP recomienda la vacunación antigripal a todos los niños de entre 6 y 59 meses de edad [Internet]. 2021 [citado 24 de abril de 2024]. Disponible en: https://www.aeped.es/sites/default/files/20210920_ndp_cav-aep_vacunacion_gripe_2021-2022.pdf.
- Ministerio de Sanidad. Recomendaciones de vacunación frente a gripe y COVID-19 en la temporada 2023-2024 en España. Actualización. [Internet]. 2023 [citado 24 de abril de 2024]. Disponible en: https://www.sanidad.gob.es/areas/promocionPrevencion/vacunaciones/gripe_covid19/docs/RecomendacionesVacunacion_Gripe-Covid19.pdf.
- OMS. Vaccines against influenza. WHO position paper November 2012 [Internet]. 2012 [citado 24 de abril de 2024]. Disponible en: https://www.who.int/docs/default-source/immunization/position_paper_documents/influenza/pp-influenza-november2012-summary.pdf?sfvrsn=d499e0d7_2.
- Pérez-Abeledo M, Sanz Moreno JC. Variantes de SARS-CoV-2, una historia todavía inacabada. Vacunas. 2021;22:173-9.
- Khandia R, Singhal S, Alqahtani T, Kamal MA, El-Shall NA, Nainu F, et al. Emergence of SARS-CoV-2 Omicron (B.1.1.529) variant, salient features, high global health concerns and strategies to counter it amid ongoing COVID-19 pandemic. Environ Res. 2022;209:112816.
- Nextstrain. [Internet]. 2024 [citado 6 de mayo de 2024]. Disponible en: https://nextstrain.org/.
- Woodall MNJ, Cujba AM, Worlock KB, Case KM, Masonou T, Yoshida M, et al. Age-specific nasal epithelial responses to SARS-CoV-2 infection. Nat Microbiol. 2024;1-19.
- Balázs A, Millar-Büchner P, Mülleder M, Farztdinov V, Szyrwiel L, Addante A, et al. Age-Related Differences in Structure and Function of Nasal Epithelial Cultures From Healthy Children and Elderly People. Front Immunol. 2022;13:822437.
- Ortiz de Lejarazu y Leonardo R. Future of vaccination against SARS-CoV-2 infection. Open Respir Arch. 2021;3:100117.
- Martinón-Torres F. Pediatric vaccination against COVID-19 and despite COVID-19. An Pediatr (Barc). 2022;96:4-7.
- Sanz-Muñoz I, Tamames-Gómez S, Castrodeza-Sanz J, Eiros-Bouza JM, de Lejarazu-Leonardo RO. Social Distancing, Lockdown and the Wide Use of Mask; A Magic Solution or a Double-Edged Sword for Respiratory Viruses Epidemiology? Vaccines (Basel). 2021;9:595.
No existen conflictos de interés en la realización de este artículo.
Situación actual de la gripe y la COVID-19 en la población infanto-juvenil