Nevus melanocíticos, trastornos de pigmentación y fotoprotección en adolescentes
A. Navarro-Bielsa(1), P. Gil-Pallares(2), Y. Gilaberte(1).
Servicio de Dermatología. (1)Hospital Universitario Miguel Servet, Zaragoza. (2)Complejo Hospitalario Universitario de Ferrol.
Fecha de recepción: 24-02-2022
Fecha de publicación: 28-02-2022
Adolescere 2022; X (1): 53-63
Resumen
|
Los nevus melanocíticos son las neoplasias más frecuentes y uno de los motivos más comunes de derivación al especialista, sobre todo con consultas relacionadas con su benignidad o malignidad así como la necesidad o no de su extirpación. De manera general los nevus melanocíticos se dividen en adquiridos y congénitos dependiendo del momento de aparición y el principal diagnóstico diferencial se realiza con otras lesiones pigmentadas como hiperplasias melanocíticas epidérmicas o melanosis dérmicas circunscritas. La incidencia del melanoma está en aumento, aunque en menores de 20 años constituyen solo el 1-3% de todos los melanomas. Se ha demostrado que una fotoprotección adecuada, sobre todo, durante la infancia y adolescencia y la autoobservación, son las principales medidas para luchar contra el melanoma.
Palabras clave: Nevus; Melanoma; Fotoprotección; Adolescentes.
|
Abstract
|
Melanocytic nevi are the most frequent neoplasm and one of the most common reasons for referral to a specialist, especially with queries related to their benignity or malignancy, as well as the need or not for their removal. Depending on the moment of appearance, melanocytic nevi are divided into acquired and congenital. The differential diagnosis includes other pigmented lesions such as epidermal melanocytic hyperplasias or circumscribed dermal melanosis, among others. Although the incidence of melanoma is increasing, melanomas in patients younger than 20 years only represent 1-3% of all melanomas. It has been shown that adequate photoprotection, especially during childhood and adolescence, and self-monitoring, are the main measures to prevent melanoma.
Key words: Nevi; Melanoma; Photoprotection; Teenagers.
|
Introducción
Los nevus melanocíticos son las neoplasias más frecuentes y uno de los motivos más comunes de derivación de los adolescentes al dermatólogo, sobre todo con consultas relacionadas con su benignidad o malignidad y con la necesidad de realizar seguimiento o establecer o no tratamiento. De manera general, los nevus melanocíticos se dividen en adquiridos y congénitos y el principal diagnóstico diferencial se realiza con otras lesiones pigmentadas como hiperplasias melanocíticas epidérmicas o melanosis dérmicas circunscritas. La aparición de nevus en niños se ha relacionado con la exposición solar intermitente, la historia de quemaduras solares y fototipos claros (I y II), así como antecedentes de leucemia y quimioterapia, siendo en este último caso de tipo acral más frecuente(1).
Los nevus melanocíticos son las neoplasias más frecuentes y uno de los motivos más comunes de derivación de los adolescentes al dermatólogo
A continuación, realizamos una revisión de estos tres principales grupos de lesiones pigmentadas con el objetivo de ayudar a discernir entre las diferentes entidades y establecer criterios por los que derivar al especialista. Además, se abordará el tema de la fotoprotección en el adolescente, factor modificable que ayuda a la prevención de quemaduras y con ello a la prevención de cáncer cutáneo.
Lesiones melanocíticas
Los nevus adquiridos comienzan a aparecer a partir de los 2 años
Las lesiones névicas se dividen en congénitas y adquiridas en función del momento en el que aparecen. Habitualmente los nevus adquiridos comienzan a aparecer a partir de los 2 años, siendo el patrón dermatoscópico globular el predominante, aumentando de forma importante tanto en número de lesiones, como en el tamaño de las mismas durante la adolescencia y cambiando el patrón dermatoscópico predominante de globular a reticular, hasta la 3º – 4º década, a partir de la cual estas lesiones tienden a la autoinvolución. En cambio, dentro de nevus congénitos se englobarían aquellos presentes al nacimiento (en un 0,2-2,1%) o que aparecen antes de los 2 años de vida(2).
Nevus melanocíticos adquiridos
Nevus melanocítico juntural
Clínicamente se presenta como una mácula hiperpigmentada, de tamaño y forma variable. En la biopsia se observan melanocitos en la unión epidérmica, agrupados en pequeños nidos o aislados. En la dermatoscopia típicamente presentan un patrón reticular. Estos nevus son los más frecuentemente encontrados en las etapas medias de la vida(3).
Nevus melanocítico compuesto
Se presenta como una lesión más o menos papulosa, muy típico de la infancia, y con un crecimiento y oscurecimiento habitual al principio de la adolescencia. En la dermatoscopia se caracterizan por presentar un patrón globular, que se correspondería con nidos más o menos grandes, en la unión dermoepidérmica, pudiendo extenderse a la dermis papilar. El patrón de glóbulos en periferia simétrico es común en los adolescentes y es indicativo de nevus en crecimiento(4).
Nevus melanocítico intradérmico
Es más frecuente en edades avanzadas que en la adolescencia e infancia. Generalmente son papulosos, con forma cupuliforme o pediculada, y no muy pigmentados, aunque también pueden presentar coloración marrón más o menos oscura. En la dermatoscopia generalmente se aprecian vasos en coma y restos de pigmento en la superficie, o también patrón en empedrado. Histológicamente se encuentran células névicas en dermis papilar y reticular con escaso pigmento, más o menos agrupadas, con tendencia a la maduración en profundidad.
Nevus melanocítico atípico
También denominados nevus displásicos, lesiones pigmentadas atípicas que se pueden presentar de forma esporádica (lesiones aisladas o múltiples) o con carácter familiar (síndrome del nevus displásico). Las características clínicas serían tamaño mayor de 5 mm, color irregular, asimetría y bordes irregulares (Fig. 1a). No hay criterios dermatoscópicos que permitan el diagnóstico de certeza pero el patrón predominante es el reticular globular, seguido del multicomponente. Estos patrones dermatoscópicos y clínicos atípicos pueden presentarse también en los melanomas, por lo que se ha de valorar la exéresis de estas lesiones.
Nevus de Spitz-Reed
Nevus de Spitz-Reed: aparecen típicamente en las dos primeras décadas de la vida y suelen presentar un crecimiento rápido (3-6 meses), asociando en ocasiones prurito, dolor o incluso sangrado
Aparecen típicamente en las dos primeras décadas de la vida y suelen presentar un crecimiento rápido (3-6 meses), asociando en ocasiones prurito, dolor o incluso sangrado. Generalmente aparecen en cara y en extremidades como una pápula o nódulo redondeado de coloración rojiza, o también como una lesión marrón muy pigmentada o negra, pudiendo tener distintos colores o forma irregular. En la dermatoscopia se ha descrito el patrón en estallido de estrellas como característico, aunque también se observa en lesiones en crecimiento (Fig 1b)(5). El principal diagnóstico diferencial es el de melanoma, por lo que en muchas ocasiones es necesaria la exéresis, aunque no existe un consenso sobre el manejo, dado que no se conoce exactamente la biología y el pronóstico de estos nevus, al existir algunos con potencial agresivo(6).
Halo nevus o nevus de Sutton
Son lesiones típicas de la adolescencia, se presenta como un halo hipopigmentado y simétrico alrededor de un nevus, generalmente en la espalda, que puede progresar hasta hacer desaparecer el propio nevus. Pueden ser múltiples en hasta un 50% de los pacientes y con el paso del tiempo, suele recuperarse la coloración del área despigmentada. Se desconoce la causa, pero se cree que podría deberse a una reacción auntoinmune contra los melanocitos dado que en algunos casos estos pacientes llegan a presentar vitíligo. Además, se ha descrito la aparición de múltiples halo nevus en pacientes con melanoma oculto, pero este fenómeno es raro en la infancia y suele darse en la edad adulta(7).
Nevus de Meyerson
Nevus de Meyerson: lesión similar a eccema alrededor y sobre un nevus melanocítico. Frecuente en dermatitis atópica y psoriasis
Se trata de un fenómeno frecuente en niños con dermatitis atópica o psoriasis, en el que aparece una lesión similar a un eccema alrededor y sobre un nevus melanocítico. Generalmente remite al tratar la reacción eccematosa(8).
Nevus en diana o escarapela y en eclipse
Frecuentemente encontrado en pacientes jóvenes, se presenta como una lesión simétrica en forma y color, con una zona central pigmentada rodeada de una zona más clara y otra externa también pigmentada. No presenta un riesgo aumentado de malignización. El nevus en eclipse es característico en el cuero cabelludo y presenta un centro más claro y un halo periférico más pigmentado.
Nevus lentiginoso o moteado de Spilus
Suele ser adquirido y presentarse al principio de la infancia, aunque también hay casos descritos congénitos. Clínicamente aparece una mácula similar a una mancha café con leche sobre la que aparecen nevus junturales lentiginosos o compuestos, muy variable en tamaño (Fig. 1c). Hay casos descritos asociados con melanoma por lo que, ante cambios sugestivos de atipia es recomendable la biopsia o exéresis(9).
Nevus melanocíticos congénitos
El nevus congénito grande/gigante se asocia con una mayor tasa de afectación del SNC y con más riesgo de desarrollar un melanoma
Los nevus melanocíticos congénitos son hamartomas del neuroectodermo causados por mosaicismos genéticos. Se presentan en el 1-6% de nacimientos y normalmente se clasifican según su tamaño (Fig. 2). El nevus congénito grande/gigante se asocia con una mayor tasa de afectación del SNC y con más riesgo de desarrollar un melanoma sobre nevus, por lo que requiere un seguimiento dermatoscópico y clínico estrecho para poder detectar estos melanomas en etapas tempranas, además de requerir pruebas de imagen en muchos de los casos para descartar la proliferación de melanocitos en el sistema nervioso central en lo que constituye el síndrome del nevus melanocítico congénito(10). Los nevus congénitos suelen evolucionar hasta la pubertad y dermatoscópicamente predomina el patrón globular(11).
Melanoma
La regla ABCDE: asimetría, bordes irregulares, varios colores, tamaño mayor de 6 mm y evolución, crecimiento o cambio
Únicamente un 1-3% de los melanomas se diagnostican antes de los 20 años de vida, suponiendo el 15% de los cánceres diagnosticados entre los 15 y los 19 años, y solo el 1,2% de los diagnosticados en menores de 15 años(12). Los melanomas pueden aparecer de “novo”, pero también pueden presentarse sobre un nevus preexistente, siendo este último caso más frecuente que en adultos, especialmente cuando se originan sobre nevus congénitos grandes y gigantes. Generalmente se presentan con una o varias de las características de la regla ABCDE: asimetría, bordes irregulares, varios colores, tamaño mayor de 6 mm y evolución, crecimiento o cambio. Otro signo a tener en cuenta es el denominado “patito feo”, en el que la lesión destaca sobre las demás, bien por coloración o tamaño, entre otras.
Del mismo modo que en los adultos, aparecen más frecuentemente en tronco y extremidades y el pronóstico es también similar, siendo el índice de Breslow el factor pronóstico más importante. La cirugía es el tratamiento de elección y en función del estadio podría ser necesaria la adición de otros tratamientos adyuvantes, como podrían ser los distintos esquemas de inmunoterapia(13).
Hiperplasias melanocíticas epidérmicas
En las hiperplasias melanocíticas hay un número normal de melanocitos, de mayor tamaño y con mayor contenido de melanina, no implica más riesgo de malignización
Las lesiones consideradas como hiperplasias melanocíticas cuentan con un número normal de melanocitos, aunque de mayor tamaño y con mayor contenido de melanina, sin implicar por ello un riesgo aumentado de malignización. Dentro de este grupo se incluyen:
Efélides
Son máculas hiperpigmentadas claras, de pequeño tamaño, bien delimitadas y redondeadas, con predilección por zonas fotoexpuestas y más en los fototipos bajos. Se caracterizan por una aumento del tamaño de los melanocitos en la capa basal junto a un aumento del número de dendritas y marcada hiperpigmentación de la epidermis, pero sin aumento de melanocitos (Fig. 3).
Manchas café con leche
En la neurofibroma-tosis tipo 1, se presentan al menos 6 manchas café con leche con un tamaño de 15 mm
Se trata de máculas de color marrón más o menos claro, con bordes netos, generalmente redondeadas. Aunque un 10% de la población presenta estos tipos de lesiones aisladas o de pequeño tamaño, se pueden ver en el contexto de algunos síndromes, siendo el más frecuente la neurofibromatosis tipo 1, si se presentan al menos 6 con un tamaño de 15 mm, o en el síndrome de Legius(14).
Lentigo simple
Consiste en una mácula marrón, parduzca, redondeada y pequeña que puede afectar a la piel y mucosas; suelen ser múltiples y están presentes en la infancia y la pubertad, sin presentar cambios con la exposición solar ni con el tiempo. Histológicamente se observa un aumento del número de melanocitos en la capa basal epidérmica además de una hiperplasia epidérmica. Hay que considerar que se pueden ver en el contexto de diferentes síndromes, el más conocido el síndrome de Peutz-Jeghers o el síndrome de Carney.
Nevus de Becker
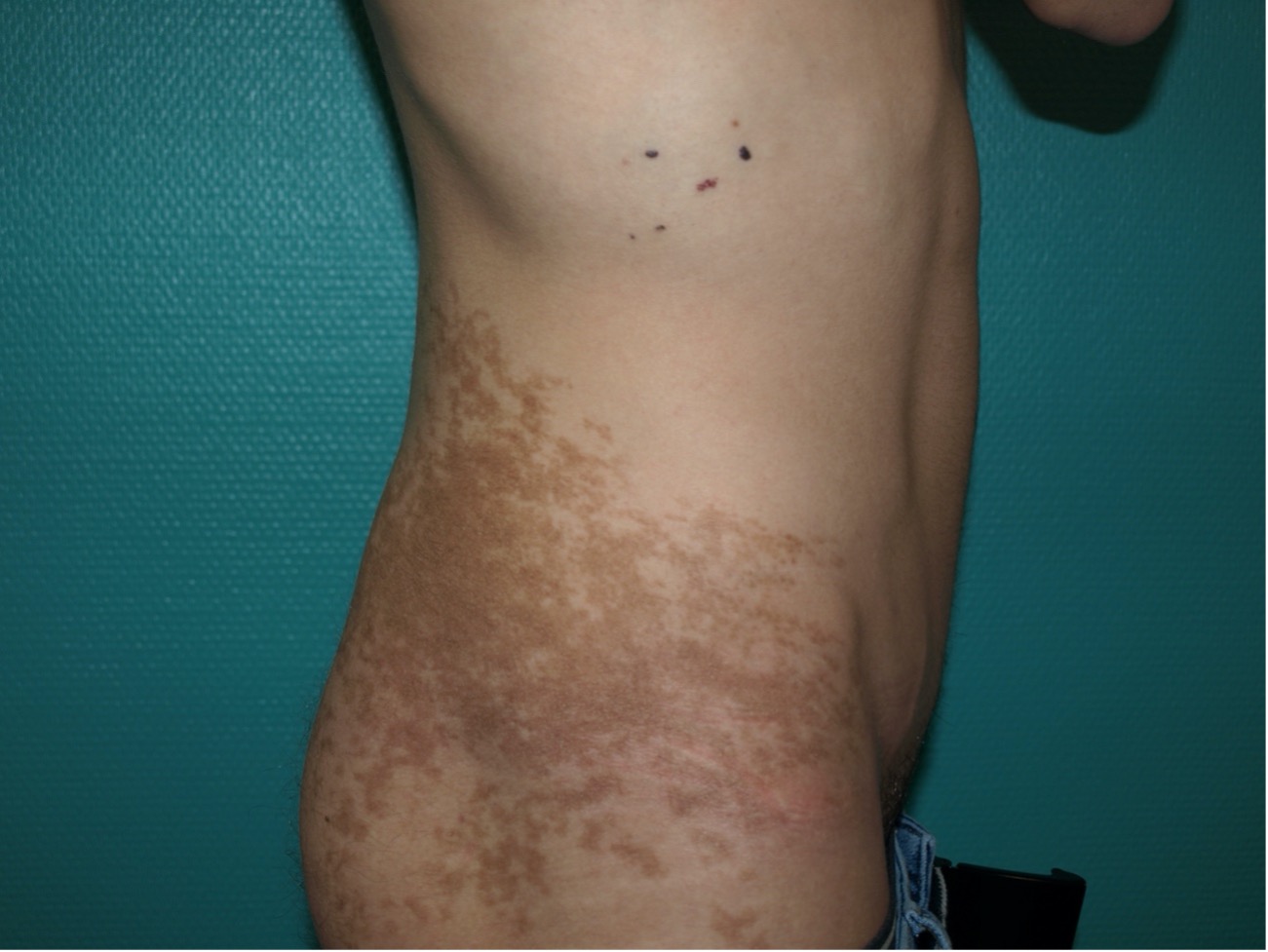
Generalmente aparecen en varones al inicio de la pubertad como una lesión única más o menos grande, hiperpigmentada, con bordes más o menos irregulares, pudiendo haber engrosamiento cutáneo así como folículos pilosos más prominentes, de localización preferentemente axial o proximal (Fig. 4)(15).
Melanosis dérmicas circunscritas
Caracterizadas por la presencia de melanocitos profundos en dermis, por lo que la localización del pigmento en estos estratos más profundos les confiere una coloración azulada(16).
Mancha mongólica
Habitualmente de bordes no bien definidos, de color grisáceo y en región lumbosacra o proximal. Está presente al nacimiento y desaparece antes de la pubertad, a los 3-4 años.
Nevus de Ota
Nevus de Ota: mácula azulada de bordes no bien definidos que se presenta en el territorio de las dos primeras ramas del trigémino, pudiendo afectar al globo ocular
Mácula azulada de bordes no bien definidos que se presenta en el territorio de las dos primeras ramas del trigémino, pudiendo afectar al globo ocular. Algunos trabajos hablan de un mayor riesgo de tumores malignos en los pacientes con nevus de Ota, especialmente oculares, cutáneos o del sistema nervioso central(17).
Nevus de Ito
Se trata de una lesión similar al nevus de Ota, pero que se presenta en la región deltoidea. Aunque es raro existe la posibilidad de aparición de melanoma en asociación con un nevus de Ito.
Nevus azul
Pueden estar presentes al nacimiento aunque habitualmente aparecen en la pubertad. Son más frecuentes en mujeres jóvenes en antebrazos y dorso de manos y pies, y el aspecto es el de una lesión máculo-papulosa bien delimitada de color azul homogéneo oscuro (Fig. 1d). Existe una variante celular con crecimiento progresivo que generalmente aparece en glúteos, región sacra o cuero cabelludo que puede presentar agresividad local o potencial de malignización, por lo que ante su sospecha
debe extirparse.
Mosaicismo pigmentario
El mosaicismo pigmentario describe patrones de pigmentación cutánea y pueden ser hiperpigmentados, hipopigmentados o combinados
El término mosaicismo pigmentario describe patrones de pigmentación cutánea causados por la heterogeneidad genética de las células de la piel. Estos mosaicismos pueden ser hiperpigmentados, hipopigmentados o combinados y pueden seguir unos patrones de distribución diversos en la piel.
Lo más importante es considerar que un número significativo de ellos se asocia a anomalías extracutáneas, especialmente neurológicas y musculoesqueléticas(18).
Fotoprotección
La exposición al sol aunque es necesaria puede tener efectos nocivos, como quemadura solar, el cáncer de piel y el fotoenvejecimiento
La exposición al sol es necesaria para la vida, nos proporciona vitamina D, regula el sistema cardiovascular y modula nuestro ánimo. Sin embargo, también puede tener efectos nocivos, siendo los más relevantes la quemadura solar, el cáncer de piel y el fotoenvejecimiento.
El espectro de radiación solar está compuesto por diferentes tipos de radiación y a cada una de ellas se le han atribuido diferentes efectos:
- Radiación ultravioleta B (UVB) (280-320 nm): daño en el ADN, inmunosupresión (favorece la aparición de herpes simple), quemadura solar, síntesis de vitamina D y estímulo de la pigmentación.
- Radiación ultravioleta A (RUVA) (320-400 nm): formación de radicales libres, daño en el ADN (directo e indirecto a través del efecto de los radicales libres), hiperpigmentación y fotoenvejecimiento.
- Radiación azul-violeta (380-455 nm): hiperpigmentación.
- Radiación infrarroja cercana (800-2500 nm): contribuye al fotoenvejecimiento.
De todos estos efectos, el énfasis se pone en el cáncer cutáneo, especialmente porque es el más frecuente del ser humano y la RUV ha sido reconocido por la OMS como su principal carcinógeno(19).
Por todo ello, tener un comportamiento adecuado de exposición solar, que nos permita aprovechar sus beneficios evitando sus efectos nocivos, es fundamental para la salud.
La exposición solar durante la infancia y la adolescencia ocurre con más frecuencia que en la vida adulta ya que se realizan más actividades de recreo y deporte
La exposición solar durante la infancia y la adolescencia ocurre con más frecuencia que en la vida adulta ya que se realizan más actividades de recreo y deporte. De hecho, el tiempo de exposición al sol en este periodo de la vida se ha asociado con un mayor riesgo de padecer cáncer de piel. El número de quemaduras en la infancia también se sabe que incrementa riesgo de melanoma(20). Incluso el grado de fotoenvejecimiento y la aparición de lentigos solares es mayor cuando la exposición solar en la infancia ha sido excesiva(21). Por todo ello, es necesario que este grupo de población realice una adecuada fotoprotección.
Campañas de fotoprotección
Se han realizado muchas campañas fotoeducativas destinadas a niños, ya que es más fácil establecer hábitos saludables a edades tempranas que modificar hábitos inadecuados con posterioridad. No obstante, es necesario que estas campañas tengan una continuidad para que esos hábitos adquiridos en la infancia persistan en la adolescencia y la juventud(22).
Es necesario que las campañas fotoeducativas tengan una continuidad para que los buenos hábitos adquiridos en la infancia persistan en la adolescencia y la juventud
La etapa de la adolescencia es un momento crítico en el tema de fotoprotección. En esta época, la influencia de la moda o de los influencers puede anteponerse a lo que es bueno para la salud.
El bronceado se ha considerado en las últimas décadas como un signo de belleza, y su búsqueda puede poner en riesgo la salud de la piel, favoreciendo la posibilidad de sufrir una quemadura solar, y a la larga incrementar el riesgo de cáncer cutáneo y fotoenvejecimiento. Se han realizado diferentes campañas de fotoprotección dirigidas a adolescentes que revelan que, aunque sus conocimientos sobre el daño solar y la fotoprotección son buenos, los hábitos no lo son. En Brasil, un estudio mostró que solo un 15% de los adolescentes usaba fotoprotector diariamente, un 67% lo usaban solo cuando iban a la playa y el 70% utilizaba un FPS (factor de protección solar) 30 o superior; el 57% iban a la playa en el momento de mayor insolación (entre las 10 a las 16h) y más de la mitad referían que la fotoprotección se les olvidaba, habiendo sufrido una quemadura solar el 73% de los encuestados(23). En nuestro país, un estudio realizado en educación secundaria reveló que tener una actitud positiva hacia el gusto por el bronceado y tomar el sol se asoció con unos hábitos de exposición solar inadecuados y unas medidas de fotoprotección deficientes(24). Además, comparativamente con los niños o los padres y profesores, los adolescentes son el grupo que sufre más quemaduras solares (44%, 54% y 75% respectivamente)(25). En una entrevista realizada a 977 jóvenes entre 14 y 24 años en USA, el 88% afirmaron que proteger su piel del sol es muy importante o importante y, aunque el 90% afirmaron usar fotoprotector, el 81,1% habían sufrido 1 o más quemaduras solares, incluso el 28,4% referían 5 o más(26).
En cuanto a las campañas de fotoeducación dirigidas a adolescentes, un metaanálisis reciente concluye que el efecto de las mismas sobre usar fotoprotector o sombrero es poco relevante y apuntan hacia usar modelos de intervención digitales e interactivos en estas campañas de fotoprotección dirigidas a enseñanza secundaria(27). Intervenciones basadas en la imagen, visualizando su imagen con una lámpara de luz negra que pone de manifiesto signos de fotoenvejecimiento, o escuchar el testimonio de una persona que ha padecido cáncer de piel pueden ayudar a concienciar a los adolescentes para adoptar unos hábitos adecuados de fotoprotección. Preguntados los adolescentes sobre iniciativas para aumentar la fotoprotección sugirieron demostrar las consecuencias de la exposición solar (41%), usando medios de comunicaciones tradicionales (16,8%) y aumentar la accesibilidad a los productos (10,6%)(26). Asimismo, instalar sistemas de medición de la radiación UV en los institutos de educación secundaria aunque no consiguió mejorar los comportamientos fotoprotectores, si incrementó el conocimiento sobre la RUV y la consulta de estos dispositivos para planear su fotoprotección(28).
Métodos de fotoprotección
Las medidas de fotoprotección que deben realizar los adolescentes son iguales que para toda la población: evitar las horas centrales del día y utilizar sombras, especialmente en la primavera y el verano, utilizar ropas y gorros, completar esto con el uso de cremas fotoprotectoras, y no olvidar la protección ocular mediante gafas de sol.
Fotoproteccción física
Los sombreros y las gorras proporcionan una buena pantalla física de fotoprotección para la cara y el cuello. No obstante, no todos los gorros son útiles ya que se necesitan mayores de 7,5 cm de ala para proteger la cara, los pabellones auriculares y el cuello.
La capacidad fotoprotectora frente a la RUV de los tejidos usados en la ropa se mide mediante el UPF (ultraviolet protection factor), término acuñado en Australia en 1996, que se mide in vitro por la transmisión de luz UVA y UVB a través del tejido mediante un espectrofotómetro. Factores como el color (los oscuros protegen mejor que los claros), el grosor, encogimiento o estiramiento de la prenda así como el grado de humedad son factores que influyen en el FPU (Factor de Protección Ultravioleta). La licra y el elastano son los tejidos con un FPU superior a 50, aunque una ropa de algodón puede también proporcionar una adecuada fotoproteccción(29). En cuanto a las sombras, reducen de forma significativa la exposición al sol, si bien hay que tener en cuenta la radiación UV reflejada por las superficies como la arena, la hierba o el agua, que refleja el 25% de la radiación que recibe, y sobre todo la nieve, que refleja el 90%.
Fotoprotectores
La piel de los adolescentes es más grasa y, por tanto, el uso de fotoprotectores demasiado oclusivos puede favorecer
el acné
En cuanto al uso de fotoprotector, no existen unas recomendaciones diferentes de las de los adultos. Utilizar fotoprotectores con al menos un FPS 30 o superior, con una fotoprotección equilibrada en el UVA (en el etiquetado debe aparecer la palabra UVA dentro de un círculo). En caso de fototipos claros (1 a 3) se recomienda un FPS 50 +.
En general, la piel de los adolescentes es más grasa y, por tanto, el uso de fotoprotectores demasiado oclusivos puede favorecer el acné; en estos casos se recomiendan fotoprotectores especialmente diseñados para pieles con tendencia acneica. Otro factor a considerar es la aparición de hiperpigmentaciones como lesión residual del acné, en cuyo caso el uso de fotoprotectores que contenga filtros que protejan de la luz azul (óxido de hierro, Triasorb) es recomendable.
Se recomienda utilizar fotoprotector con FPS 50 o incluso 100 en situaciones de exposición solar intensa, especialmente en deportes de nieve o acuáticos en verano
Un aspecto importante en este grupo de edad es la práctica de deportes al aire libre en los cuales la fotoprotección es fundamental; sin embargo, la incomodidad de los mismos (escozor de ojos, sensación pegajosa, manos resbaladizas) puede llevar a rechazar su uso. En este sentido una revisión reciente sobre fotoprotección en el deporte, en la que hemos participado, recomienda utilizar fotoprotector con FPS 50 o incluso 100 en situaciones de exposición solar intensa, especialmente en deportes de nieve o acuáticos en verano. También se deben elegir fotoprotectores resistentes al agua y al sudor(30).
Los fotoprotectores deben aplicarse en cantidad abundante, algo que puede ser complicado ya que cosméticamente puede no ser agradable, deben reaplicarse cada 2 horas, aunque cada vez la remanencia de algunos fotoprotectores es mayor.
Se deben evitar los fotoprotectores que contengan dióxido de titanio nanosomado en forma de spray por el riesgo de inhalación de estas nanoparticulas
Se deben evitar los fotoprotectores que contengan dióxido de titanio nanosomado en forma de spray por el riesgo de inhalación de estas nanoparticulas.
Hay fotoprotectores que pueden absorberse a través de la piel; entre los más polémicos, para las personas y el medio ambiente, está la oxibenzona
En cuanto a la seguridad de algunos filtros, tanto para los individuos como para el medio ambiente, es un tema de debate en la actualidad. Existen estudios que han demostrado que los fotoprotectores pueden absorberse a través de la piel; entre los filtros más polémicos, tanto para las personas como para el medio ambiente, se encuentra la oxibenzona(31). No obstante, las evidencias que tenemos en la actualidad avalan que los fotoprotectores son eficaces y seguros y se investiga para que sean más eficientes y sostenibles.
Fotoprotección oral
En cuanto a los fotoprotectores orales, se basan principalmente en sustancias antioxidantes entre las que se incluye la vitamina C, E, las sinecatequinas del té verde o el Polipodium leucotomus, además de la vitamina D, entre otros. No existen estudios específicos en adolescentes, y parecen ser útiles en las personas con fototipos claros y en pacientes con fotodermatosis, como la erupción solar polimorfa, pero siempre asociados a los fotoprotectores tópicos(32).
Fotoprotección y vitamina D
Se ha comprobado que utilizando el fotoprotector en las condiciones habituales no influye negativamente en los niveles de vitamina D
Por último, un aspecto controvertido de la fotoprotección es el riesgo de provocar un déficit de vitamina D, dado el papel relevante de la radiación UVB en la síntesis cutánea de vitamina D. No hay estudios específicos en adolescentes, pero tanto en adultos como en niños se ha comprobado que utilizando el fotoprotector en las condiciones habituales no influye negativamente en los niveles de vitamina D(33). La cantidad de exposición solar necesaria para sintetizar vitamina D depende del fototipo, la hora del día, el mes del año y la latitud(34). Sin embargo, evitar la exposición solar o usar ropas fotoprotectoras sí puede comprometer esta síntesis.
Conclusiones
Los trastornos de la pigmentación son un motivo de consulta dermatológica muy frecuente en los adolescentes. Si bien los nevus melanocíticos son el tipo de lesión que más dudas presenta, especialmente por su potencial riesgo de malignidad, existen otros trastornos de la pigmentación que el pediatra debe conocer. Los mosaicismos pigmentarios, las manchas café con leche, los lentigos o incluso el nevus de Becker, hay que considerarlos como posibles marcadores cutáneos de enfermedades y síndromes más complejos.
Los adolescentes necesitan una fotoprotección adaptada a su tipo de piel, a sus gustos cosméticos y a las actividades que realizan para conseguir una buena adherencia
La mejor forma para prevenir los cambios en todas estas lesiones pigmentadas es la práctica de la fotoprotección. El uso de ropas, gorros, gafas solares, como evitar las horas centrales del día y consultar el índice ultravioleta diario son elementos fundamentales para una exposición saludable al sol. Las cremas fotoprotectoras son un complemento eficaz y muy importante a lo anterior; estos fotoprotectores han de ser cada vez más personalizados, adaptándose al fototipo, a la actividad en exterior, a las enfermedades dermatológicas si las hubiese, y por supuesto a la edad. Así, los fototipos más bajos, con mucho riesgo de quemadura solar, han de usar un elevado FPS (50+); sin embargo, para los fototipos más altos, que se broncean fácilmente, un FPS 30 puede ser suficiente, pero necesitarán tener una eficaz fotoprotección frente a la radiación UVA y azul para evitar pigmentaciones indeseadas. Los adolescentes necesitan una fotoprotección adaptada a su tipo de piel, a sus gustos cosméticos y a las actividades que realizan, solo así se conseguirá una buena adherencia y, en definitiva, una prevención eficaz de la quemadura solar y del cáncer cutáneo a largo plazo.
Tablas y figuras
Figura 1. Imágenes clínicas y dermatoscópicas
de nevus
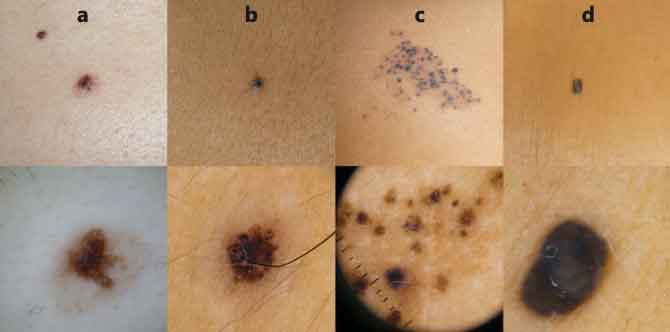
a) Nevus displásico, con retículo pigmentado atípico a la dermatoscopia; b) Nevus de Spitz, con patrón dermatoscópico en estallido de estrellas; c) Nevus spilus; d) Nevus azul, con patrón azul homogéneo a la dermatoscopia.
Figura 2. Nevus congénito, con aumento de pelo terminal e islas de mayor pigmento en su interior
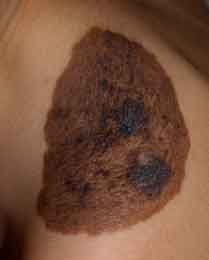
Figura 3. Léntigos y efélides en zonas fotoexpuestas en niña con xeroderma pigmentoso
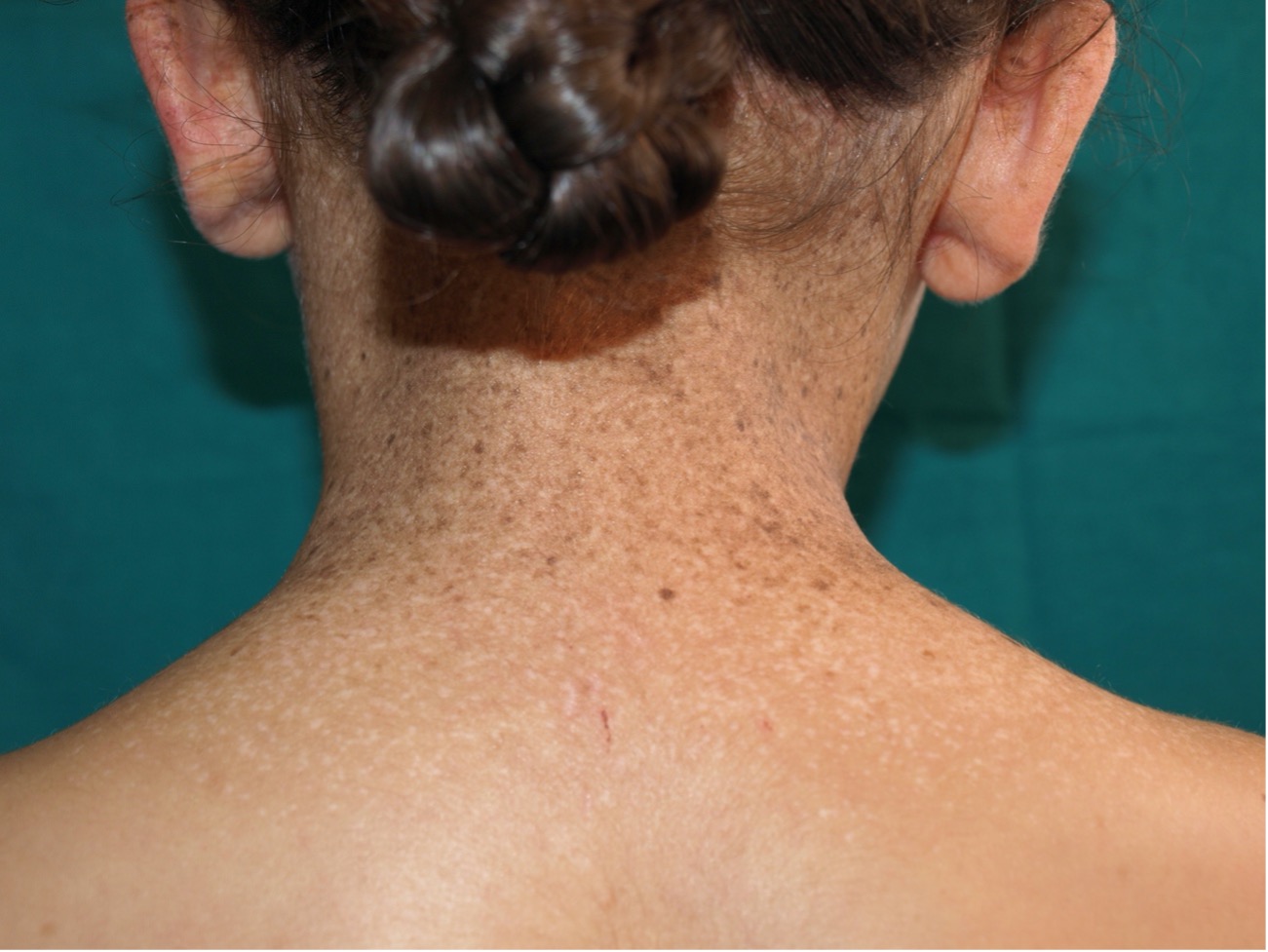
Figura 4. Nevus de Becker
Bibliografía
1. Schaffer JV. Update on melanocytic nevi in children. Clin Dermatol. 2015;33(3):368-386.
2. Levy R, Lara-Corrales I. Melanocytic Nevi in Children: A Review. Pediatr Ann. 2016;45(8):e293-298.
3. Westhafer J, Gildea J, Klepeiss S, Clarke L, Helm K. Age distribution of biopsied junctional nevi. J Am Acad Dermatol. 2007;56(5):825-827.
4. Aguilera P, Puig S, Guilabert A, Julià M, Romero D, Vicente A, et al. Prevalence study of nevi in children from Barcelona. Dermoscopy, constitutional and environmental factors. Dermatology. 2009;218(3):203-214.
5. Ferrara G, Zalaudek I, Savarese I, Scalvenzi M, Argenziano G. Pediatric atypical spitzoid neoplasms: a review with emphasis on “red” (‘spitz’) tumors and “blue” (‘blitz’) tumors. Dermatology. 2010;220(4):306-310.
6. Brown A, Sawyer JD, Neumeister MW. Spitz Nevus: Review and Update. Clin Plast Surg. 2021;48(4):677-686.
7. Nedelcu R, Dobre A, Brinzea A, Hulea I, Andrei R, Zurac S, et al. Current Challenges in Deciphering Sutton Nevi-Literature Review and Personal Experience. J Pers Med. 2021;11(9):904.
8. Loh J, Kenny P. Meyerson phenomenon. J Cutan Med Surg. 2010;14(1):30-32.
9. Vaidya DC, Schwartz RA, Janniger CK. Nevus spilus. Cutis. 2007;80(6):465-468.
10. Farabi B, Akay BN, Goldust M, Wollina U, Atak MF, Rao B. Congenital melanocytic naevi: An up-to-date overview. Australas J Dermatol. 2021;62(2):e178-e191.
11. Lanna C, Tartaglia C, Caposiena Caro RD, Sara Mazzilli S, Ventura A, Bianchi L, et al. Melanocytic lesion in children and adolescents: an Italian observational study. Sci Rep. 2020;10(1):8594.
12. Jen M, Murphy M, Grant-Kels JM. Childhood melanoma. Clin Dermatol. 2009;27(6):529-536.
13. Merkel EA, Mohan LS, Shi K, Panah E, Zhang B, Gerami P. Paediatric melanoma: clinical update, genetic basis, and advances in diagnosis. Lancet Child Adolesc Health. 2019;3(9):646-654.
14. Anderson S. Café au Lait Macules and Associated Genetic Syndromes. J Pediatr Health Care. 2020;34(1):71-81.
15. Torchia D. Becker nevus syndrome: A 2020 update. J Am Acad Dermatol. 2021;85(2):e101-e103.
16. Valdés F, Ginarte M, Toribio J. Melanocitosis dérmicas. Actas Dermosifiliogr. 2001;92(9):379-388.
17. Franceschini D, Dinulos JG. Dermal melanocytosis and associated disorders. Curr Opin Pediatr. 2015;27(4):480-485.
18. Kromann AB, Ousager LB, Ali IKM, Aydemir N, Bygum A. Pigmentary mosaicism: a review of original literature and recommendations for future handling. Orphanet J Rare Dis. 2018;13(1):39.
19. Radiation: Ultraviolet (UV) radiation and skin cancer. Accessed March 22, 2022. https://www.who.int/news-room/questions-and-answers/item/radiation-ultraviolet-(uv)-radiation-and-skin-cancer.
20. Dennis LK, Vanbeek MJ, Beane Freeman LE, Smith BJ, Dawson DV, Coughlin JA. Sunburns and risk of cutaneous melanoma: does age matter? A comprehensive meta-analysis. Ann Epidemiol. 2008;18(8):614-627.
21. Ghazi S, Couteau C, Paparis E, Coiffard LJM. Interest of external photoprotection by means of clothing and sunscreen products in young children. J Eur Acad Dermatol Venereol. 2012;26(8):1026-1030.
22. Sirera Rus MP, Ipiens Serrate JR, Ferrer Gracia E, Teruel Melero P, Gállego Diéguez J, Gilaberte Y. Effectiveness of SolSano Program on Sun Protection Habits, Knowledge, and Attitudes Among University Students. Actas Dermosifiliogr (Engl Ed). 2020;111(5):381-389.
23. Andreola GM, Carvalho VO de, Huczok J, Cat MNL, Abagge KT. Photoprotection in adolescents: what they know and how they behave. An Bras Dermatol. 2018;93(1):39-44.
24. Fernández Morano T, De Troya Martín M, Rivas-Ruiz F, Blázquez Sánchez N, Del Boz González J, Fernández Peñas P, et al. Behaviour, attitudes and awareness concerning sun exposure in adolescents on the Costa del Sol. Eur J Dermatol. 2014;24(1):85-93.
25. Blázquez Sánchez N, Rivas Ruiz F, Bueno Fernández S, Fernández Morano MT, Arias-Santiago S, Rodríguez Martí-nez A, et al. Photoprotection habits, attitudes and knowledge among school communities in the Costa del sol (Spain).
Eur J Public Health. 2021;31(3):508-514.
26. Strome A, Herbert K, Walsh K, Lamberg O, Waselewski ME, Chang T. Assessment of Sun Protection Knowledge and Behaviors of US Youth. JAMA Netw Open. 2021;4(11):e2134550.
27. Sim WMB, Zeng MX, Rojas-Garcia A. The effectiveness of educational programmes in promoting sun protection among children under the age of 18: a systematic review and meta-analysis. J Eur Acad Dermatol Venereol. 2021;35(11):2154-2165.
28. Pettigrew S, Parnell A, Strickland M, Neale R, Lucas R. The Potential of Ultraviolet Radiation Meters in Secondary Schools as a Sun Protection Intervention Mechanism for Adolescents. Int J Environ Res Public Health. 2020;17(4):E1137.
29. Aguilera J, de Gálvez MV, Sánchez-Roldán C, Herrera-Ceballos E. New advances in protection against solar ultraviolet radiation in textiles for summer clothing. Photochem Photobiol. 2014;90(5):1199-1206.
30. Gilaberte Y, Trullàs C, Granger C, de Troya-Martín M. Photoprotection in Outdoor Sports: A Review of the Literature and Recommendations to Reduce Risk Among Athletes. Dermatol Ther (Heidelb). 2022;12(2):329-343.
31. Schneider SL, Lim HW. Review of environmental effects of oxybenzone and other sunscreen active ingredients. J Am Acad Dermatol. 2019;80(1):266-271.
32. Parrado C, Philips N, Gilaberte Y, Juarranz A, González S. Oral Photoprotection: Effective Agents and Potential Candidates. Front Med (Lausanne). 2018;5:188.
33. Narbutt J, Philipsen PA, Lesiak A, Sandberg Liljendahl T, Segerbäck D, Heydenreich J, et al. Children sustain high levels of skin DNA photodamage, with a modest increase of serum 25-hydroxyvitamin D3 , after a summer holiday in Northern Europe. Br J Dermatol. 2018;179(4):940-950.
34. Aguilera J, de Gálvez MV, Aguilera P, de Troya-Martín M, Gilaberte Y, del Grupo Español de Fotobiología de la AEDV. Recommendations on Sun Exposure and Photoprotection Following Easing of the COVID19 Pandemic Lockdown: Spanish Photobiology Group of the Spanish Academy of Dermatology and Venerology (AEDV). Actas Dermosifiliogr (Engl Ed). 2020;111(9):799-801.