Talleres simultáneos.
Taller de urgencias en la adolescencia
Taller de urgencias en la adolescencia
I.Manrique Martínez(1), V.Sebastián Barberán(2).
(1)Pediatra. Acreditación como Especialista en Urgencias Pediátricas. Director del Instituto Valenciano de Pediatría. Valencia. (2)Pediatra. Acreditación como Especialista en Urgencias Pediátricas. Consultorio Auxiliar Arquitecto Tosla. Valencia
Adolescere 2024; XII (2): 111-128
Resumen
|
Las urgencias en la adolescencia continúan siendo un desafío para el personal sanitario. Se presentan el manejo inicial y las estrategias terapéuticas en diferentes situaciones: intoxicación, dolor torácico y crisis asmática que no mejora con el tratamiento. La mayoría de los adolescentes que acuden a urgencias suelen salir con el diagnóstico de problemas musculoesqueléticos, psicógenos, problemas respiratorios, gastrointestinales, etc. Siempre se deben descartar patologías graves para la salud del joven. Palabras clave: Urgencias; Adolescente; Intoxicación; Dolor torácico; Neumomediastino; Crisis asmática. |
Abstract
|
Emergencies in adolescence continue to be a challenge for health professionals. The initial management and therapeutic strategies in various situations are presented: intoxication, chest pain and asthmatic crisis that does not improve with treatment. Most adolescents who come to the Emergency Room usually leave with a diagnosis of musculoskeletal problems, psychogenic, respiratory, gastrointestinal problems, etc. Severe health-comprimising pathologies for the young person should always be ruled out. Key words: Emergency Room; Adolescent; Intoxication; Chest pain; Pneumomediastinum; Asthmatic crisis. |
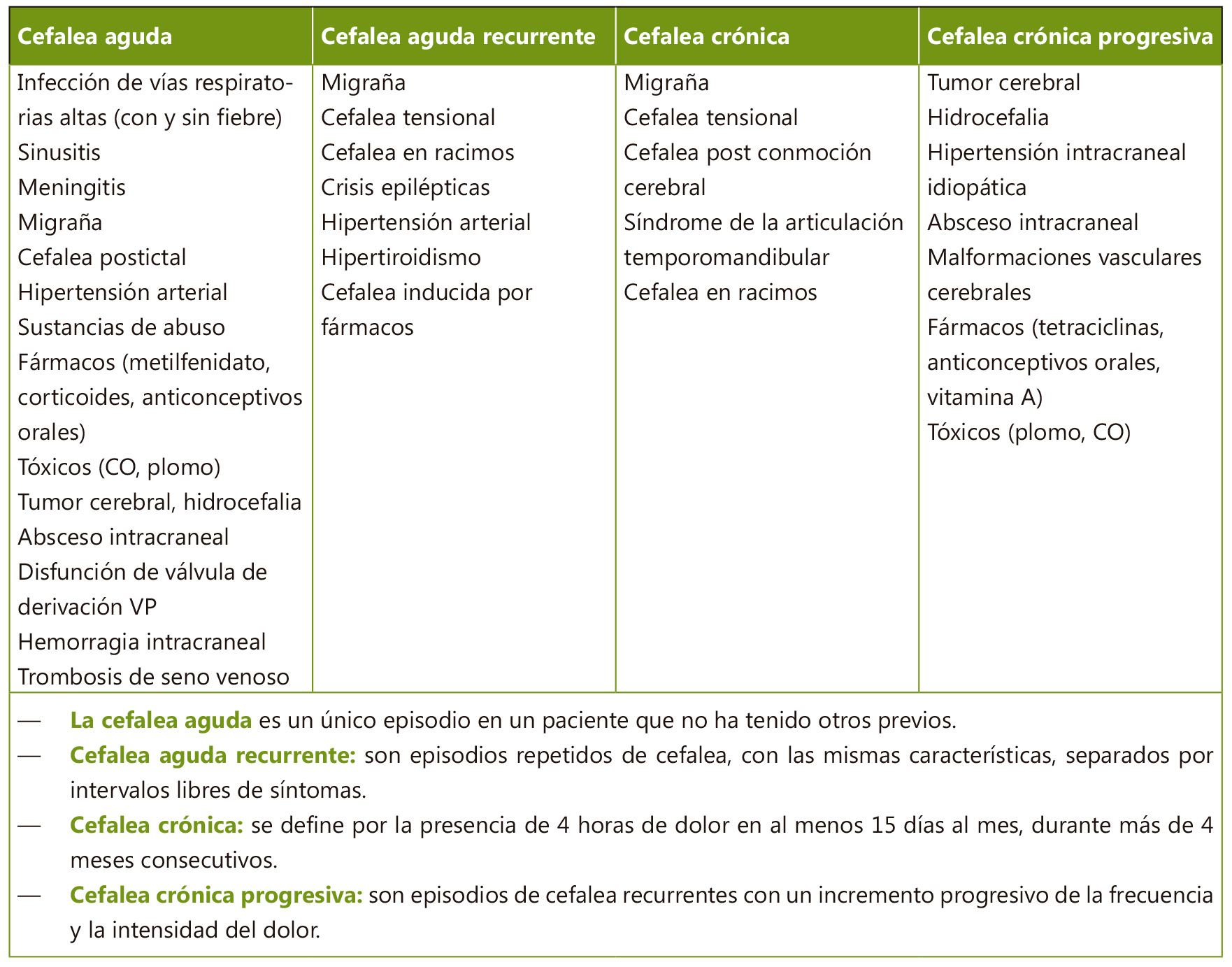
Caso 1. Niña de 14 años con palpitaciones
Niña de 14 años de edad, que es llevada por sus padres a urgencias de su CS un sábado por la mañana, pues al despertarla les ha dicho que tenía palpitaciones y que el corazón le iba muy rápido. Les cuenta que anoche tuvo una discusión con su grupo de amigos y que volvió a casa llorando. Los padres deciden llevarla al CS pues quizás necesite alguna pastillita para tranquilizarla. Llegan al mostrador y cuentan a la administrativa lo que le pasa a la niña y que por el camino la han notado un poco “adormilada”. La remiten a la pediatra que está de urgencias. Cuando la pediatra va a la sala de espera la niña está reclinada con los ojos cerrados, con aspecto ausente, y la madre hablando en voz alta a la niña mientras le dice: ¿No habrás tomado drogas, verdad?
1ª Pregunta. Con los pocos datos de que dispones hasta este momento, ¿qué valoración le darías al TEP (Triángulo de Evaluación Pediátrica)? (Figura 1).
La apariencia parece estar alterada (anormal) con lo cual se catalogaría inicialmente como una Disfunción SNC.
2ª Pregunta. Después de valorar el TEP y por lo visto y oído, ¿qué harías con esta niña?
- La dejo un rato en la sala de espera y cuando termine con los otros cuatro niños que tengo pendientes, la vuelvo a “ver”.
- Que se marche a casa, pues lo que tiene es un “colocón” y se le pasará durmiendo.
- Por la historia que me cuentan no me queda claro que le pasa y me la quedo para explorarla inmediatamente.
- Que se marchen al hospital de referencia para que allí la hagan analíticas.
Respuesta: La respuesta correcta es la c). Siguiendo la sistemática de Evaluación del TEP realizamos ahora la comprobación de los signos vitales FC 140 lpm; FR 15 rpm;Tª 39,0ºC axilar; Sat O2: No funciona el aparato; T. Arterial: 150/9,5; Peso 35 kgs (P 10).
3ª Pregunta. ¿Alguna de estas constantes te parece alterada?
Respuesta: La frecuencia cardíaca está elevada para su edad 140 lpm (rango edad 80-100 lpm) así como la temperatura 39,0ºC axilar, al igual que la tensión arterial: 150/9,5 (rango edad 110/70).
Continuamos con evaluación de los ABC y en la exploración observamos que la niña presenta una piel seca, caliente y está roja. La mucosa oral está muy seca. Midriasis.
La paciente indica que sigue con las palpitaciones y que el corazón le va muy rápido. Y además que lleva con retención urinaria desde hace más de 4 horas (ella indica que es muy “meona”). Sigue somnolienta, quizás más que al verla en la sala de espera y la respiración es algo más baja (13-14 rpm).
Tras la exploración a la pediatra se le plantean algunas dudas, ¿pero qué le pasa a esta adolescente? Por todo lo observado hasta ese momento, esta niña presenta signos y síntomas anticolinérgicos y con lo cual dirige sus preguntas en este sentido.
Tras unos minutos haciéndole preguntas dirigidas, finalmente, la adolescente dice que ha tomado hace unas 5 horas seis pastillas de las que toma su abuela para la depresión (ADT – Amitriptilina 50 mgrs comprimido oral) ya que cuando se las toma luego duerme muy bien, y ella con el disgusto que tenía tras romper con sus amigas lo único que quería es dormir y no pensar.
4ª Pregunta. Con esta dosis, ¿estamos en dosis de riesgo de complicaciones?
- Si
- No
Respuesta: Si. Se señala que con dosis inferiores a 3 mg/kg es poco probable que sean fatales o causen graves complicaciones, pero están descritas a dosis de 8-10 mgr/kgr y una dosis que puede ser letal es de 15-20 mg/kg (niños). La dosis tóxica es 10 veces mayor que la terapéutica.
¿Cuánto tomó nuestra niña? Dosis ingerida: 6 comprimidos x 50 mgrs= 300 mgrs.
¿Dosis de riesgo? 8-10 mgr x 35 kgrs= 280-350 mgrs. Mortalidad 15 mgrs x 35 kgrs= 525 mgrs.
Desde hace muchos años la mayoría de los expertos consideran que “cualquier niño que tenga ingestión de ATC debe ser ingresado en hospital”.
5ª Pregunta. Una vez conocido el agente causal, ¿qué tratamiento pautarías?
- Inducir inmediatamente el vómito
- Descontaminación gastrointestinal con carbón activado
- Flumazenil IV
- Ninguna de ellas
Inducir el vómito no tiene utilidad en este caso y puede ser deletéreo en un paciente que está con alteración de la conciencia y riesgo de broncoaspiración
Respuesta correcta: b). a) Inducir el vómito no tiene utilidad y no está indicado. Puede considerarse deletéreo en un paciente que está con alteración de la conciencia y riesgo de broncoaspiración. b) Descontaminación gastrointestinal con carbón activado podría considerarse durante las 6 horas posteriores a su ingesta, dado que estos fármacos enlentecen el vaciamiento gástrico. Debido a que los modelos in vitro demuestran que el carbón activado permite adsorber grandes cantidades de ADT su uso suele ser la conducta más generalizada al momento de contemplar las medidas de descontaminación. En ingestas potencialmente letales su utilización es habitual. c) El antídoto flumazenil no se recomienda en pacientes que hayan ingerido antidepresivos tricíclicos, ya que puede desencadenar crisis comiciales.
El flumazenil no se recomienda en pacientes que hayan ingerido antidepresivos tricíclicos, ya que puede desencadenar crisis comiciales
Mientras estamos valorando el posible tratamiento la niña presentó de forma súbita convulsiones que empezaron a ser tratadas con Benzodiacepinas IV dado que es la primera elección para el control de las convulsiones asociadas a toxicidad. La segunda línea es el fenobarbital (15 mg/kg) y repetir a 5 mg/kg si las convulsiones continúan.
Tras la recuperación de las convulsiones presenta inmediatamente hipotensión severa seguida de alteración del ritmo cardiaco y desvanecimiento brusco. Parece que no respira y no le encontramos el pulso. El ECG mostró el ritmo de Figura 2 (en el monitor del desfibrilador que tenemos en el Centro de Salud).
6ª Pregunta. ¿Ante qué ritmo nos encontramos?
- Taquicardia sinusal
- Taquicardia ventricular
- Taquicardia supraventicular
- Fibrilación ventricular
Respuesta: b) Taquicardia ventricular. Se confirma que la niña no tiene pulso y no respira, es decir, nos encontramos ante una parada cardiorrespiratoria.
Los ADT presentan tanto manifestaciones neurológicas como cardiovasculares, sobre todo entre 2-6 horas post ingesta
Recordar que los ADT presentan tanto manifestaciones neurológicas como cardiovasculares, sobre todo entre 2-6 horas post ingesta con hallazgos como taquicardia sinusal, TV/Fibrilación ventricular, complejos QRS > o = a 100 ms.
Ante esta situación se inician manobras de RCP siguiendo el algoritmo de parada cardiorrespiratoria por ritmo desfibrilable, en nuestro caso TV sin pulso.
7ª Pregunta. ¿Qué fármacos utilizarías para revertir esta TV sin pulso?
- Adrenalina y amiodarona
- Bicarbonato, adrenalina y amiodarona
- Adrenalina y adenosina
- No requiere fármacos ya que el tratamiento es la desfibrilación y masaje cardiaco con ventilación.
Respuesta: La respuesta correcta es la b.
En este caso inicialmente se siguió el algoritmo propuesto por el Grupo Español de RCP pediátrica y neonatal para las taquicardias ventriculares sin pulso (Figura 3).
Se dieron tres descargas a 4 J/kg seguida cada una de ellas de 2 minutos de RCP (ventilación+O2 con bolsa resucitadora, mascarilla facial y guedel) y tras la tercera dosis se puso una dosis de Adrenalina (3,5 ml de la dilución 1/10.000) y Amiodarona (175 mgs).
Adrenalina 1/1.000: 1 ampolla = 1ml = 1mg vía intravenosa o intraósea.
Niños hasta la pubertad: 0,1 ml/kg (dilución 1/10.000 ) 1 ampolla + 9 ml agua bidestilada o suero fisiológico.
Ante la ausencia de respuesta la pediatra realizó un repaso rápido de las causas reversibles (4Hs y 4 Ts) que podrían ser el origen de la falta de respuesta. En nuestro caso era por un tóxico (antidepresivo tricíclico), que requiere de la administración de bicarbonato para la resolución de la arritmia.
No hay evidencias para administrar bicarbonato sódico de forma rutinaria durante la RCP. Se puede valorar su administración en el niño con parada cardiaca prolongada y/o con acidosis metabólica severa. También puede administrarse en casos de inestabilidad hemodinámica con hiperpotasemia y en el tratamiento de la intoxicación por antidepresivos tricíclicos.
A nuestra paciente se le administró bicarbonato sódico 1 molar (1 ampolla = 10 ml = 10 mEq) diluida al 1/2 en agua bidestilada o suero fisiológico).
Dosis: 1 mEq/kg (1 ml/kg) + 1 ml/kg de SSF o agua destilada: 35 ml bicarbonato + 35 ml de SSF.
Tras su administración se produjo una recuperación del pulso central y de los signos vitales (respiración, movimientos, tos, etc). El ritmo cardiaco bajo a 100 lpm. La niña recuperó la consciencia.
Se realizó trasporte en SAMU medicalizado al hospital de referencia en donde fue ingresada en UCI, siendo dada de alta del hospital 48 horas más tarde. Remitida posteriormente a consultas externas de psiquiatría.
Intoxicación por antidepresivos tricíclicos
Introducción
Los antidepresivos tricíclicos —entre otros, amitriptilina, desipramina, dibenzepina, doxepina, imipramina, clomipramina u opipramol— son inhibidores inespecíficos de la recaptación de monoaminas (ATC N 06 AA). Presentan una fuerte actividad anticolinérgica y adrenérgica, inhiben los receptores α-adrenérgicos y la recaptación de noradrenalina, serotonina y dopamina. Poseen acción estabilizadora de membrana.
Se utilizan principalmente en psiquiatría para el tratamiento de los síndromes depresivos, trastornos de estrés postraumático, trastornos hipercinéticos y enuresis nocturna en niños. Los efectos clínicos en las intoxicaciones se deben a la inhibición de los canales rápidos de sodio en el miocardio y al efecto inhibidor sobre los receptores muscarínicos, α1-adrenérgicos, GABAA y H1.
Tras las benzodiacepinas, los antidepresivos tricíclicos constituyen la segunda causa más frecuente de intoxicación medicamentosa en nuestro medio
Tras las benzodiacepinas, los antidepresivos tricíclicos constituyen la segunda causa más frecuente de intoxicación medicamentosa en nuestro medio, y la que con mayor frecuencia requiere ingreso en una Unidad de Cuidados Intensivos(1). Los ADT como agentes únicos de intoxicación medicamentosa, son la 2ª causa de muerte en menores de 6 años y la 3ª en adultos(6).
El año 2009 en EE.UU. se registraron 1.158 muertes por todo tipo de tóxicos y exposiciones.
El 15 % de ellas fue por ingesta de medicamentos antidepresivos tricíclicos, inhibidores selectivos de la recaptación de serotonina, benzodiacepinas, antipsicóticos y analgésicos opiáceos(2). En estudios en EE.UU. en 2019, los antidepresivos fueron la cuarta sustancia reportada por los centros de intoxicación (Gummin et al 2020) siendo las intoxicaciones por ATC y los inhibidores de la monoamino oxidasa los de la tasa más alta de morbimortalidad. Entre los medicamentos para la depresión la amitriptilina en particular fue responsable de dos tercios de todas las exposiciones por ATC y un 39,5 % de las muertes (Nelson y Spyker 2017).
Clínica
En fases iniciales puede presentar hipertensión arterial apareciendo rápidamente hipotensión (signo de complicación). Evoluciona a convulsiones (10-20 % de los casos), coma y arritmias mayores
El inicio es precoz habitualmente inician entre 30-40 minutos después de la ingesta, pero pueden ser más tardíos debido al retraso del vaciado gastrointestinal secundario al efecto anticolinérgico(5). Un periodo de 8-12 h sin toxicidad suele excluir una toxicidad importante. Inicialmente, síndrome anticolinérgico (taquicardia, midriasis, sequedad de mucosas, retención urinaria, alucinaciones y rubor). En fases iniciales puede presentar hipertensión arterial apareciendo rápidamente hipotensión (signo de complicación). Evoluciona a convulsiones (10-20 % de los casos), coma y arritmias mayores. Toxicidad de SNC: depresión, letargia y alucinaciones. Coreoatetosis, mioclonías, convulsiones(3). Otras manifestaciones clínicas incluyen hipertermia, midriasis, mucosas secas, retención urinaria y disminución del peristaltismo(7).
Los efectos cardiovasculares, son los principales responsables de la morbilidad y mortalidad en los pacientes intoxicados por ATC. El signo más común es la taquicardia sinusal (Foulke, 1995), la cual ocurre en el 70 % de los pacientes sintomáticos, y se debe al efecto anticolinérgico y la inhibición de la recaptación de noradrenalina (Thanacoody & Thomas, 2005). Asociado a esto, los efectos más graves asociados a los ATC se producen por su efecto en el enlentecimiento de la despolarización del potencial de acción por el bloqueo de los canales de sodio en el sistema His-Purkinje y el resto del miocardio. Por lo anterior, también se produce un retraso en la repolarización y prolongación del complejo QRS y del intervalo QT, lo que predispone a distintos tipos de arritmias, especialmente ventriculares, como es la prolongación del intervalo QT y eventualmente una torsión de puntas(15). La hipotensión, muchas veces refractaria, también se presenta en estos pacientes a causa del antagonismo de los receptores alfa-1 adrenérgicos y la depleción de noradrenalina (Shannon et al., 1988).
Dosis tóxica
En general se considera que dosis superiores a 5 mg/kg son dosis tóxicas, y dosis entre 10-20 mg/kg pueden dar lugar a toxicidad grave
Los ADT tienen un estrecho margen terapéutico y se han documentado serias complicaciones con dosis relativamente bajas. En general se considera que dosis superiores a 5 mg/kg son dosis tóxicas, y dosis entre 10-20 mg/kg pueden dar lugar a toxicidad grave. Se han reportado casos letales con dosis mayores de 25 mg/kg(4,5).
Basado en lo anterior se ha propuesto que la dosis tóxica mínima para ADT sea: 5 mg/kg con excepciones de los siguientes medicamentos (desipramina, nortriptilina, trimipramina y protriptilina) en donde se considerará que la dosis tóxica mínima sea: 2,5 mg/kg(5,8).
Estudios complementarios
La utilidad de medir la concentración de ADT en sangre no es buena, debido a que valores muy bajos pueden estar presentes en pacientes muy graves, esto depende del momento de la toma, la cantidad ingerida del antidepresivo y la aplicación de las medidas de descontaminación(5). Sin embargo, los estudios que permiten determinar los niveles en sangre de ADT, pueden ser de utilidad para confirmar el diagnóstico ante un paciente con cuadro clínico compatible y etiología no clara(9).
Otros exámenes que se deberán solicitar dependen del contexto clínico del paciente. Si presenta alteración de la conciencia sin una causa clara, se deberán solicitar electrolitos, glucemia, función renal, transaminasas, hormonas tiroideas, TAC de cráneo y gasometría. De esta manera se planteará la posibilidad de diagnósticos diferenciales.
Manejo en urgencias
En todo paciente que ingrese al servicio de URG con sospecha de intoxicación por antidepresivos tricíclicos se procurará la monitorización de los signos vitales y la vigilancia electrocar-diográfica continua debido a las complicaciones cardiovasculares asociadas
En todo paciente que ingrese al servicio de urgencias con sospecha de intoxicación por antidepresivos tricíclicos se procurará la monitorización de los signos vitales y la vigilancia electrocardiográfica continua debido a las complicaciones cardiovasculares asociadas. Se considerará establecer la protección de la vía aérea definitiva si hay marcada alteración de la conciencia (Glasgow menor o igual a 8) o deterioro rápidamente progresivo del estado de conciencia, dado que en este escenario es muy probable que se pierdan los reflejos de protección de la vía aérea, y se genere neumonía aspirativa, sobre todo cuando se usan medidas de descontaminación como el lavado gástrico o el uso de carbón activado(10).
Medidas de descontaminación
En la intoxicación por ADT, contemplar la inducción del vómito no tiene utilidad y puede considerarse deletéreo en un paciente que puede cursar con alteración del estado de conciencia y riesgo de bronco aspiración(11).
En general se considera que dosis superiores a 5 mg/kg son dosis tóxicas, y dosis entre 10-20 mg/kg pueden dar lugar a toxicidad grave. Ya que estos fármacos enlentecen el vaciamiento gástrico(12). Debido a que los modelos in vitro demuestran que el carbón activado permite adsorber grandes cantidades de ADT su uso suele ser la conducta más generalizada al momento de contemplar las medidas de descontaminación. La dosis de carbón activado es de 0,5-1 g/kg, con un máximo de 50 g/kg(16).
Tratamiento
En el paciente deprimido con sospecha de consumo concomitante de benzodiacepinas no se recomienda el uso de flumazenil ya que esto puede desencadenar la aparición de convulsiones por ADT(6).
Depresión cardíaca: se ha de iniciar tratamiento con bicarbonato y, si persiste, administrar drogas inotrópicas. Existen estudios en animales que sugieren que la terapia más efectiva es la administración de adrenalina y bicarbonato sódico simultáneamente (vías diferentes)
Aproximadamente el 10-30 % de los pacientes con sobredosis por ATC presentan convulsiones, en los cuales los benzodiacepinas son la primera línea de terapia. Para el control de las convulsiones en el paciente con intoxicación con ADT se recomienda el uso de diazepam 5 a 10 mg IV (niños dosis 0.2-0.5 mg/kg) y repetir cada 5 minutos si es necesario(7). Se debe anotar que, aunque la fenítoina no se ha comparado en estudios controlados y aleatorizados contra las benzodiacepinas en pacientes con sobredosis de ADT, la evidencia disponible indica que el beneficio del uso de la fenítoina en ese contexto sólo proviene de estudios de casos esporádicos. Sin embargo, como existen dudas con respecto a la seguridad de este medicamento en pacientes con este tipo de intoxicación, su uso se debería evitar(13).
Depresión cardíaca: se ha de iniciar tratamiento con bicarbonato y, si persiste, administrar drogas inotrópicas. Existen estudios en animales que sugieren que la terapia más efectiva es la administración de adrenalina y bicarbonato sódico simultáneamente(4), si se utilizara esta pauta siempre hay que recordar que estas deberán ser administradas por vías diferentes dado que la adrenalina precipita con el bicarbonato. El bicrbonato se administra a razón de 1-2 mEq/kg peso IV en la primera hora, pudiendo repetir dosis para mantener un pH aproximado de 7,45 a 7,55, dejando una perfusión de Bi 1/6 M para 24 horas como mantenimiento. En general se han publicado diversos estudios que han reportado efectos benéficos como resolución de la prolongación del complejo QRS, corrección de la hipotensión y reversión exitosa de arritmias así como retorno a la circulación espontánea después del colapso cardiovascular. La meta del pH es llegar a valores entre 7,45-7,55(13).
Sulfato de magnesio: el sulfato de magnesio se ha indicado en casos en los que el paciente cursa con arritmias secundarias a la intoxicación con ADT y no han resuelto con las medidas iniciales. Sin embargo aún no hay estudios comparativos de calidad que permitan definir su eficacia frente a otros antiarrítmicos.
Lidocaína y fenitoína se recomienda usar estos medicamentos en el contexto de un paciente con intoxicación por ADT asociado a cardiotoxicidad (arritmias e hipotensión) refractaria al manejo con bicarbonato de sodio o solución hipertónica, o en situaciones en las cuales el uso de estos medicamentos pueda ser contraproducente (alcalosis e hipernatremia)(5).
Algoritmo tratamiento de la taquicardia ventricular sin pulso. Se utilizará el recomendado por el GERCPPYN (Figura 3). No existen evidencias para administrar bicarbonato de forma rutinaria, motivo por el cual ya quedó fuera del algoritmo, con la excepción de paciente con hiperpotasemia o en sobredosis por antidepresivos tricíclicos (como ocurrió en nuestro caso clínico).
Conclusiones
Conocer los mecanismos de acción, metabolismo, toxicidad e interacciones de los psicofármacos permite entender la fisiopatología de la intoxicación por estas sustancias
Conocer los mecanismos de acción, metabolismo, toxicidad e interacciones de los psicofármacos permite entender la fisiopatología de la intoxicación por estas sustancias. La evaluación clínica detallada facilita detectar síntomas y signos que conforman el tipo de proceso. Reconocerlo ayudará a sospechar cual clase de fármaco es el causante y la severidad de la intoxicación, para tratarla precozmente o determinar a quiénes se debe observar o derivar a centros de alta complejidad; pacientes asintomáticos con estado leve de intoxicación requieren ingreso en UCIP con monitorización. Se deberá solicitar evaluación por parte del servicio de psiquiatría si la ingestión fue intencionada.
Tablas y figuras caso 1
Tabla I. Posible situación del paciente tras evaluación del TEP
Figura 1. Triángulo de Evaluación Pediátrica (TEP)
Fuente: Dieckmann RA, Brownstein D, Gausche-Hill M, eds. Pediatric Education for Prehospital Professionals: PEPP Textbook. Sudbury, MA: Jones & Bartlett Publishers; 2000.
Figura 2. Ritmo electrocardiográfico en pantalla del monitor
Fuente: Elaboración propia.
Figura 3. Actuación ante un ritmo desfibrilable
Fuente: Grupo Español de RCP Pediátrica y Neonatal para las Taquicardias Ventriculares sin pulso.
Caso clínico 2. Dolor torácico
La etiología más frecuente del dolor torácico en edad pediátrica se relaciona con la pared torácica (costocondritis, traumatismo, dolor muscular) o con enfermedades respiratorias que cursan con tos
El dolor torácico (DT) supone el 0,25-1 % de las visitas a los servicios de urgencias pediátricas, siendo más frecuente en el periodo prepuberal y en la adolescencia. Aunque en la gran mayoría de casos su etiología es benigna, es motivo de preocupación y angustia en el adolescente y las familias. Una historia clínica en profundidad y la exploración física suelen ser suficientes para diferenciar los casos banales de aquellos que pueden deberse a enfermedades más graves(1). El diagnóstico diferencial es muy amplio, no existiendo guías estandarizadas para su abordaje clínico y diagnóstico. La patología cardiaca es la que plantea mayor preocupación y riesgo vital. Aunque la lista de causas es extensa, la etiología más frecuente del dolor torácico en edad pediátrica se relaciona con la pared torácica (costocondritis, traumatismo, dolor muscular) o con enfermedades respiratorias, especialmente aquellas que cursan con tos. El origen cardiovascular es raro. El diagnóstico más habitual, al alta de los servicios de urgencias, es el dolor torácico inespecífico o idiopático(2).
Anamnesis: Varón de 12 años que acude a su centro de salud por presentar un episodio de tos, disnea, odinofagia y vómitos (en dos ocasiones), asocia en la última hora dolor torácico retroesternal.
Antecedentes personales: Asma bronquial tratado con inmunoterapia y corticoides inhalados. La madre refiere que ha realizado tratamiento de rescate en domicilio y al no mejorar clínicamente acude para ser valorado por su pediatra.
Exploración física: Consciente, buena coloración piel y mucosas. Constantes: FR 32 rpm, FC: 140 lpm. TA: 90/57. Sat O2: 94 %. Peso 30 kg. Auscultación CP: disminución de murmullo vesicular, tiraje supraesternal. Tonos cardiacos normales. Pulmonary Score: 6 con Sat O2: 94 %. Moderado.
Se administra nebulización 0,15 mg/kg salbutamol (máx. 5 mg) + 500 μg de bromuro de ipratropio, cada 20 minutos hasta 3 dosis + 1 mg/kg de predinisolona. Posteriormente a la administración de la medicación comienza de manera súbita con sudoración profusa y dolor centrotorácico retroesternal de alta intensidad, irradiado a región cervical anterior, que empeora con el decúbito.
Presenta las siguientes constantes: TA:100/85 mmHg, Sat O2: 94%. FC: 142 lpm. FR: 42 rpm.
Exploración física: taquipneico, signos de trabajo respiratorio (tiraje subcostal, intercostal y supraesternal), con hipoventilación generalizada en ambos campos pulmonares, más marcada en el campo izquierdo, sin ruidos sobreañadidos. Dolor de tipo quemazón intenso 9/10 en región centrotorácica e irradiado a región cervical anterior derecha. Resto de la exploración: normal.
Se realiza un diagnóstico diferencial del dolor torácico en pediatría por parte del residente y su pediatra de AP: (Tabla I y II)(3).
Evolución: Ante esta situación clínica se administra analgesia para el dolor y se remite en un SAMU al hospital. A su llegada al hospital es valorado por el pediatra de guardia presentando la siguiente situación clínica: taquipneico, signos de trabajo respiratorio (tiraje subcostal, intercostal y supraesternal), con hipoventilación generalizada en ambos campos pulmonares, más marcada en el campo izquierdo, se observa una crepitación sincrónica en hemitórax izquierdo y ruidos interpretados como frote pleural.
Pruebas complementarias: Radiografía de tórax (Figura 1). Hemograma con 24.530 leucocitos, neutrófilos 82,7 %, linfocitos 11,3 %, monocitos 5 %, hemoglobina 16 mg/dl, hematocrito 34,6 %, plaquetas 345.000, PCR y procalcitonina negativas, gasometría normal, función renal y electrólitos normales. Troponina negativa con un valor de 0,007 ng/ml.
ECG: normal. El ecocardiograma se encontró dentro de límites normales, descartándose la presencia de pericarditis, derrame pericárdico u otra patología cardiaca. La Rx de tórax fue determinante para el diagnóstico: Signo de diafragma continuo: presencia de aire entre el pericardio y el diafragma. Signo de la V de Naclerio: presencia de aire entre la aorta descendente y el hemidiafragma izquierdo y el enfisema subcutáneo. (Figura 1).
Diagnóstico: Neumomediastino.
Tratamiento: Sintomático con muy buena evolución, administrándole analgésicos y recomendando reposo. El paciente se mantuvo ingresado 3 días, dándole de alta por mejoría clínica del dolor.
Discusión: El dolor torácico en los adolescentes es un motivo frecuente en urgencias, en el caso del neumomediastino, la sospecha clínica es fundamental, en algunos casos los antecedentes de asma deben hacernos sospechar, por lo que debemos incluirlo en el diagnóstico diferencial, la radiografía de tórax es junto con la clínica suficiente para el diagnóstico por sus hallazgos característicos, como el signo de la V de Naclerio o el signo de Hamman. El tratamiento inicial es conservador con analgesia y posición incorporada, suelen estar ingresados, se resuelve espontáneamente en 2 o 3 días.
Resumen: Se presenta el caso de un varón con antecedentes de asma que acude por dolor torácico de corta evolución, con sintomatología compatible de crisis asmática. El caso plantea los diagnósticos diferenciales de un cuadro de dolor torácico en un adolescente y las determinadas pruebas diagnósticas para poder llegar a un diagnóstico temprano con tratamiento adecuado.
Neumomediastino
Introducción
El término enfisema mediastínico, neumomediastino o síndrome de Hamman(5) describe la presencia de aire libre en el mediastino, fue descrito por primera vez por Louis Hamman en 1939. Tiene una mayor incidencia en varones jóvenes. Se puede asociar a crisis asmática en el 5,4 %. Presenta una clínica característica con dolor torácico retroesternal y disnea, otros síntomas como disfagia, torticolis, disfonía y el dolor abdominal, fiebre, lo que nos puede hacer pensar en una etiología infecciosa.
Manifestaciones clínicas
La manifestación clínica más frecuente de neumomediastino espontáneo es el dolor torácico de características pleuríticas, disnea, tos y odinofagia
La manifestación clínica más frecuente de neumomediastino espontáneo es el dolor torácico de características pleuríticas (54 %), seguido por disnea (39 %), tos (32 %) y odinofagia(4). En el neumomediastino secundario las manifestaciones clínicas están relacionadas con la enfermedad o condición de base.
En el examen físico los hallazgos más frecuentes son el enfisema subcutáneo de localización cervical y a nivel de fosas supraclaviculares (50 %), en otras localizaciones (32 %), el edema de tejidos blandos del cuello (14 %) y la presencia de cianosis e ingurgitación yugular(4). Durante el examen físico es importante reconocer signos específicos que orientan sobre la presencia de un neumomediastino, como es el signo de Hamman, que se describe como un crujido en la región precordial sincrónico con los latidos del corazón y que puede confundirse con un frote pericárdico y la presencia de derrame pericárdico.
Diagnóstico diferencial
Es importante realizar el diagnóstico diferencial según el origen (Tabla III).
En el diagnóstico diferencial de neumomediastino se debe considerar: neumopericardio, neumotórax, neumatocele paramediastinal y efecto Mach. La distribución del aire permite hacer la diferenciación entre neumomediastino y neumotórax medial. En el neumomediastino las colecciones de aire son múltiples, lineales y definen estructuras anatómicas mediastinales como la arteria pulmonar, la aorta, el esófago y estructuras de la vía aérea. Por otra parte, el aire mediastinal no se desplaza con los cambios de posición. En el neumopericardio se observa una imagen radiolúcida que rodea el corazón, la aorta ascendente y la arteria pulmonar, sin extenderse al arco aórtico, la tráquea y los grandes bronquios o el cuello. El Mach es un efecto retiniano que condiciona la presencia de una banda radiolúcida adyacente al contorno cardíaco, sin que se definan otros signos de neumomediastino o neumopericardio. Finalmente, es conveniente considerar la posibilidad de la coexistencia de neumomediastino y neumopericardio.
En el neumo-mediastino las colecciones de aire son múltiples, lineales y definen estructuras anatómicas mediastinales como la arteria pulmonar, la aorta, el esófago y estructuras de la vía aérea
El neumomediastino espontáneo es una patología rara en la infancia(9). En series españolas se estima una frecuencia de ingresos del 0,06 %, por lo que se considera una entidad en la que raramente se piensa ante un dolor torácico como diagnóstico diferencial. En pediatría, se ha observado un predominio en varones y una distribución bimodal por edades, con predominio en menores de 3 años y en preadolescentes.
En preadolescentes, casi nunca suele faltar en la anamnesis la práctica de algún deporte, vómitos y accesos de tos, que provocaría la rotura de alvéolos terminales como antecedente personal a la crisis. En algunas series de neumomediatismo espontáneo, aparece el uso habitual de drogas inhaladas como el crack, cannabis, éxtasis o cocaína. Esta inhalación se acompaña de un esfuerzo inspiratorio prolongado y forzado, seguido de una maniobra de Valsalva. Este antecedente se deberá tener en cuenta cuando se trate de adolescentes con esta entidad.
En algunas series de neumomediatismo espontáneo, aparece el uso habitual de drogas inhaladas como el crack, cannabis, éxtasis o cocaína. Esta inhalación se acompaña de un esfuerzo inspiratorio prolongado y forzado
Pruebas complementarias
En el electrocardiograma se observa bajo voltaje en todas las derivaciones y cambios inespecíficos tanto en la onda T como en el segmento ST. El diagnóstico de neumomediastino se basa en la identificación de aire extraluminal en los estudios radiológicos. La radiografía de tórax es el estudio inicial en la valoración de pacientes en quienes se sospecha neumomediastino (Figura 1). La radiografía de tórax habitualmente es suficiente para el diagnóstico (aproximadamente en un 69 % de los casos). La delimitación de las estructuras anatómicas normales del mediastino por el aire extraluminal confirma el diagnóstico y determina los signos radiológicos asociados. Las interfases de la pleura mediastinal con el aire mediastinal y el aire pulmonar adyacente permiten delimitar la pleura mediastinal como una línea radio-opaca fina, lateral a la arteria pulmonar y al arco aórtico. El aire adyacente a los troncos supra-aórticos hace posible la visualización de las paredes de estas estructuras vasculares, lo que se conoce como el signo de la “arteria tubular”.
De manera similar, la definición de la pared de los bronquios centrales se denomina signo de la “doble pared bronquial”. Cuando el aire rodea la arteria pulmonar y sus ramas principales se produce un anillo de aire alrededor de esta estructura, que se hace más evidente cuando el aire rodea el segmento mediastinal. La delimitación de la cara superior diafragmática se conoce como el signo del “diafragma continuo”. Otros signos de neumomediastino son: la “V de Naclerio” que ocurre cuando el aire delimita el margen lateral de la aorta descendente extendiéndose lateralmente entre la pleura parietal y la parte medial del hemidiafragma izquierdo y el signo de la “V”, que se da cuando el aire diseca la confluencia de los troncos venosos. En población infantil, la presencia de aire mediastinal desplaza el timo lateralmente y produce el signo denominado “alas de ángel”. La extensión apical del aire mediastinal genera el signo del “casquete apical radiolúcido” y puede confundirse con neumotórax.
La radiografía de tórax habitualmente es suficiente para el diagnóstico de Neumomediastino (aproximadamente en un 69 % de los casos)
Tratamiento
El tratamiento de Neumomediastino es conservador, con analgesia oral y reposo
El tratamiento es conservador, con analgesia oral y reposo. Se espera a que el neumomediastino se reabsorba lentamente con el reposo(8). En algunos centros se emplea oxigenoterapia para favorecer la reabsorción aérea, aunque no es necesario si el paciente presenta buena oxigenación. La utilización de laxantes forma parte de uno de los posibles tratamientos al alta, se aconseja el uso de laxantes los días siguientes al alta hospitalaria para evitar aumentos de presión torácica con la defecación. La ventilación mecánica no invasiva, no es la mejor opción para mantener una adecuada ventilación. Recordemos que el intercambio gaseoso, no suele alterarse en estos casos.
Nuestros datos sugieren que los pacientes con neumomediastino espontáneo que tienen buen aspecto clínico pueden ser tratados de forma conservadora con observación clínica, evitando la exposición a radiación y procedimientos invasivos.
Tablas y figuras caso 2
Tabla I. Diagnóstico diferencial del dolor torácico
Fuente: Rev Pediatr Aten Primaria. 2022;24:e37-e44. https://pap.es.
Tabla II Motivos más frecuentes y causas de dolor torácico en atención primaria
Fuente: Rev Pediatr Aten Primaria. 2022;24:71-4. https://pap.es.
Tabla III. Diagnóstico diferencial según el origen
Fuente: Campbell S, Vargas SA, Gómez JM, Escobar AE, Muñoz JK. Síndrome de Hamman. Acta Med Colomb. 2016; 41:206-10.
Figura 1. Rx de tórax donde se aprecia enfisema subcutáneo
Fuente: Elaboración propia.
Caso clínico 3. Crisis asmática. ¿Por qué no mejora?
El reconocimiento precoz de la crisis asmática y su tratamiento ayuda a disminuir la morbilidad y mortalidad
Las crisis asmáticas representan una causa frecuente de asistencia tanto a los centros de atención primaria como a las urgencias hospitalarias. Suponen alrededor del 5 % de los motivos de consulta, alcanzando cifras cercanas al 15 % durante los meses otoñales. Son frecuentes las guías de diagnóstico y tratamiento y se han elaborado documentos de consenso entre las distintas sociedades científicas que ayudan a una orientación en la práctica diaria de niños y adolescentes. La exacerbación (agudización, ataque o crisis) es un episodio en el que se manifiestan o empeoran los síntomas de asma habituales del paciente. El reconocimiento precoz y su tratamiento ayuda a disminuir la morbilidad y mortalidad. La evaluación inicial a través de los hallazgos de la exploración física y de los factores de riesgo nos ayudará a evaluar la gravedad de la crisis.
El TEP (triángulo de evaluación pediátrica) junto con la escalas de gravedad como el Pumonary Score y la saturación de oxígeno, nos ayudarán a decidir el tratamiento adecuado, cuyo objetivo será revertir de forma rápida la obstrucción al flujo aéreo. El tratamiento con oxígeno, los agonistas selectivos de receptores β2 adrenérgicos de acción corta tanto inhalados como nebulizados y los glucocorticoides representan las base generalizada del tratamiento de las crisis asmáticas(1).
Anamnesis: Varón de 12 años que acude al centro de salud como urgencia, porque según la madre tiene tos y está fatigado. Comenzó hace 24 horas con tos y dificultad respiratoria que ha ido aumentando de forma progresiva y le notan con fiebre (Tª 37.5 axilar). Como antecedente refiere que estuvo el día anterior en un apartamento que estaba cerrado.
Antecedentes personales: Asma alérgico: ácaros, pelo de perro y gato. Lleva tratamiento de base con budesonida y montelukast, controlado en consultas externas de neumología pediátrica del hospital.
Antecedentes familiares: Padre asmático, madre rinitis alérgica.
Exploración física: A su llegada al centro de salud se traslada al área de triaje de enfermería, se registra un TEP alterado por la dificultad respiratoria. En la evaluación inicial está consciente, buena coloración piel y mucosas. Tiraje intercostal, FR 39 rpm, FC: 125 lpm, Sat O2: 92 %, Peso 30 kg.
ACP sibilantes espiratorios bilaterales. El pediatra solicita al residente que le acompaña que realice el Pulmonary Score, obteniendo una puntuación de 6 que junto a la sat O2 da una valoración de gravedad moderada. Con esta puntuación se decide administrar el siguiente tratamiento: salbutamol nebulizado cada 20 minutos hasta 3 dosis: 0,15 mg/kg (0,9 ml) + 1 ampolla de 500 µgr de bromuro de ipatropio + O2, según el siguiente algoritmo(2)(Figura 1).
Evolución: Se valora de nuevo tras el tratamiento de rescate: FC: 36; Sibilantes presentes en ambos hemitórax, SatO2: 92%. Pulmonary Score: 6 con respuesta incompleta.
Ante la situación clínica se decide remitir al paciente al servicio de urgencias del hospital de referencia según los siguientes criterios(3):
Todas las crisis graves. Con riesgo de la parada cardiorrespiratoria. Con respuesta incompleta o mala al tratamiento. Todas las crisis moderadas y graves asociadas a factores de riesgo de sufrir un episodio fatal. Todas las crisis moderadas con mala respuesta al tratamiento.
Se remite al hospital con un SAMU. A su llegada tras ser valorado se administra tratamiento de rescate presentando una mejora de su score y una SatO2 96 %. Como pruebas complementarias se realiza una radiografía de tórax: sin hallazgos patológicos. Queda en observación 6 horas. No presenta alteración score y con saturación 97 %, es dado de alta para control por su pediatra.
A los 7 días acude de nuevo al Centro de Salud, presentando la misma clínica con un Pulmonary Score de 6. Es tratado de la misma forma: Salbutamol nebulizado cada 20 minutos hasta 3 dosis: 0,15 mg/kg + 2 cc de SF + bromuro de ipatropio más O2. Tras administrar la tercera dosis presenta de nuevo la misma sintomatología, no mejorando el Score. El pediatra y el residente discuten sobre que está ocurriendo y porque no mejora tras la administración de la medicación a la dosis correcta. En este momento se revisa la medicación administrada, tanto las ampollas de salbutamol como su preparación para la inhalación. Se corrige la dosificación administrando salbutamol nebulizado 4.5 ml + 1 ampolla de 500 µgr de bromuro de ipatropio + más O2.
Tras tres dosis de Salbutamol (4.5 ml) muestra un score de 3 y la saturación de O2 sube a 96 %.
Se revisó la dosificación en función de las presentaciones de salbutamol existentes en el centro de salud. Calculando la dosis por los 30 kg que pesa el niño:
- Ventolin: 0,03 ml/kg = 0,9 ml
- Salbuair (2,5 mg/2,5 ml) : 0,15 ml/kg = 4.5 ml
- Salbuair (5 mg/2,5 ml) : 0,07 ml/kg = 2.25 ml (Tabla I)
Ante esta situación se valora lo ocurrido. Se revisó una nota enviada por la Coordinación del Centro de Salud que refería lo siguiente: La especialidad farmacéutica Ventolín solución para inhalación 5 mg/ml frasco de 10 ml se sustituyó del petitorio. Esta nueva forma de presentación de salbutamol en solución para inhalación ha sido motivo de multitud de errores de administración, ya que son ampollas unitarias para inhalación. Sin embargo, hay que hacer notar que el nuevo medicamento Salbuair tiene una concentración 5 VECES MENOR (1 mg/1 ml) que la concentración del anterior envase multidosis (5 mg/1 ml).
Diagnóstico: Error en la administración de la medicación (cambio dosificación de Ventolín a Salbuair).
Discusión del caso: Los avances en el tratamiento del asma en los últimos años han mejorado la morbididad y mortalidad, las crisis o exacerbaciones asmáticas siguen siendo la causa más común de consultas en los servicios de urgencias de pediatria(5).
El 30 % de los niños tratados por crisis asmáticas en las UE tienen que ser hospitalizados por fracaso del tratamiento
Cerca de dos millones de niños consultan anualmente por asma aguda y un 20 % de ellos recaen y requieren una nueva visita a los servicios de urgencias en las tres semanas siguientes(6) ; y el 30 % de los niños tratados por crisis asmáticas en las UE tienen que ser hospitalizados por fracaso del tratamiento(7). En general y en cualquier nivel de atención, antes de que el paciente reciba el tratamiento específico para el asma aguda, es fundamental evaluar la gravedad del cuadro.
Las crisis asmáticas en el adolescente son una causa frecuente en atención primaria también, las guías clínicas nos orientan hacia el tratamiento adecuado con la sintomatología y la gravedad, las medidas terapéuticas en el ámbito prehospitalario son en muchas ocasiones las mismas que en las puertas de urgencias. En nuestro caso coincidió con el cambio en la forma de presentación de un fármaco fundamental en el tratamiento y la respuesta clínica. Se debe estar pendiente de los cambios en las formulaciones de las distintas presentaciones de los fármacos, para no inducir errores que alteren el curso evolutivo de la enfermedad. Revisar constantemente los protocolos de actuación de las crisis asmáticas y sus criterios de remisión al hospital forma parte del buen hacer de los profesionales, indistintamente del lugar donde estén ejerciendo su profesión.
Se debe estar pendiente de los cambios en las formulaciones de las distintas presentaciones de los fármacos, para no inducir errores que alteren el curso evolutivo de la enfermedad
Tablas y figuras caso 3
Tabla I. Dosis recomendadas para los principales medicamentos utilizados en la crisis de asma
Fuente: Moral Gil L, Asensi Monzó M, Juliá Benito JC, Ortega Casanueva C, Paniagua Calzón NM, Pérez García MI, Rodríguez Fernández-Oliva CR, Sanz Ortega J, Valdesoiro Navarrete L, Valverde Molina J. Asma en pediatría. Consenso regAp [Internet]. Alicante (España): Luis Moral; 2021.
Figura 1. Algoritmo de tratamiento de crisis asmática en Atención Primaria
SABA: agonista β2 de corta acción. MDI: inhalador dosis media.
Fuente: Guía de práctica clínica del asma infantil en Atención Primaria. En: https://neumoped.org/wp-content/uploads/2019/07/GUIA-ASMA-PEDIATRIA-2019.pdf.
Figura 2. Guía Gema 5.3
SABA: agonista β2 de corta acción.
Bibliografía de intoxicación por antidepresivos tricíclicos
1. Fernández Salvatierra L. Intoxicación por antidepresivos tricíclicos. Revista Médica Electrónica PortalesMedicos.com. Mayo 2016. https://www.revista-portalesmedicos.com/revista-medica/intoxicacion-antidepresivos-triciclicos/.
2. 2009 Annual Report of the American Association of Poison Control Centers’ National Poison Data System (NPDS): 27th Annual Report. Clinical Toxicology 2010; 48: 979-1178.
3. Mintegui S. Intoxicaciones medicamentosas. En Protocolos diagnóstico-terapéuticos de Urgencias Pediátricas SEUP-AEP. Capítulo 17. 2ª edición. Madrid: Ergon, 2010. p. 145-151.
4. Herranz Aguirre M, Clerigué Arrieta N. Intoxicaciones por psicofármacos. En: Mintegui S (ed.). Manual de intoxicaciones en Pediatría. 3.ª edición. Madrid: Ergón; 2012. p. 167-184).
5. Montenegro Apraez A, López Calvache MF. Intoxicación por antidepresivos tricíclicos. Urgentia, R. Int. Med. Emergencias, 1(4): 23-27, octubre – diciembre, 2015.
6. Acuña JP. Intoxicaciones graves por psicofármacos. Rev. Med. Clin. Condes .2011; 22(3): 332-339.
7. Peña LM, Zuluaga AF. Protocolos de manejo del paciente intoxicado. 2012. Disponible en: https://www.dssa.gov.co/index.php/descargas/1016-protocolos-manejode-intoxicados-versionabreviada%202011/file. Acceso 17/05/2015.
8. Woolf AD, Erdman AR, Nelson LS, Caravati EM, Cobaugh DJ, Booze LL, et al. Tricyclic antidepressant poisoning: an evidence-based consensus guideline for out-of-hospital management. Clin Toxicol (Phila) 2007; 45(3): 203-233.
9. Boehnert MT, Lovejoy FH. Value of the QRS Duration versus the Serum Drug Level in Predicting Seizures and Ventricular Arrhythmias after an Acute Overdose of Tricyclic Antidepressants. N Engl J. Med 1985 08/22; 2015/06; 313(8): 474-479.
10. Liisanantti J, Kaukoranta P, Martikainen M, Ala-Kokko T. Aspiration pneumonia following severe self-poisoning. Resuscitation 2003 1; 56(1): 49-53.
11. Woolf AD, Erdman AR, Nelson LS, Caravati EM, Cobaugh DJ, Booze LL, et al. Tricyclic antidepressant poisoning: an evidence-based consensus guideline for out-of-hospital management. Clin Toxicol (Phila) 2007; 45(3): 203-233.
12. Roldan Ovalle T, López Millan A. Intoxicación por antidepresivos tricíclicos en pediatría: aproximación y manejo. 2012 enero-marzo, 2013; 1(59): 79-91.
13. Body R, Bartram T, Azam F, Mackway-Jones K. Guidelines in Emergency Medicine Network (GEMNet): guideline for the management of tricyclic antidepressant overdose. Emerg Med J 2011 Apr; 28(4): 347-368.
14. Vasquez V, Lara B, Basauri S. Intoxicación por antidepresivos tricíclicos. ARS medica (Santiago) 48.1 (2023): 31-38.
15. Miura, N, Saito, T, Taira, T, Umebachi R & Inokuchi S (2015). Risk factors for QT prolongation associated with acute psychotropic drug overdose. The American journal of emergency medicine 33, 142–149.
16. Zellner T, Prasa D, Färber E, Hoffmann-Walbeck P, Genser D & Eyer F. (2019) The Use of Activated Charcoal to Treat Intoxications. Dtsch Arztebl Int. 3, 116:311-317.
Bibliografía de dolor torácico
- Cava JR, Sayger PL. Chest pain in children and adolescents. Pediatr Clin North 2004;51(6):1553-68.
- Guixeres Esteve T, Moriano Gutiérrez A, Insa Albert B. Guía de Algoritmos en Pediatría de Atención Primaria. Dolor torácico. AEPap. 2015 (en línea).Disponible en algoritmos.aepap.org.
- Gómez Tena G, Curto Simón B, Janer Subías E, Tello Martín A. Neumomediastino espontáneo: ¿más frecuente de lo que pensamos? Rev Pediatr Aten Primaria 201618(72): 341-343.
- López Matiacci MM, Zafra Anta MA, Penela Vélez de Guevara MT, Mohedas Tamayo AI. Adolescente con fiebre y dolor torácico. El abordaje de siempre; pero lo ya conocido a veces sorprende. Rev Pediatr Aten Primaria. 2022;24:71-4.
- Karen L. Morcillo, Ernesto L. Vallejob. Síndrome de Hamman: presentación de dolor torácico en un adolescente. En: Rev Colomb Cardiol. 2015;22(1):62-65.
- Selbst, Steven M. Abordaje del niño con dolor en el pecho. Clínicas Pediátricas 57.6 (2010): 1221-1234.
- Thull-Freedman, J. Evaluación del dolor torácico en el paciente pediátrico. Clínicas Médicas 94.2 (2010): 327-347.
- Noorbakhsh KA, Williams AE, Langham JJ, Wu L, Krafty RT, Furtado AD, Manole, M. D. (2021). Management and outcomes of spontaneous pneumomediastinum in children. Pediatric emergency care, 37(12), e1051-e1056.
- Gasser, Celine Rey-Bellet, Rachel Pellaton, and Cosette Pharisa Rochat. Pediatric spontaneous pneumomediastinum: narrative literature review. Pediatric emergency care 33.5 (2017): 370-374.
Bibliografía de crisis asmática
- Moral Gil L, Asensi Monzó M, Juliá Benito JC, Ortega Casanueva C, Paniagua Calzón NM, Pérez García MI, Rodríguez Fernández-Oliva CR, Sanz Ortega J, Valdesoiro Navarrete L, Valverde Molina J. Asma en pediatría. Consenso regAp [Internet]. Alicante (España): Luis Moral; 2021.
- Hernández Pombo G, Carrasco Azcona MA, Martínez Virumbrales L, Asensi M. Crisis asmática, abordaje y tratamiento desde la Atención Primaria. Protocolos del GVR. Disponible en: https://www.respirar.org/index.php/grupo-vias-respiratorias/protocolos.
- Paniagua Calzón N, Benito Fernández J. Diagnóstico y tratamiento de la crisis asmática en Urgencias. En: Protocolos diagnósticos y terapéuticos en urgencias de pediatría. SEUP. 3ª edición.2019.
- García Gijón C, Muñoz Aranda Á, Blázquez Gómez CJ. Dolor torácico durante un rescate farmacológico de un broncoespasmo agudo, ¿cómo actuar? Pediatr Integral 2021; XXV (2): 110.e1 – 110.e8.
- Schuh S, Johnson D, Stephens D, Callahan S, Canny G..Hospitalization patterns in severe acute asthma in children. Pediatr Pulmonol, 23 (1997), pp. 184-92.
- Mannino DM, Homa DM, Akinbami LJ, Moorman JE, Gwynn C, Redd SC. Surveillance for asthma United States, 1980-1999. MMWR Surveill Summ, 51 (2002), pp. 1-13.
- Canny GJ, Reisman J, Healy R, Schwartz C, Petrou C, Rebuck AS, et al. Acute asthma: observations regarding the management of a pediatric emergency room. Pediatrics, 83 (1989), pp. 507-12.
No existen conflictos de interés en la realización de este artículo.
Taller de urgencias en la adolescencia